Изотопная маркировка (или изотопная маркировка ) — это метод, используемый для отслеживания прохождения изотопа ( атома с обнаруживаемым изменением числа нейтронов ) через химическую реакцию , метаболический путь или биологическую клетку . [1] Реагент «маркируется» путем замены одного или нескольких конкретных атомов их изотопами . Затем реагенту дают возможность вступить в реакцию. Положение изотопов в продуктах измеряется, чтобы определить, какую последовательность изотопный атом следовал в реакции или метаболическом пути клетки. Нуклиды , используемые при изотопной маркировке, могут быть стабильными нуклидами или радионуклидами . В последнем случае мечение называется радиомечением .
При изотопной маркировке существует несколько способов обнаружения присутствия меченых изотопов; через их массу , колебательный режим или радиоактивный распад . Масс-спектрометрия обнаруживает разницу в массе изотопа, а инфракрасная спектроскопия обнаруживает разницу в колебательных модах изотопа. Ядерный магнитный резонанс обнаруживает атомы с разными гиромагнитными отношениями. Радиоактивный распад можно обнаружить с помощью ионизационной камеры или авторадиограммы гелей.
Примером использования изотопной метки является исследование фенола (C 6 H 5 OH) в воде путем замены обычного водорода ( протия ) на дейтерий ( дейтериевая метка ). При добавлении фенола к дейтерированной воде (воде, содержащей D 2 O помимо обычной H 2 O ) в гидроксильной группе фенола наблюдается замещение водорода дейтерием (приводящее к C 6 H 5 OD), что указывает на то, что фенол легко подвергается реакции водородного обмена с водой. Затрагивается только гидроксильная группа, что указывает на то, что остальные 5 атомов водорода в реакциях обмена не участвуют. [ нужна цитата ]

Изотопный индикатор (также «изотопный маркер» или «изотопная метка») используется в химии и биохимии , чтобы помочь понять химические реакции и взаимодействия. В этом методе один или несколько атомов интересующей молекулы заменяются атомом того же химического элемента , но другого изотопа (например, радиоактивного изотопа, используемого при радиоактивном отслеживании ). Поскольку меченый атом имеет такое же количество протонов, он будет вести себя почти точно так же, как и его немеченый аналог, и, за некоторыми исключениями, не будет мешать исследуемой реакции. Однако разница в количестве нейтронов означает, что его можно обнаружить отдельно от других атомов того же элемента.
Ядерный магнитный резонанс (ЯМР) и масс-спектрометрия (МС) используются для исследования механизмов химических реакций. ЯМР и МС обнаруживают изотопные различия, что позволяет определить информацию о положении меченых атомов в структуре продуктов. Имея информацию о расположении изотопных атомов в продуктах, можно определить путь реакции, который исходные метаболиты используют для превращения в продукты. Радиоактивные изотопы можно исследовать с помощью авторадиограмм гелей при гель-электрофорезе . Излучение соединений, содержащих радиоактивные изотопы, затемняет кусок фотопленки , фиксируя положение меченых соединений относительно друг друга в геле.
Изотопные индикаторы обычно используются в виде соотношений изотопов. Изучая соотношение между двумя изотопами одного и того же элемента, мы избегаем эффектов, связанных с общим содержанием элемента, которые обычно подавляют гораздо меньшие вариации содержания изотопов. Изотопные индикаторы являются одними из наиболее важных инструментов в геологии , поскольку их можно использовать для понимания сложных процессов смешивания в земных системах. Дальнейшее обсуждение применения изотопных индикаторов в геологии рассматривается в разделе изотопной геохимии .
Изотопные индикаторы обычно подразделяют на две категории: индикаторы стабильных изотопов и индикаторы радиогенных изотопов. Индикаторы стабильных изотопов включают только нерадиогенные изотопы и обычно зависят от массы. Теоретически в качестве изотопного индикатора можно использовать любой элемент с двумя стабильными изотопами. Однако наиболее часто используемые индикаторы стабильных изотопов включают относительно легкие изотопы, которые легко подвергаются фракционированию в природных системах. См. также изотопную подпись . Радиогенный изотоп-индикатор [3] включает в себя изотоп, образующийся в результате радиоактивного распада , который обычно находится в соотношении с нерадиогенным изотопом (содержание которого в Земле не меняется из-за радиоактивного распада).
Маркировка стабильными изотопами предполагает использование нерадиоактивных изотопов , которые могут выступать в качестве индикаторов, используемых для моделирования нескольких химических и биохимических систем. Выбранный изотоп может действовать как метка на этом соединении, которую можно идентифицировать с помощью ядерного магнитного резонанса (ЯМР) и масс-спектрометрии (МС). Некоторыми из наиболее распространенных стабильных изотопов являются 2 H, 13 C и 15 N, которые в дальнейшем можно производить в растворителях ЯМР , аминокислотах , нуклеиновых кислотах , липидах , обычных метаболитах и средах для роста клеток . [5] Соединения, полученные с использованием стабильных изотопов, определяются либо по процентному содержанию меченых изотопов (т.е. 30% однородно меченной глюкозы 13 C содержат смесь, которая на 30% мечена изотопом углерода 13 и 70% естественно меченного углерода), либо по конкретному меченые положения углерода в соединении (т.е. 1-13 C -глюкоза, которая мечена в первом положении углерода глюкозы).
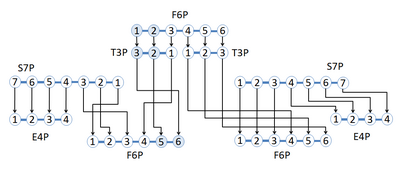
Показана сеть реакций, заимствованная из пути гликолиза и пентозофосфатного пути, в которой меченый изотоп углерода перестраивается в разные положения углерода по всей сети реакций. Сеть начинается с фруктозо-6-фосфата (F6P), который имеет 6 атомов углерода с меткой 13 C в положениях углерода 1 и 2. 1,2-13 C F6P превращается в два глицеральдегид-3-фосфата (G3P), один 2,3 - 13 С Т3П и один немеченый Т3П. 2,3-13 C T3P теперь может вступать в реакцию с седогептулозо - 7-фосфатом (S7P) с образованием немеченого эритрозо-4-фосфата (E4P) и 5,6-13 C F6P. Немеченый T3P будет реагировать с S7P с образованием немеченых продуктов. [4] На рисунке показано использование мечения стабильными изотопами для обнаружения перегруппировки атомов углерода посредством реакций с использованием соединений, меченных в определенном положении.

Анализ метаболических потоков (MFA) с использованием мечения стабильными изотопами является важным инструментом для объяснения потока определенных элементов через метаболические пути и реакции внутри клетки . В клетку вводят изотопную метку, затем клетке дают возможность расти, используя меченый корм. Для анализа стационарного метаболического потока клетка должна достичь устойчивого состояния (изотопы, поступающие и покидающие клетку, остаются постоянными во времени) или квазистационарного состояния (стационарное состояние достигается в течение заданного периода времени). [6] Определен изотопный состав выходного метаболита . Выходная изотопная картина предоставляет ценную информацию, которую можно использовать для определения величины потока и скорости превращения реагентов в продукты в каждой реакции. [7]
На рисунке продемонстрирована возможность использования разных меток для определения потока через определенную реакцию. Предположим, что исходный метаболит, трехуглеродное соединение, обладает способностью либо расщепляться на двухуглеродный метаболит и один углеродный метаболит в одной реакции, а затем рекомбинировать, либо оставаться трехуглеродным метаболитом. Если в реакции участвуют два изотопа метаболита в равных пропорциях, один полностью меченый (синие кружки), обычно известный как равномерно меченный, и один полностью немеченый (белые кружки). Путь в левой части диаграммы не показывает никаких изменений в метаболитах, тогда как правая часть показывает расщепление и рекомбинацию. Как показано, если метаболит идет только по левой стороне, соотношение равномерно меченого и немеченого метаболита остается 50–50. Если метаболит принимает только правую сторону, могут возникнуть новые модели маркировки, причем все в равной пропорции. Другие пропорции могут иметь место в зависимости от того, какая часть исходного метаболита следует по левой стороне пути, а какая по правой стороне пути. Здесь пропорции показаны для ситуации, когда половина метаболитов занимает левую сторону, а половина — правую, но могут иметь место и другие пропорции. [8] Эти структуры меченых и немеченых атомов в одном соединении представляют собой изотопомеры . Измеряя распределение изотопомеров метаболитов, меченных по-разному, можно определить поток через каждую реакцию. [9]
MFA объединяет данные, полученные в результате мечения изотопов, со стехиометрией каждой реакции, ограничениями и процедурой оптимизации, позволяющей получить карту потоков. Необратимые реакции обеспечивают термодинамические ограничения, необходимые для определения потоков. Строится матрица , содержащая стехиометрию реакций. Внутриклеточные потоки оцениваются с помощью итерационного метода , в котором смоделированные потоки включаются в стехиометрическую модель. Смоделированные потоки отображаются на карте потоков, которая показывает скорость превращения реагентов в продукты для каждой реакции. [7] На большинстве карт потоков чем толще стрелка, тем больше значение потока реакции. [10]
Можно использовать любой метод измерения разницы между изотопомерами . Два основных метода, ядерный магнитный резонанс (ЯМР) и масс-спектрометрия (МС), были разработаны для измерения массы изотопомеров при мечении стабильных изотопов.
Протонный ЯМР был первым методом, использованным для экспериментов по мечению 13 C. Используя этот метод, каждую позицию протонированного углерода внутри определенного пула метаболитов можно наблюдать отдельно от других позиций. [11] Это позволяет узнать процентное содержание изотопомеров, меченных в этом конкретном положении. Ограничением протонного ЯМР является то, что если в метаболите имеется n атомов углерода, может быть только не более n различных значений позиционного обогащения, что составляет лишь небольшую часть общей информации об изотопомере. Хотя использование маркировки протонным ЯМР ограничено, эксперименты с чистым протонным ЯМР гораздо легче оценить, чем эксперименты с большим количеством информации об изотопомерах.
Помимо протонного ЯМР , использование методов ЯМР 13 С позволит более детально рассмотреть распределение изотопомеров. Меченый атом углерода будет производить разные сигналы сверхтонкого расщепления в зависимости от состояния мечения его прямых соседей в молекуле. [11] Синглетный пик возникает, если соседние атомы углерода не помечены. Дублетный пик возникает, если помечен только один соседний атом углерода. Размер расщепления дублета зависит от функциональной группы соседнего атома углерода. Если два соседних атома углерода помечены, дублет дублетов может выродиться в триплет, если расщепления дублетов равны.
Недостатком использования методов ЯМР для анализа метаболических потоков является то, что они отличаются от других приложений ЯМР, поскольку это довольно специализированная дисциплина. ЯМР-спектрометр может быть доступен не всем исследовательским группам. Оптимизация параметров измерений ЯМР и правильный анализ структур пиков требуют квалифицированного специалиста по ЯМР. Для некоторых метаболитов также могут потребоваться специальные процедуры измерения для получения дополнительных данных по изотопомерам. Кроме того, необходимы специально адаптированные программные средства для определения точного количества площадей пиков, а также выявления разложения запутанных синглетных, дублетных и триплетных пиков.
В отличие от ядерного магнитного резонанса, масс-спектрометрия (МС) является еще одним методом, который более применим и чувствителен к экспериментам по анализу метаболических потоков. Инструменты MS доступны в различных вариантах. В отличие от двумерного ядерного магнитного резонанса ( 2D-ЯМР ), приборы МС работают непосредственно с гидролизатом . [11]
При газовой хроматографии-масс-спектрометрии ( ГХ-МС ) МС соединяется с газовым хроматографом для разделения соединений гидролизата. Соединения, элюируемые из колонки ГХ, затем ионизируются и одновременно фрагментируются. Преимущество использования ГХ-МС заключается в том, что измеряются не только массы изотопомеров молекулярного иона, но и массовый изотопомерный спектр нескольких фрагментов, что значительно увеличивает измеряемую информацию.
В жидкостной хроматографии-масс-спектрометрии ( ЖХ-МС ) ГХ заменяется жидкостным хроматографом. [12] Основное отличие состоит в том, что химическая дериватизация не требуется. Однако применение ЖХ-МС для МФА встречается редко.
В каждом случае приборы МС делят определенное распределение изотопомера по его молекулярной массе. Все изотопомеры конкретного метаболита, содержащие одинаковое количество меченых атомов углерода, собираются в один пик сигнала. Поскольку каждый изотопомер вносит вклад ровно в один пик в спектре МС, процентное значение затем можно рассчитать для каждого пика, получив массовую долю изотопомера. [11] Для метаболита с n атомами углерода производится n+1 измерений. После нормализации остается ровно n информативных масс изотопомеров. [11]
Недостатком использования методов МС является то, что для газовой хроматографии образец необходимо подготовить путем химической дериватизации, чтобы получить молекулы с зарядом. Существует множество соединений, используемых для дериватизации образцов. Диметилацеталь N,N-диметилформамида (DMFDMA) [13] и N-(трет-бутилдиметилсилил)-N-метилтрифторацетамид (MTBSTFA) [14] являются двумя примерами соединений, которые использовались для получения производных аминокислот.
Кроме того, наблюдаемые сильные изотопные эффекты влияют на время удерживания по-разному меченых изотопомеров в колонке ГХ. Также необходимо предотвратить перегрузку колонки ГХ. [14]
Наконец, естественное содержание других атомов, помимо углерода, также приводит к нарушению массового спектра изотопомеров. Например, каждый атом кислорода в молекуле может также присутствовать как изотоп 17 O и как изотоп 18 O. Более существенное влияние естественного содержания изотопов оказывает влияние кремния с естественным содержанием изотопов 29 Si и 30 Si. Si используется в производных агентов для методов МС. [11]
Радиоизотопная маркировка — это метод отслеживания прохождения образца вещества через систему. Вещество «маркируется» включением в его химический состав радионуклидов . Когда они распадаются , их присутствие можно определить, обнаружив испускаемое ими излучение . Радиоизотопная маркировка представляет собой особый случай изотопной маркировки.
Для этих целей особенно полезным типом радиоактивного распада является эмиссия позитронов . Когда позитрон сталкивается с электроном, он испускает два фотона высокой энергии , движущихся в диаметрально противоположных направлениях. Если позитрон создается внутри твердого объекта, он, скорее всего, сделает это, прежде чем пролетит более миллиметра. [ нужна цитация ] Если оба этих фотона могут быть обнаружены, место распада может быть определено очень точно.
Строго говоря, к радиоизотопной маркировке относятся лишь случаи, когда радиоактивность вводится экспериментаторами искусственно, однако некоторые природные явления позволяют провести аналогичный анализ. В частности, радиометрическое датирование использует тесно связанный принцип.
Впервые об использовании индикаторов стабильных изотопов для изучения минерального питания и обмена веществ у человека было сообщено в 1960-х годах. [15] Хотя радиоизотопы использовались в исследованиях питания человека в течение нескольких десятилетий до этого, стабильные изотопы представляли собой более безопасный вариант, особенно для субъектов, в отношении которых существует повышенная обеспокоенность по поводу радиационного воздействия, например, беременных и кормящих женщин и детей. Другие преимущества, предлагаемые стабильными изотопами, включают возможность изучать элементы, не имеющие подходящих радиоизотопов, и изучать долговременное поведение индикаторов. [16] [17] Таким образом, использование стабильных изотопов стало обычным явлением с увеличением доступности изотопно-обогащенных материалов и неорганических масс-спектрометров. Использование стабильных изотопов вместо радиоизотопов имеет несколько недостатков: требуются большие количества индикатора, который может нарушить естественно существующий минерал; подготовка аналитических проб более сложна, а оборудование для масс-спектрометрии более дорогое; присутствие индикатора во всем организме или в отдельных тканях невозможно измерить внешним способом. [18] Тем не менее, преимущества преобладали, сделав стабильные изотопы стандартом в исследованиях на людях.
Большинство минералов, которые необходимы для здоровья человека и представляют особый интерес для исследователей в области питания, содержат стабильные изотопы, некоторые из которых хорошо подходят в качестве биологических индикаторов из-за их низкой естественной распространенности. [16] [18] Железо , цинк , кальций , медь , магний , селен и молибден входят в число важнейших минералов, имеющих стабильные изотопы, к которым применялись методы изотопного индикатора. В частности, активно изучались железо, цинк и кальций.
Изучаемые аспекты минерального питания/обмена веществ включают всасывание (из желудочно-кишечного тракта в организм), распределение, хранение, выведение и кинетику этих процессов. Изотопные индикаторы вводятся субъектам перорально (с пищей или без нее, или с минеральной добавкой) и/или внутривенно. Затем измеряют обогащение изотопов в плазме крови, эритроцитах, моче и/или фекалиях. [19] [20] Обогащение также измерялось в грудном молоке [21] и содержимом кишечника. План эксперимента с индикаторами иногда различается для разных минералов из-за различий в их метаболизме. Например, абсорбцию железа обычно определяют по включению индикатора в эритроциты, тогда как абсорбцию цинка или кальция измеряют по появлению индикатора в плазме, моче или кале. [22] [23] Введение нескольких изотопных индикаторов в одном исследовании является обычным явлением, что позволяет использовать более надежные методы измерения и одновременно исследовать несколько аспектов метаболизма.
Измерение абсорбции минералов из рациона, часто называемое биодоступностью , является наиболее распространенным применением методов изотопных индикаторов в исследованиях питания. Среди целей таких исследований - изучение того, как на всасывание влияет тип пищи (например, растительное или животное происхождение, грудное молоко или смесь), другие компоненты диеты (например, фитаты ), заболевания и метаболические нарушения (например, кишечная дисфункция, связанная с окружающей средой). ), репродуктивный цикл, количество минералов в рационе, хронический дефицит минералов , возраст субъекта и гомеостатические механизмы. Когда результаты таких исследований доступны для минерала, они могут служить основой для оценки физиологических и диетических потребностей человека в этом минерале. [24] [25]
Когда индикатор вводят вместе с пищей с целью наблюдения за всасыванием и метаболизмом минералов, он может иметь форму внутренней или внешней метки. [26] [27] Внутренняя маркировка — это изотоп, который был введен в пищу во время ее производства, тем самым обогащая природный минеральный состав пищи, тогда как внешняя маркировка означает добавление индикаторного изотопа в пищу во время исследования. Поскольку это очень трудоемкий и дорогостоящий подход, внутренняя маркировка обычно не используется. Исследования, сравнивающие измерения абсорбции с использованием внутренней и внешней маркировки различных пищевых продуктов, в целом продемонстрировали хорошее согласие между двумя методами маркировки, подтверждая гипотезу о том, что внешние и природные минералы обрабатываются одинаково в желудочно-кишечном тракте человека.
Обогащение количественно определяется путем измерения изотопных соотношений , отношения изотопа-индикатора к эталонному изотопу, с помощью масс-спектрометрии. Различные определения и расчеты обогащения были приняты разными исследователями. [28] Расчеты обогащения становятся более сложными, когда одновременно используются несколько индикаторов. Поскольку препараты обогащенных изотопов никогда не бывают изотопно чистыми, т. е. они содержат все изотопы элементов в неестественных количествах, расчеты обогащения нескольких изотопов-индикаторов должны учитывать возмущение каждого соотношения изотопов присутствием других трассеров. [28]
Из-за распространенности дефицита полезных ископаемых и его критического воздействия на здоровье и благополучие людей в странах с бедными ресурсами Международное агентство по атомной энергии недавно опубликовало подробные и всесторонние описания методов стабильных изотопов, чтобы облегчить распространение этих знаний среди исследователей за пределами западные академические центры. [22] [29]
В протеомике изучение полного набора белков , экспрессируемых геномом , выявление биомаркеров заболеваний может включать использование мечения стабильных изотопов аминокислотами в культуре клеток (SILAC), которое обеспечивает меченные изотопами формы аминокислот, используемые для оценки уровней белка. . [30] При рекомбинантных белках измененные белки производятся в больших количествах, а изотопная маркировка является инструментом для проверки соответствующих белков. Раньше метод заключался в избирательном обогащении ядер 13 C или 15 N или истощении из них 1 H. Рекомбинант будет экспрессироваться в E.coli со средой, содержащей 15 N- хлорид аммония в качестве источника азота. [31] Полученные 15 N-меченные белки затем очищают с помощью сродства к иммобилизованным металлам и оценивают их процентное содержание. Чтобы увеличить выход меченых белков и снизить стоимость меченных изотопами сред, альтернативная процедура сначала увеличивает клеточную массу с использованием немеченой среды, а затем вводит ее в минимальное количество меченой среды. [32] Еще одним применением изотопной маркировки может быть измерение синтеза ДНК, то есть пролиферации клеток in vitro . Использует маркировку H 3 -тимидина для сравнения характера синтеза (или последовательности) в клетках. [33]
Изотопные индикаторы используются для изучения процессов в природных системах, особенно в наземной и водной среде. В почвоведении трассеры 15 N широко используются для изучения круговорота азота, тогда как 13 C и 14 C, стабильные и радиоизотопы углерода соответственно, используются для изучения круговорота органических соединений и фиксации CO 2 автотрофами . Например, Марш и др. (2005) использовали мочевину, меченную двойной меткой ( 15 N- и 14 C), чтобы продемонстрировать использование соединения окислителями аммиака как в качестве источника энергии (окисление аммиака), так и в качестве источника углерода (хемоавтотрофная фиксация углерода). [34] Дейтерированную воду также используют для отслеживания судьбы и возраста воды на дереве [35] или в экосистеме. [36]
Трассеры также широко используются в океанографии для изучения широкого спектра процессов. Используемые изотопы обычно встречаются в природе и имеют хорошо известные источники и скорости образования и распада. Однако с большим успехом можно использовать и антропогенные изотопы. Исследователи измеряют соотношение изотопов в разных местах и в разное время, чтобы получить информацию о физических процессах в океане.
Океан представляет собой разветвленную сеть транспорта частиц. Изотопы тория могут помочь исследователям расшифровать вертикальное и горизонтальное движение материи. 234 Th имеет постоянную, четко определенную скорость производства в океане и период полураспада 24 дня. Было показано, что этот природный изотоп линейно меняется с глубиной. Следовательно, любые изменения этой линейной картины можно объяснить переносом 234 Th на частицах. Например, низкие соотношения изотопов в поверхностных водах с очень высокими значениями на глубине нескольких метров будут указывать на вертикальный поток в нисходящем направлении. Кроме того, изотоп тория можно проследить на определенной глубине, чтобы расшифровать латеральный перенос частиц. [37]
Циркуляцию внутри местных систем, таких как заливы, устья рек и грунтовые воды, можно исследовать с помощью изотопов радия. 223 Ra имеет период полураспада 11 дней и может встречаться в естественных условиях в определенных местах рек и источников подземных вод. Изотопное соотношение радия будет уменьшаться по мере того, как вода из реки-источника попадает в залив или устье. Измерив количество 223 Ra в различных местах, можно расшифровать схему циркуляции. [38] Тот же самый процесс можно использовать для изучения движения и сброса подземных вод. [39]
Различные изотопы свинца можно использовать для изучения циркуляции в глобальном масштабе. Различные океаны (т.е. Атлантический, Тихий, Индийский и т. д.) имеют разные изотопные характеристики. Это является результатом различий в изотопных соотношениях отложений и горных пород в разных океанах. [40] Поскольку период полураспада различных изотопов свинца составляет 50–200 лет, времени для гомогенизации изотопных соотношений во всем океане недостаточно. Таким образом, точный анализ изотопных соотношений Pb можно использовать для изучения циркуляции различных океанов. [41]
Изотопы с чрезвычайно длительным периодом полураспада и продукты их распада можно использовать для изучения многомиллионных процессов, таких как тектоника и экстремальное изменение климата. Например, при датировании рубидием-стронцием изотопное соотношение стронция ( 87 Sr/ 86 Sr) можно анализировать в кернах льда, чтобы изучить изменения на протяжении жизни Земли. Различия в этом соотношении внутри ледяного ядра могут указывать на значительные изменения в геохимии Земли. [41]
Вышеупомянутые процессы можно измерить с использованием встречающихся в природе изотопов. Тем не менее, антропогенные изотопы также чрезвычайно полезны для океанографических измерений. Испытания ядерного оружия привели к выбросу множества необычных изотопов в мировой океан. 3 H, 129 I и 137 Cs можно обнаружить в морской воде в растворенном виде, а 241 Am и 238 Pu прикреплены к частицам. Изотопы, растворенные в воде, особенно полезны при изучении глобальной циркуляции. Например, различия в латеральных соотношениях изотопов в океане могут указывать на сильные водные фронты или круговороты. [42] И наоборот, изотопы, прикрепленные к частицам, могут быть использованы для изучения переноса массы в толщах воды. Например, высокие уровни Am или Pu могут указывать на нисходящий поток, если наблюдать на больших глубинах, или на подъем, если наблюдать на поверхности. [43]
{{cite book}}: CS1 maint: multiple names: authors list (link){{cite journal}}: CS1 maint: multiple names: authors list (link){{cite book}}: CS1 maint: multiple names: authors list (link) CS1 maint: numeric names: authors list (link){{cite book}}: CS1 maint: others (link)