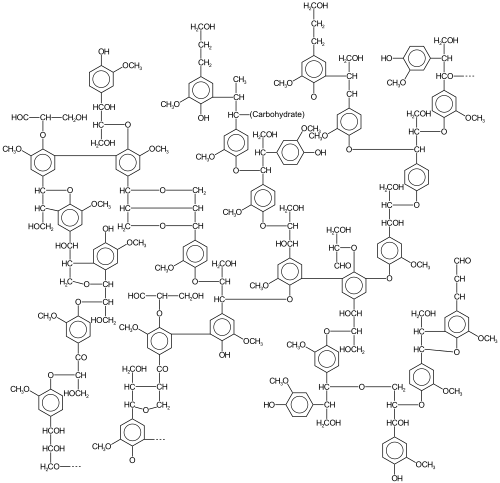
Лигнин — это класс сложных органических полимеров , которые образуют ключевые структурные материалы в опорных тканях большинства растений. [1] Лигнины особенно важны для формирования клеточных стенок , особенно в древесине и коре , поскольку они придают жесткость и не подвержены гниению . С химической точки зрения лигнины — это полимеры, полученные путем сшивания фенольных предшественников. [2]
Лигнин был впервые упомянут в 1813 году швейцарским ботаником А. П. де Кандоллем , который описал его как волокнистый, безвкусный материал, нерастворимый в воде и спирте, но растворимый в слабых щелочных растворах, и который может быть осажден из раствора с помощью кислоты. [3] Он назвал вещество «лигнин», которое происходит от латинского слова lignum , [4] означающего дерево. Это один из самых распространенных органических полимеров на Земле , уступающий только целлюлозе и хитину . Лигнин составляет 30% наземного неископаемого органического углерода [ 5] на Земле и от 20 до 35% сухой массы древесины. [6]
Лигнин присутствует в красных водорослях , что предполагает, что общий предок растений и красных водорослей также синтезировал лигнин. Это открытие также предполагает, что первоначальная функция лигнина была структурной, поскольку он играет эту роль в красной водоросли Calliarthron , где он поддерживает соединения между кальцинированными сегментами. [7]
Состав лигнина варьируется от вида к виду. Пример состава образца осины [8] : 63,4% углерода, 5,9% водорода, 0,7% золы (минеральные компоненты) и 30% кислорода (по разнице), [9] что приблизительно соответствует формуле (C 31 H 34 O 11 ) n .
Лигнин представляет собой набор высокогетерогенных полимеров , полученных из нескольких исходных лигнолов. Гетерогенность возникает из-за разнообразия и степени сшивания между этими лигнолами. Лигнолы , которые сшиваются, бывают трех основных типов, все они получены из фенилпропана: конифериловый спирт (3-метокси-4-гидроксифенилпропан; его радикал G иногда называют гваяцилом), синапиловый спирт (3,5-диметокси-4-гидроксифенилпропан; его радикал S иногда называют сирингилом) и паракумариловый спирт (4-гидроксифенилпропан; его радикал H иногда называют 4-гидроксифенилом). [ необходима цитата ]
Относительные количества предшественников «мономеров» (лигнолов или монолигнолов) варьируются в зависимости от растительного источника. [5] Лигнины обычно классифицируются в соответствии с их соотношением сирингил/гваяцил (S/G). Лигнин из голосеменных растений образуется из хвойного спирта , который дает G при пиролизе. В покрытосеменных растениях часть хвойного спирта преобразуется в S. Таким образом, лигнин в покрытосеменных растениях имеет как компоненты G, так и S. [10] [11]
Молекулярные массы лигнина превышают 10 000 а.е.м. Он гидрофобен , так как богат ароматическими субъединицами. Степень полимеризации трудно измерить, так как материал неоднороден. Были описаны различные типы лигнина в зависимости от способа выделения. [12]

Многие злаки в основном содержат G, в то время как некоторые пальмы в основном содержат S. [13] Все лигнины содержат небольшое количество неполных или модифицированных монолигнолов, а другие мономеры преобладают в недревесных растениях. [14]
Лигнин заполняет пространство в клеточной стенке между целлюлозой , гемицеллюлозой и пектиновыми компонентами, особенно в сосудистых и опорных тканях: трахеидах ксилемы , сосудистых элементах и склереидных клетках. [ необходима цитата ]
Лигнин играет важную роль в проведении воды и водных питательных веществ в стеблях растений . Полисахаридные компоненты клеточных стенок растений являются высокогидрофильными и, таким образом, проницаемыми для воды, тогда как лигнин более гидрофобен . Сшивание полисахаридов лигнином является препятствием для поглощения воды клеточной стенкой. Таким образом, лигнин позволяет сосудистой ткани растения эффективно проводить воду. [15] Лигнин присутствует во всех сосудистых растениях , но не в бриофитах , что подтверждает идею о том, что изначальная функция лигнина была ограничена транспортом воды.
Он ковалентно связан с гемицеллюлозой и, следовательно, образует поперечные связи между различными растительными полисахаридами , придавая механическую прочность клеточной стенке и, следовательно, всему растению в целом. [16] Его наиболее часто упоминаемая функция — поддержка посредством укрепления древесины (в основном состоящей из клеток ксилемы и одревесневших волокон склеренхимы ) в сосудистых растениях. [17] [18] [19]
Наконец, лигнин также придает устойчивость к болезням, накапливаясь в месте проникновения патогена, делая растительную клетку менее подверженной деградации клеточной стенки. [20]

Глобальное коммерческое производство лигнина является следствием производства бумаги. В 1988 году во всем мире было произведено более 220 миллионов тонн бумаги. [21] Большая часть этой бумаги была делигнифицирована; лигнин составляет около 1/3 массы лигноцеллюлозы, предшественника бумаги. Лигнин является препятствием для производства бумаги, поскольку он окрашен, желтеет на воздухе, и его присутствие ослабляет бумагу. После отделения от целлюлозы он сжигается как топливо. Только часть используется в широком диапазоне малообъемных применений, где важна форма, а не качество. [22]
Механическая или высокопродуктивная целлюлоза , которая используется для производства газетной бумаги , все еще содержит большую часть лигнина, изначально присутствующего в древесине. Этот лигнин отвечает за пожелтение газетной бумаги со временем. [4] Высококачественная бумага требует удаления лигнина из целлюлозы. Эти процессы делигнификации являются основными технологиями бумажной промышленности, а также источником значительных экологических проблем. [ необходима цитата ]
При сульфитной варке лигнин удаляется из древесной массы в виде лигносульфонатов , для которых было предложено множество применений. [23] Они используются в качестве диспергаторов , увлажнителей , стабилизаторов эмульсий и секвестрантов ( очистка воды ). [24] Лигносульфонат также был первым семейством водоредуцирующих веществ или суперпластификаторов, которые добавлялись в 1930-х годах в качестве добавки к свежему бетону для уменьшения соотношения воды к цементу ( в/ц ), основного параметра, контролирующего пористость бетона и, следовательно, его механическую прочность , его диффузионную способность и его гидравлическую проводимость , все параметры, необходимые для его долговечности. Он применяется в экологически устойчивом пылеподавляющем средстве для дорог. Кроме того, лигнин может использоваться при изготовлении биоразлагаемого пластика вместе с целлюлозой в качестве альтернативы пластику, полученному из углеводородов, если извлечение лигнина достигается с помощью более экологически жизнеспособного процесса, чем обычное производство пластика. [25]
Лигнин, удаляемый в процессе крафт-процесса , обычно сжигается из-за его топливной ценности, обеспечивая энергией бумажную фабрику. Существуют два коммерческих процесса удаления лигнина из черного щелока для более ценных применений: LignoBoost (Швеция) и LignoForce (Канада). Лигнин более высокого качества представляет потенциал стать возобновляемым источником ароматических соединений для химической промышленности с целевым рынком более 130 млрд долларов. [26]
Учитывая, что лигнин является наиболее распространенным биополимером после целлюлозы , его исследовали в качестве сырья для производства биотоплива, и он может стать важнейшим растительным экстрактом при разработке нового класса биотоплива. [27] [28]
Биосинтез лигнина начинается в цитозоле с синтеза гликозилированных монолигнолов из аминокислоты фенилаланина . Эти первые реакции являются общими с фенилпропаноидным путем. Присоединенная глюкоза делает их водорастворимыми и менее токсичными . После транспортировки через клеточную мембрану в апопласт глюкоза удаляется, и начинается полимеризация. [29] Многое в его анаболизме не изучено даже после более чем столетия изучения. [5]

Этап полимеризации , то есть радикально-радикальное соединение, катализируется окислительными ферментами . Ферменты пероксидазы и лакказы присутствуют в стенках растительных клеток , и неизвестно, участвует ли одна или обе эти группы в полимеризации. Низкомолекулярные окислители также могут быть вовлечены. Окислительный фермент катализирует образование радикалов монолигнола . Часто говорят, что эти радикалы подвергаются некатализируемому соединению для образования лигнинового полимера . [30] Альтернативная теория подразумевает неопределенный биологический контроль. [1]
В отличие от других биополимеров (например, белков, ДНК и даже целлюлозы), лигнин устойчив к деградации. Он невосприимчив как к кислотно-, так и к щелочно-катализируемому гидролизу. Способность к деградации зависит от вида и типа растительной ткани. Например, сирингил (S) лигнин более восприимчив к деградации грибковым распадом, поскольку имеет меньше арильных связей и более низкий окислительно-восстановительный потенциал, чем гваяцильные единицы. [31] [32] Поскольку он сшит с другими компонентами клеточной стенки, лигнин минимизирует доступность целлюлозы и гемицеллюлозы для микробных ферментов, что приводит к снижению усвояемости биомассы. [15]
Некоторые лигнолитические ферменты включают гем-пероксидазы, такие как лигнинпероксидазы , марганцевые пероксидазы , универсальные пероксидазы и красители-обесцвечивающие пероксидазы , а также лакказы на основе меди . Лигнинпероксидазы окисляют нефенольный лигнин, тогда как марганцевые пероксидазы окисляют только фенольные структуры. Красители-обесцвечивающие пероксидазы, или DyPs, проявляют каталитическую активность в широком спектре модельных соединений лигнина, но их субстрат in vivo неизвестен. В целом, лакказы окисляют фенольные субстраты, но было показано, что некоторые грибковые лакказы окисляют нефенольные субстраты в присутствии синтетических окислительно-восстановительных медиаторов. [33] [34]
Хорошо изученные лигнолитические ферменты обнаружены в Phanerochaete chrysosporium [35] и других грибах белой гнили . Некоторые грибы белой гнили, такие как Ceriporiopsis subvermispora , могут разрушать лигнин в лигноцеллюлозе , но другие лишены этой способности. Большая часть деградации грибкового лигнина включает секретируемые пероксидазы . Также секретируются многие грибковые лакказы , которые облегчают деградацию соединений, полученных из фенольного лигнина, хотя также было описано несколько внутриклеточных грибковых лакказ. Важным аспектом деградации грибкового лигнина является активность вспомогательных ферментов для производства H 2 O 2 , необходимого для функционирования лигнинпероксидазы и других гемпероксидаз . [33]
Бактерии лишены большинства ферментов, используемых грибами для разложения лигнина, а производные лигнина (алифатические кислоты, фураны и солюбилизированные фенолы) подавляют рост бактерий. [36] Тем не менее, бактериальная деградация может быть довольно обширной, [37] особенно в водных системах, таких как озера, реки и ручьи, где в водные пути могут попадать материалы с суши (например, опавшие листья ). Лигнолитическая активность бактерий не была широко изучена, хотя она была впервые описана в 1930 году. Было охарактеризовано множество бактериальных DyP. Бактерии не экспрессируют ни одну из пероксидаз растительного типа (лигнинпероксидазу, Mn пероксидазу или универсальные пероксидазы), но три из четырех классов DyP встречаются только у бактерий. В отличие от грибов, большинство бактериальных ферментов, участвующих в разложении лигнина, являются внутриклеточными, включая два класса DyP и большинство бактериальных лакказ. [34]
В окружающей среде лигнин может разлагаться либо биотически с помощью бактерий, либо абиотически с помощью фотохимического изменения, и часто последнее способствует первому. [38] Помимо наличия или отсутствия света, на биоразлагаемость лигнина влияют несколько факторов окружающей среды, включая состав бактериального сообщества, минеральные ассоциации и окислительно-восстановительное состояние. [39] [40]
У корабельных червей лигнин, который они поглощают, переваривается бактериями- симбионтами « подгруппы Alteromonas » в тифлозольном суборгане слепой кишки . [41]
Пиролиз лигнина во время сжигания древесины или производства древесного угля дает ряд продуктов, из которых наиболее характерными являются метоксизамещенные фенолы . Из них наиболее важными являются гваякол и сирингол и их производные. Их присутствие может быть использовано для отслеживания источника дыма в дровяном огне. В кулинарии лигнин в форме твердой древесины является важным источником этих двух соединений, которые придают характерный аромат и вкус копченым продуктам , таким как барбекю . Основными вкусовыми соединениями копченой ветчины являются гваякол и его 4-, 5- и 6-метилпроизводные, а также 2,6-диметилфенол. Эти соединения производятся путем термического разложения лигнина в древесине, используемой в коптильне. [42]
Обычным методом количественного определения лигнина в целлюлозной промышленности является тест на лигнин Класона и кислоторастворимый лигнин, который представляет собой стандартизированные процедуры. Целлюлоза подвергается термическому расщеплению в присутствии кислоты. Остаток называется лигнином Класона. Кислоторастворимый лигнин (ASL) количественно определяется по интенсивности его ультрафиолетовой спектроскопии . Состав углеводов также может быть проанализирован из щелоков Класона, хотя могут быть продукты распада сахара (фурфурол и 5-гидроксиметилфурфурол ). [43]
Раствор соляной кислоты и флороглюцина используется для обнаружения лигнина (тест Визнера). Образуется ярко-красный цвет, обусловленный наличием в лигнине кониферальдегидных групп. [44]
Тиогликолиз — это аналитический метод количественного определения лигнина . [45] Структуру лигнина также можно изучать с помощью компьютерного моделирования. [46]
Термохемолиз (химическое расщепление вещества в вакууме и при высокой температуре) с тетраметиламмонийгидроксидом (TMAH) или оксидом меди [47] также использовался для характеристики лигнинов. Соотношение сирингиллигнола (S) к ванилиллигнолу (V) и циннамиллигнола (C) к ванилиллигнолу (V) варьируется в зависимости от типа растения и, следовательно, может использоваться для отслеживания источников растений в водных системах (древесные против недревесных и покрытосеменные против голосеменных). [48] Соотношения форм карбоновой кислоты (Ad) к альдегиду (Al) лигнолов (Ad/Al) раскрывают диагенетическую информацию, причем более высокие соотношения указывают на более сильно деградированный материал. [31] [32] Увеличение значения (Ad/Al) указывает на то, что произошла реакция окислительного расщепления боковой цепи алкиллигнина, которая, как было показано, является этапом в разложении древесины многими грибами белой гнили и некоторыми грибами мягкой гнили . [31] [32] [49] [50] [51]
Лигнин и его модели были хорошо изучены с помощью спектроскопии ЯМР 1 H и 13 C. Из-за структурной сложности лигнинов спектры плохо разрешены, а количественная оценка затруднена. [52]