Лютеинизирующий гормон ( ЛГ , также известный как лютеинизирующий гормон , [1] лютропин и иногда лютрофин [2] ) — это гормон, вырабатываемый гонадотропными клетками передней доли гипофиза . Производство ЛГ регулируется гонадотропин-рилизинг-гормоном (ГнРГ) гипоталамуса. [3] У женщин резкое повышение уровня ЛГ, известное как всплеск ЛГ , вызывает овуляцию [4] и развитие желтого тела . У мужчин, где ЛГ также называли гормоном, стимулирующим интерстициальные клетки ( ICSH ), [5] он стимулирует выработку тестостерона клетками Лейдига . [4] Он действует синергично с фолликулостимулирующим гормоном ( ФСГ ).
Термин «лютеинизирующий» происходит от латинского «luteus», что означает «желтый». Это относится к желтому телу , которое представляет собой массу клеток, которая образуется в яичнике после выхода яйцеклетки (яйцеклетки), но остается неоплодотворенной. Желтое тело названо так потому, что оно часто имеет характерный желтый цвет. Процесс формирования желтого тела известен как « лютеинизация », поэтому гормон, запускающий этот процесс, называется «лютеинизирующим» гормоном.
ЛГ представляет собой гетеродимерный гликопротеин . Каждая мономерная единица представляет собой молекулу гликопротеина ; одна альфа- и одна бета-субъединица составляют полноценный функциональный белок.
Его структура аналогична структуре других гликопротеиновых гормонов : фолликулостимулирующего гормона (ФСГ), тиреотропного гормона (ТТГ) и хорионического гонадотропина человека (ХГЧ). Димер белка содержит 2 гликопептидные субъединицы (обозначенные альфа- и бета-субъединицы), которые нековалентно связаны: [6]
Различный состав этих олигосахаридов влияет на биологическую активность и скорость разложения. Биологический период полувыведения ЛГ составляет 20 минут, что короче, чем у ФСГ (3–4 часа) и ХГЧ (24 часа). [ нужна цитация ] Биологический период полураспада ЛГ составляет 23 часа при подкожном введении [7] или терминальный период полувыведения 10-12 часов. [8]
Ген альфа- субъединицы расположен на хромосоме 6q 12.21.
Ген бета-субъединицы лютеинизирующего гормона локализован в кластере генов LHB/CGB на хромосоме 19q 13.32. В отличие от активности альфа-гена, активность гена субъединицы бета-ЛГ ограничена гонадотропными клетками гипофиза. Он регулируется гонадотропин -высвобождающим гормоном гипоталамуса . Ингибин , активин и половые гормоны не влияют на генетическую активность продукции бета-субъединицы ЛГ.

Как у мужчин, так и у женщин ЛГ воздействует на эндокринные клетки гонад, производя андрогены.
ЛГ поддерживает тека-клетки в яичниках, которые обеспечивают андрогены и гормональные предшественники для производства эстрадиола . Во время менструации ФСГ инициирует рост фолликулов , специфически воздействуя на гранулезные клетки . [9] С увеличением уровня эстрогенов рецепторы ЛГ также экспрессируются на созревающем фолликуле, что заставляет его производить больше эстрадиола . В конце концов, когда фолликул полностью созревает, всплеск выработки 17α-гидроксипрогестерона фолликулом подавляет выработку эстрогенов . Ранее предовуляторный всплеск ЛГ связывали с уменьшением эстроген-опосредованной отрицательной обратной связи ГнРГ в гипоталамусе , что впоследствии стимулировало высвобождение ЛГ из передней доли гипофиза . [10] Однако более поздние исследования связывают всплеск ЛГ с положительной обратной связью от эстрадиола после того, как выработка доминантным фолликулом превышает определенный порог. Исключительно высокие уровни эстрадиола индуцируют гипоталамусную выработку прогестерона , который стимулирует повышенную секрецию ГнРГ, вызывая всплеск ЛГ. [11] Увеличение производства ЛГ длится всего от 24 до 48 часов. Этот «выброс ЛГ» запускает овуляцию , тем самым не только высвобождая яйцеклетку из фолликула, но и инициируя преобразование остаточного фолликула в желтое тело , которое, в свою очередь, вырабатывает прогестерон для подготовки эндометрия к возможной имплантации . ЛГ необходим для поддержания лютеиновой функции в течение вторых двух недель менструального цикла. Если наступит беременность , уровень ЛГ снизится, а лютеиновая функция будет поддерживаться под действием ХГЧ ( хорионического гонадотропина человека ), гормона, очень похожего на ЛГ, но секретируемого новой плацентой.
Гонадные стероиды ( эстрогены и андрогены) обычно оказывают отрицательное влияние обратной связи на высвобождение ГнРГ-1 на уровне гипоталамуса и гонадотропных гормонов, снижая их чувствительность к ГнРГ. Положительная обратная связь с эстрогенами также возникает в гонадной оси самок млекопитающих и отвечает за выброс ЛГ в середине цикла, который стимулирует овуляцию. Хотя эстрогены ингибируют высвобождение кисспептина (Kp) из нейронов Kiss1 в ARC, эстрогены стимулируют высвобождение Kp из Kp-нейронов в AVPV. По мере постепенного повышения уровня эстрогенов преобладает положительный эффект, приводящий к всплеску ЛГ. ГАМК -секретирующие нейроны, иннервирующие нейроны ГнРГ-1, также могут стимулировать высвобождение ГнРГ-1. Эти нейроны ГАМК также обладают ЭР и могут быть ответственны за выброс ГнРГ-1. Часть ингибирующего действия эндорфинов на высвобождение GnRH-1 осуществляется за счет ингибирования этих ГАМК-нейронов. Разрыв фолликула яичника при овуляции вызывает резкое снижение синтеза эстрогенов и заметное увеличение секреции прогестерона желтым телом яичника, восстанавливая преимущественно отрицательную обратную связь на гипоталамическую секрецию ГнРГ-1. [12]
ЛГ действует на клетки Лейдига яичка и регулируется гонадотропин-высвобождающим гормоном (ГнРГ). [13] Клетки Лейдига производят тестостерон под контролем ЛГ. ЛГ связывается с рецепторами ЛГ на поверхности мембраны клеток Лейдига. Связывание с этим рецептором вызывает увеличение циклического аденозинмонофосфата (цАМФ), вторичного мессенджера, который позволяет холестерину перемещаться в митохондрии. В митохондриях холестерин превращается в прегненолон с помощью CYP11A1. [14] Прегненолон затем преобразуется в дегидроэпиандростерон (ДГЭА). [15] ДГЭА затем преобразуется в андростендион под действием 3β-гидроксистероиддегидрогеназы (3β-HSD) [16] и затем, наконец, превращается в тестостерон под действием 17β-гидроксистероиддегидрогеназы (HSD17B). Начало полового созревания контролируется двумя основными гормонами: ФСГ инициирует сперматогенез, а ЛГ сигнализирует о высвобождении тестостерона, [17] андрогена , который оказывает как эндокринную активность, так и интратестикулярную активность на сперматогенез .
ЛГ высвобождается гипофизом и контролируется импульсами гонадотропин-рилизинг гормона . Когда уровень тестостерона в крови низкий, гипофиз стимулирует выработку ЛГ. [13] По мере увеличения уровня тестостерона он будет действовать на гипофиз через петлю отрицательной обратной связи и, следовательно, ингибировать высвобождение ГнРГ и ЛГ. [18] Андрогены (включая тестостерон и дигидротестостерон ) ингибируют моноаминоксидазу (МАО) в шишковидной железе, что приводит к повышению уровня мелатонина и снижению ЛГ и ФСГ за счет мелатонин-индуцированного увеличения синтеза и секреции гонадотропин-ингибирующего гормона (ГнИГ) [19] . Тестостерон также можно ароматизировать в эстрадиол (Е2) для ингибирования ЛГ. E2 снижает амплитуду пульса и чувствительность к ГнРГ из гипоталамуса в гипофиз. [20]
Изменения уровней ЛГ и тестостерона в крови, а также пульсовой секреции вызваны изменениями сексуального возбуждения у мужчин. [21]
Рецепторы лютеинизирующего гормона расположены в областях мозга, связанных с когнитивной функцией . [22] Роль ЛГ в центральной нервной системе (ЦНС) может иметь отношение к пониманию и лечению постменопаузального снижения когнитивных функций. [23]
Недавние исследования выявили обратную зависимость между уровнями циркулирующего ЛГ и ЛГ в ЦНС. [24] После овариэктомии (процедуры, имитирующей менопаузу) у самок мышей уровень циркулирующего ЛГ резко возрастает, а уровень ЛГ в ЦНС падает. [25] Лечение, снижающее уровень циркулирующего ЛГ, восстанавливает уровни ЛГ в ЦНС. [25]
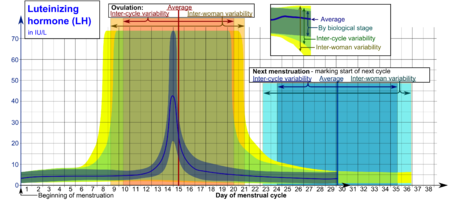
Уровни ЛГ обычно низкие в детстве , а у женщин высокие после менопаузы . Поскольку ЛГ секретируется импульсами, необходимо следить за его концентрацией в течение достаточного периода времени, чтобы получить правильную информацию о его уровне в крови.
В репродуктивный период типичные уровни составляют от 1 до 20 МЕ/л. Физиологически высокие уровни ЛГ наблюдаются во время всплеска ЛГ (vs) и обычно сохраняются в течение 48 часов.
У мужчин старше 18 лет референтный диапазон оценивается в 1,8–8,6 МЕ/л. [27]
ЛГ измеряется в международных единицах (МЕ). При количественном определении количества ЛГ в образце в МЕ важно знать, по какому международному стандарту была откалибрована ваша партия ЛГ, поскольку они могут сильно варьироваться от года к году. Для человеческого ЛГ в моче одна МЕ в последнее время определяется как 1/189 ампулы, обозначенной 96/602 и распределяемой NIBSC , что соответствует примерно 0,04656 мкг белка ЛГ на одну МЕ, но более старые стандартные версии все еще широко используются. . [28] [29]


Обнаружение всплеска выброса лютеинизирующего гормона свидетельствует о приближающейся овуляции . ЛГ можно обнаружить с помощью наборов для прогнозирования овуляции в моче (OPK, также набор для определения ЛГ), которые проводятся, как правило, ежедневно, примерно в то время, когда можно ожидать овуляции. [31] Преобразование отрицательного значения в положительное предполагает, что овуляция произойдет в течение 24–48 часов, что дает женщинам два дня для вступления в половой акт или искусственного оплодотворения с целью зачатия . [32]
Рекомендуемая частота тестирования различается у разных производителей. Например, тест Clearblue проводится ежедневно, и повышенная частота не снижает риск пропуска всплеска ЛГ. [33] С другой стороны, китайская компания Nantong Egens Biotechnology рекомендует использовать свой тест два раза в день. [34] При тестировании один раз в день не было обнаружено существенной разницы между тестированием ЛГ утром и вечером в отношении частоты зачатия, [35] и рекомендации о том, в какое время дня проводить тест, различаются у разных производителей. и работники здравоохранения. [36] Тесты можно считывать вручную, используя меняющую цвет бумажную полоску, или в цифровом виде с помощью считывающей электроники.
Тесты на лютеинизирующий гормон можно сочетать с тестами на эстрадиол в таких тестах, как монитор фертильности Clearblue . [ нужна медицинская ссылка ]
Чувствительность тестов на ЛГ измеряется в милли международных единицах , при этом обычно доступные тесты находятся в диапазоне 10–40 мкМ (чем меньше число, тем выше чувствительность). [ нужна цитата ]
Поскольку сперматозоиды могут оставаться жизнеспособными у женщины в течение нескольких дней, тесты на ЛГ не рекомендуются при использовании методов контрацепции , поскольку всплеск ЛГ обычно происходит после начала периода фертильности. [ нужна цитата ]
У детей с преждевременным половым созреванием гипофизарного или центрального происхождения уровни ЛГ и ФСГ могут находиться в репродуктивном диапазоне вместо низких уровней, типичных для их возраста.
В репродуктивном возрасте относительно повышенный уровень ЛГ часто наблюдается у пациенток с синдромом поликистозных яичников ; однако для них было бы необычно иметь уровни ЛГ, выходящие за пределы нормального репродуктивного диапазона.
Постоянно высокие уровни ЛГ указывают на ситуации, когда нормальная ограничивающая обратная связь от гонад отсутствует, что приводит к выработке гипофизом как ЛГ, так и ФСГ. Хотя это типично для менопаузы, в репродуктивном возрасте это ненормально. Там это может быть признаком:
Примечание. Медицинским препаратом для ингибирования секреции лютеинизирующего гормона является бутиназоцин . [37]
Снижение секреции ЛГ может привести к нарушению функции половых желез (гипогонадизму). Это состояние обычно проявляется у мужчин как нарушение выработки нормального количества сперматозоидов. У женщин часто наблюдается аменорея . К состояниям с очень низкой секрецией ЛГ относятся:
ЛГ доступен в смеси с ФСГ в форме менотропина и других форм мочевых гонадотропинов . Более очищенные формы гонадотропинов мочи могут снижать долю ЛГ по отношению к ФСГ. Рекомбинантный ЛГ доступен в форме лютропина альфа (Luveris). [40] Все эти лекарства следует вводить парентерально. Их обычно используют при терапии бесплодия для стимуляции развития фолликулов, особенно при ЭКО .
Часто препараты ХГЧ используются в качестве заменителей ЛГ, поскольку они активируют тот же рецептор. Используемый в медицине ХГЧ получают из мочи беременных женщин, он дешевле и имеет более длительный период полураспада, чем ЛГ.
Фосфорилирование — это биохимический процесс, который включает присоединение фосфата к органическому соединению. Стероидогенез включает в себя процессы, посредством которых холестерин превращается в биологически активные стероидные гормоны. Недавнее исследование показывает, что ЛГ через сигнальный путь PKA регулирует фосфорилирование и локализацию DRP1 в митохондриях стероидогенных клеток яичника. [41]