Потенциал клетки – это способность клетки дифференцироваться в другие типы клеток. [1] [2] Чем больше типов клеток может дифференцироваться в клетку, тем выше ее эффективность. Потенциал также описывается как потенциал активации гена внутри клетки, который, как и континуум, начинается с тотипотентности , обозначающей клетку с наибольшим потенциалом дифференцировки, плюрипотентностью , мультипотентностью , олигопотентностью и, наконец, унипотентностью .

Тотипотентность (лат. totipotentia , букв. «способность ко всему [вещам]») — это способность отдельной клетки делиться и производить все дифференцированные клетки организма . Споры и зиготы являются примерами тотипотентных клеток. [3] В спектре клеточной активности тотипотентность представляет собой клетку с наибольшим потенциалом дифференцировки , способную дифференцироваться в любую эмбриональную клетку, а также в любую внеэмбриональную тканевую клетку. Напротив, плюрипотентные клетки могут дифференцироваться только в эмбриональные клетки. [4] [5]
Полностью дифференцированная клетка может вернуться в состояние тотипотентности. [6] Преобразование в тотипотентность сложное и до конца не изученное. В 2011 году исследование показало, что клетки могут дифференцироваться не в полностью тотипотентные клетки, а в «сложную клеточную вариацию» тотипотентности. [7]
Модель развития человека можно использовать для описания того, как возникают тотипотентные клетки. [8] Развитие человека начинается, когда сперматозоид оплодотворяет яйцеклетку, и в результате оплодотворенная яйцеклетка создает единственную тотипотентную клетку, зиготу . [9] В первые часы после оплодотворения эта зигота делится на идентичные тотипотентные клетки, которые в дальнейшем могут развиться в любой из трех зародышевых листков человека ( энтодерму , мезодерму или эктодерму ) или в клетки плаценты ( цитотрофобласт или синцитиотрофобласт ). Достигнув 16-клеточной стадии, тотипотентные клетки морулы дифференцируются в клетки, которые в конечном итоге становятся либо внутренней клеточной массой бластоцисты , либо внешними трофобластами . Примерно через четыре дня после оплодотворения и после нескольких циклов клеточного деления эти тотипотентные клетки начинают специализироваться. Внутренняя клеточная масса, источник эмбриональных стволовых клеток , становится плюрипотентной.
Исследования Caenorhabditis elegans показывают, что множество механизмов, включая регуляцию РНК, могут играть роль в поддержании тотипотентности на разных стадиях развития у некоторых видов. [10] Работа с рыбками данио и млекопитающими предполагает дальнейшее взаимодействие между микроРНК и РНК-связывающими белками (RBP) в определении различий в развитии. [11]
В первичных зародышевых клетках мыши полногеномное перепрограммирование , ведущее к тотипотентности, включает стирание эпигенетических отпечатков. Перепрограммированию способствует активное деметилирование ДНК с участием ферментативного пути репарации вырезания оснований ДНК . [12] Этот путь влечет за собой стирание метилирования CpG (5mC) в первичных зародышевых клетках посредством первоначального преобразования 5mC в 5-гидроксиметилцитозин (5hmC), реакции, вызываемой высокими уровнями ферментов десять-одиннадцать диоксигеназ TET-1 и TET-. 2 . [13]
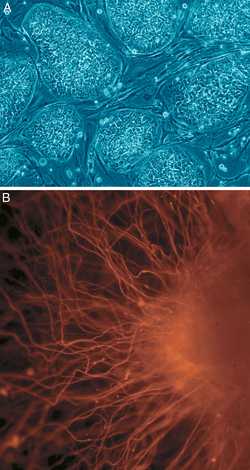
В клеточной биологии плюрипотентность (лат. pluripotentia , букв. «способность ко многим [вещам]») [14] относится к стволовой клетке, которая обладает потенциалом дифференцироваться в любой из трех зародышевых слоев : энтодерму (кишечник, легкие и печень). ), мезодерму (мышцы, скелет, кровеносные сосуды, мочеполовые органы, дерма) или эктодерму (нервная, сенсорная, эпидермис), но не во внеэмбриональные ткани, такие как плацента или желточный мешок. [15]
Индуцированные плюрипотентные стволовые клетки, обычно сокращенно называемые iPS-клетками или iPSC, представляют собой тип плюрипотентных стволовых клеток, искусственно полученных из неплюрипотентной клетки, обычно взрослой соматической клетки , путем индуцирования «принудительной» экспрессии определенных генов и факторов транскрипции . [16] Эти факторы транскрипции играют ключевую роль в определении состояния этих клеток, а также подчеркивают тот факт, что эти соматические клетки сохраняют ту же генетическую информацию, что и ранние эмбриональные клетки. [17] Способность переводить клетки в плюрипотентное состояние была впервые открыта в 2006 году с использованием мышиных фибробластов и четырех факторов транскрипции: Oct4 , Sox2 , Klf4 и c- Myc ; [18] этот метод, названный перепрограммированием , позже принес Шинья Яманаке и Джону Гердону Нобелевскую премию по физиологии и медицине. [19] Затем в 2007 году последовала успешная индукция ИПСК человека, полученных из фибробластов дермы человека, с использованием методов, аналогичных тем, которые используются для индукции клеток мыши. [20] Эти индуцированные клетки обладают свойствами, схожими с таковыми эмбриональных стволовых клеток (ЭСК), но не требуют использования эмбрионов. Некоторые сходства между ЭСК и ИПСК включают плюрипотентность, морфологию , способность к самообновлению (признак, который подразумевает, что они могут делиться и реплицироваться бесконечно), а также экспрессию генов . [21]
Считается также, что эпигенетические факторы участвуют в фактическом перепрограммировании соматических клеток с целью индукции плюрипотентности. Было высказано предположение, что определенные эпигенетические факторы могут фактически работать на очистку исходных соматических эпигенетических меток с целью приобретения новых эпигенетических меток, которые являются частью достижения плюрипотентного состояния. Хроматин также реорганизуется в ИПСК и становится таким же, как в ЭСК, поскольку он менее конденсирован и, следовательно, более доступен. Модификации эухроматина также распространены, что также согласуется с состоянием эухроматина , обнаруженного в ЭСК. [21]
Из-за их большого сходства с ЭСК ИПСК интересуют медицинское и исследовательское сообщество. ИПСК потенциально могут иметь те же терапевтические последствия и применения, что и ЭСК, но без спорного использования эмбрионов в этом процессе, что является темой больших биоэтических дебатов. Индуцированная плюрипотентность соматических клеток в недифференцированные iPS-клетки первоначально рассматривалась как конец спорного использования эмбриональных стволовых клеток . Однако было обнаружено, что ИПСК потенциально канцерогенны , и, несмотря на достижения, [16] до недавнего времени никогда не были одобрены для клинических исследований в США. В настоящее время аутологичные дофаминергические клетки-предшественники, полученные из ИПСК, используются в исследованиях по лечению болезни Паркинсона. [22] При создании ИПСК также наблюдались такие недостатки, как низкая скорость репликации и раннее старение, [23] что затрудняло их использование в качестве замены ЭСК.
Соматическая экспрессия комбинированных факторов транскрипции может напрямую индуцировать судьбу других определенных соматических клеток ( трансдифференцировка ); Исследователи определили три транскрипционных фактора, специфичных для нейронных линий, которые могут напрямую превращать мышиные фибробласты (клетки соединительной ткани) в полностью функциональные нейроны . [24] Этот результат ставит под сомнение терминальную природу клеточной дифференцировки и целостность коммитирования клонов; и подразумевает, что при наличии соответствующих инструментов все клетки тотипотентны и могут образовывать любые виды тканей.
Некоторые из возможных медицинских и терапевтических применений ИПСК, полученных от пациентов, включают их использование при трансплантации клеток и тканей без риска отторжения, который обычно встречается. ИПСК потенциально могут заменить непригодные модели на животных, а также модели in vitro, используемые для исследования заболеваний. [25]

Результаты, касающиеся эпибластов до и после имплантации, позволили классифицировать плюрипотентность на два состояния: «наивное» и «праймированное», представляющее эпибласт до и после имплантации соответственно. [26] Континуум от наивного к праймированному контролируется за счет уменьшения димеризации Sox2/Oct4 на элементах ДНК SoxOct, контролирующих наивную плюрипотентность. [27] Примированные плюрипотентные стволовые клетки разных видов можно вернуть в наивное состояние с помощью коктейля, содержащего Klf4 и Sox2 или «супер-Sox» — химерного транскрипционного фактора с повышенной способностью димеризоваться с Oct4. [27]
Исходные стволовые клетки, обычно используемые в науке и называемые эмбриональными стволовыми клетками (ЭСК), происходят из предимплантационного эпибласта; такой эпибласт способен генерировать весь плод, а одна клетка эпибласта может вносить вклад во все клеточные линии, если ее инъецировать в другую бластоцисту. С другой стороны, между эпибластами до и после имплантации можно наблюдать несколько заметных различий, таких как разница в морфологии, при которой эпибласт после имплантации меняет свою морфологию на чашеобразную форму, называемую «яйцевым цилиндром», как а также хромосомные изменения, при которых одна из Х-хромосом подвергается случайной инактивации на ранней стадии яйцевого цилиндра, известное как Х-инактивация . [28] Во время этого развития клетки эпибласта яйцевого цилиндра систематически подвергаются воздействию факторов роста фибробластов , передачи сигналов Wnt и других индуктивных факторов через окружающий желточный мешок и ткань трофобласта, [29] так, что они становятся инструктивно специфичными в соответствии с пространственным расположением клеток. организация. [30]
Еще одним важным отличием является то, что постимплантационные стволовые клетки эпибласта не способны вносить вклад в химеры бластоцисты [31] , что отличает их от других известных плюрипотентных стволовых клеток. Клеточные линии, полученные из таких постимплантационных эпибластов, называются стволовыми клетками, полученными из эпибластов , которые впервые были получены в лаборатории в 2007 году. И ESC, и EpiSCs происходят из эпибластов, но находятся на разных фазах развития. Плюрипотентность все еще сохраняется в постимплантационном эпибласте, о чем свидетельствует консервативная экспрессия Nanog , Fut4 и Oct-4 в EpiSCs, [32] до сомитогенеза и может быть обращена вспять в середине индуцированной экспрессии Oct-4 . [33]
_Ranunculus_asiaticus_-_example_of_Totipotency.jpg/440px-(MHNT)_Ranunculus_asiaticus_-_example_of_Totipotency.jpg)
Неиндуцированная плюрипотентность наблюдалась в культуре ткани корневой меристемы, особенно Каримом и др., 2015, Кимом и др., 2018 и Росспопоффом и др., 2017. Эта плюрипотентность регулируется различными регуляторами, включая PLETHORA 1 и PLETHORA 2 ; и PLETHORA 3 , PLETHORA 5 и PLETHORA 7 , экспрессия которых, как обнаружил Карим, провоцируется ауксином . (Они также известны как PLT1, PLT2, PLT3, PLT5, PLT7 и экспрессируются одноименными генами.) [обновлять]Ожидается, что с 2019 года это откроет возможности для будущих исследований плюрипотентности в тканях корня. [34]

Мультипотентность — это когда клетки-предшественники обладают потенциалом активации генов, позволяющим дифференцироваться в отдельные типы клеток. Например, гемопоэтическая стволовая клетка – и этот тип клеток может дифференцироваться в несколько типов клеток крови, таких как лимфоциты , моноциты , нейтрофилы и т. д., но до сих пор неясно, обладают ли HSC способностью дифференцироваться в клетки мозга , костные клетки или другие типы клеток, не относящиеся к крови. [ нужна цитата ]
Исследования, связанные с мультипотентными клетками, показывают, что мультипотентные клетки могут быть способны превращаться в клетки неродственных типов. В другом случае стволовые клетки пуповинной крови человека были преобразованы в человеческие нейроны. [35] Также проводятся исследования по превращению мультипотентных клеток в плюрипотентные клетки. [36]
Мультипотентные клетки обнаружены во многих, но не во всех типах клеток человека. Мультипотентные клетки были обнаружены в пуповинной крови , [37] жировой ткани, [38] сердечных клетках, [39] костном мозге и мезенхимальных стволовых клетках (МСК), которые обнаруживаются в третьих молярах . [40]
МСК могут оказаться ценным источником стволовых клеток из коренных зубов в возрасте 8–10 лет, до кальцификации зубов у взрослых. МСК могут дифференцироваться в остеобласты, хондроциты и адипоциты. [41]
В биологии олигопотентность — это способность клеток-предшественников дифференцироваться в несколько типов клеток . Это степень могущества . Примерами олигопотентных стволовых клеток являются лимфоидные или миелоидные стволовые клетки. [2] В частности, лимфоидная клетка может давать начало различным клеткам крови, таким как В- и Т-клетки, но не другому типу клеток крови, например эритроцитам. [42] Примерами клеток-предшественников являются сосудистые стволовые клетки, которые способны становиться как эндотелиальными , так и гладкомышечными клетками.
В клеточной биологии унипотентная клетка — это концепция, согласно которой одна стволовая клетка способна дифференцироваться только в один тип клеток. [43] В настоящее время неясно, существуют ли настоящие унипотентные стволовые клетки. Гепатобласты, которые дифференцируются в гепатоциты (составляющие большую часть печени ) или холангиоциты (эпителиальные клетки желчных протоков), являются бипотентными. [44] Близким синонимом унипотентной клетки является клетка-предшественник .