В клеточной биологии паракринная передача сигналов — это форма клеточной передачи сигналов , тип клеточной коммуникации , при котором клетка вырабатывает сигнал, вызывающий изменения в соседних клетках, изменяя поведение этих клеток. Сигнальные молекулы, известные как паракринные факторы , диффундируют на относительно короткое расстояние (локальное действие), в отличие от передачи сигналов клеткам эндокринными факторами , гормонами , которые перемещаются на значительно большие расстояния через систему кровообращения ; юкстакринные взаимодействия ; и аутокринная сигнализация . Клетки, продуцирующие паракринные факторы, секретируют их в непосредственную внеклеточную среду. Затем факторы перемещаются в соседние клетки, в которых градиент полученного фактора определяет результат. Однако точное расстояние, на которое могут распространяться паракринные факторы, не установлено.
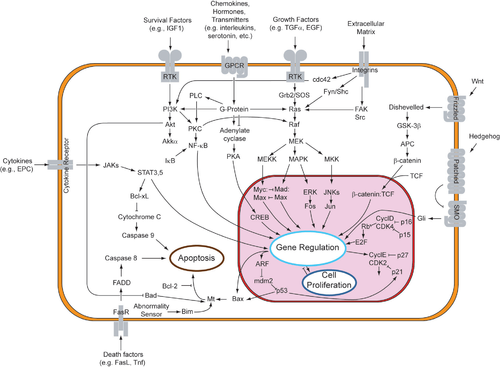
Хотя паракринная передача сигналов вызывает разнообразный набор ответов в индуцированных клетках, большинство паракринных факторов используют относительно упорядоченный набор рецепторов и путей. Фактически, известно, что разные органы тела – даже у разных видов – используют одинаковый набор паракринных факторов в дифференцированном развитии. [1] Высококонсервативные рецепторы и пути могут быть организованы в четыре основных семейства на основе схожих структур: семейство факторов роста фибробластов (FGF), семейство Hedgehog , семейство Wnt и суперсемейство TGF-β . Связывание паракринного фактора с соответствующим рецептором инициирует каскады передачи сигнала , вызывая различные ответы.
Чтобы паракринные факторы успешно вызывали ответ в принимающей клетке, эта клетка должна иметь соответствующие рецепторы, доступные на клеточной мембране для приема сигналов, также известные как компетентность . Кроме того, отвечающая клетка также должна обладать способностью механически индуцироваться.
Хотя семейство паракринных факторов FGF обладает широким спектром функций, основные результаты подтверждают идею о том, что они в первую очередь стимулируют пролиферацию и дифференцировку. [2] [3] Для выполнения множества разнообразных функций FGF можно альтернативно сплайсировать или даже иметь разные инициирующие кодоны для создания сотен различных изоформ FGF . [4]
Одна из наиболее важных функций рецепторов FGF (FGFR) связана с развитием конечностей. В этой передаче сигналов участвуют девять различных альтернативно сплайсированных изоформ рецептора. [5] Fgf 8 и Fgf 10 — два важнейших игрока в развитии конечностей. При зарождении передних конечностей и росте конечностей у мышей аксиальные (продольные) сигналы от промежуточной мезодермы производят Tbx 5, который впоследствии передает той же мезодерме сигнал о выработке Fgf 10. Fgf 10 затем сигнализирует эктодерме о начале производства Fgf 8, который также стимулирует выработку Fgf 10. Удаление Fgf 10 приводит к появлению мышей без конечностей. [6]
Кроме того, паракринная передача сигналов Fgf важна для развивающихся глаз цыплят. МРНК fgf8 локализуется в нейральной сетчатке глазного бокала . Эти клетки контактируют с клетками внешней эктодермы, которые в конечном итоге станут хрусталиком. [4]
Фенотип и выживаемость мышей после нокаута некоторых генов FGFR: [5]
Паракринная передача сигналов через факторы роста фибробластов и соответствующие рецепторы использует рецепторный тирозиновый путь. Этот сигнальный путь был тщательно изучен с использованием глаз дрозофилы и рака человека. [7]
Связывание FGF с FGFR фосфорилирует холостую киназу и активирует путь RTK. Этот путь начинается на поверхности клеточной мембраны, где лиганд связывается со своим специфическим рецептором. Лиганды, которые связываются с RTK, включают факторы роста фибробластов , эпидермальные факторы роста, тромбоцитарные факторы роста и фактор стволовых клеток . [7] Это димеризует трансмембранный рецептор в другой RTK-рецептор, что вызывает аутофосфорилирование и последующее конформационное изменение гомодимеризованного рецептора. Это конформационное изменение активирует спящую киназу каждой RTK на остатке тирозина. В связи с тем, что рецептор проходит через мембрану из внеклеточной среды, через липидный бислой и в цитоплазму , связывание рецептора с лигандом также вызывает трансфосфорилирование цитоплазматического домена рецептора. [8]
Адаптерный белок (такой как SOS) распознает фосфорилированный тирозин на рецепторе. Этот белок действует как мост, соединяющий RTK с промежуточным белком (таким как GNRP), запуская внутриклеточный сигнальный каскад. В свою очередь, промежуточный белок стимулирует GDP-связанный Ras к активированному GTP-связанному Ras. GAP в конечном итоге возвращает Ras в неактивное состояние. Активация Ras может инициировать три сигнальных пути ниже Ras: путь киназы Ras → Raf → MAP, путь киназы PI3 и путь Ral. Каждый путь приводит к активации факторов транскрипции, которые проникают в ядро и изменяют экспрессию генов. [9]

Было показано, что паракринная передача сигналов факторов роста между соседними клетками усугубляет канцерогенез . Фактически, мутантные формы одной RTK могут играть причинную роль в самых разных типах рака. Протоонкоген Kit кодирует рецептор тирозинкиназы, лигандом которого является паракринный белок, называемый фактором стволовых клеток (SCF), который важен для кроветворения (образования клеток в крови). [10] Рецептор Kit и связанные с ним тирозинкиназные рецепторы на самом деле являются ингибирующими и эффективно подавляют активацию рецептора. Мутантные формы рецептора Kit, которые активируются конститутивно, независимо от лигандов, обнаруживаются при различных раковых новообразованиях. [11]
Исследования рака щитовидной железы пролили свет на теорию о том, что паракринная передача сигналов может способствовать созданию микроокружения опухоли. Транскрипция хемокинов усиливается, когда Ras находится в состоянии, связанном с GTP. Затем хемокины высвобождаются из клетки и могут свободно связываться с другой близлежащей клеткой. Паракринная передача сигналов между соседними клетками создает эту петлю положительной обратной связи. Таким образом, конститутивная транскрипция активированных белков создает идеальную среду для возникновения опухолей. [12] Фактически, множественные связывания лигандов с рецепторами RTK чрезмерно стимулируют путь Ras-Raf-MAPK, который сверхэкспрессирует митогенную и инвазивную способность клеток. [13]
В дополнение к пути RTK факторы роста фибробластов также могут активировать сигнальный путь JAK-STAT . Вместо того, чтобы нести ковалентно связанные тирозинкиназные домены, рецепторы Jak-STAT образуют нековалентные комплексы с тирозинкиназами класса Jak ( Janus kinase ). Эти рецепторы связываются с эритропоэтином (важным для эритропоэза ), тромбопоэтином (важным для образования тромбоцитов ) и интерфероном (важным для обеспечения функции иммунных клеток). [14]
После димеризации рецепторов цитокинов после связывания лиганда JAK трансфосфорилируют друг друга. Образующиеся фосфотирозины привлекают белки STAT. Белки STAT димеризуются и проникают в ядро, действуя в качестве факторов транскрипции и изменяя экспрессию генов. [14] В частности, STAT транскрибируют гены, которые способствуют пролиферации и выживанию клеток, такие как myc. [15]
Фенотип и выживаемость мышей после нокаута некоторых генов JAK или STAT: [16]
Сигнальный путь JAK-STAT играет важную роль в развитии конечностей, в частности, в его способности регулировать рост костей посредством паракринной передачи сигналов цитокинов. Однако мутации в этом пути связаны с тяжелыми формами карликовости: танатофорной дисплазией (летальной) и ахондроплазионной карликовостью (жизнеспособной). [17] Это связано с мутацией гена Fgf , вызывающей преждевременную и конститутивную активацию транскрипционного фактора Stat1 . Деление хондроцитов преждевременно прекращается, что приводит к летальной карликовости. Клетки пластинок роста костей ребер и конечностей не транскрибируются. Таким образом, неспособность грудной клетки расширяться препятствует дыханию новорожденного. [18]
Исследование паракринной передачи сигналов через путь JAK-STAT выявило его потенциал в активации инвазивного поведения эпителиальных клеток яичников . Этот эпителиально- мезенхимальный переход очень очевиден при метастазах . [19] Паракринная передача сигналов через путь JAK-STAT необходима при переходе от стационарных эпителиальных клеток к мобильным мезенхимальным клеткам, которые способны вторгаться в окружающие ткани. Было обнаружено, что только путь JAK-STAT индуцирует миграцию клеток. [20]
Семейство белков Hedgehog участвует в индукции типов клеток, создании границ тканей и формировании паттерна и обнаружено во всех двусторонних организмах. Белки ежей были впервые обнаружены и изучены у дрозофилы . Белки Hedgehog производят ключевые сигналы для установления строения конечностей и тела плодовых мух, а также гомеостаза взрослых тканей, участвующих в позднем эмбриогенезе и метаморфозе . У позвоночных были обнаружены по крайней мере три гомолога ежа «Drosophila»: звуковой еж, пустынный еж и индийский еж. Sonic hedgehog ( SHH ) играет различные роли в развитии позвонков, опосредуя передачу сигналов и регулируя организацию центральной нервной системы, полярности конечностей и сомитов . Пустынный еж ( DHH ) экспрессируется в клетках Сертоли, участвующих в сперматогенезе . Индийский еж ( IHH ) экспрессируется в кишечнике и хрящах, что играет важную роль в постнатальном росте костей. [21] [22] [23]


Члены семейства белков Hedgehog действуют путем связывания с трансмембранным « патченным » рецептором, который связан с « сглаживанным » белком, с помощью которого может передаваться сигнал Hedgehog . В отсутствие Hedgehog рецептор Patched ингибирует действие Smoothened. Ингибирование Smoothened приводит к тому, что белковый комплекс Cubitus Interruptus (Ci), Fused и Cos, прикрепленный к микротрубочкам, остается интактным. В этой конформации белок Ci расщепляется, так что часть белка может проникнуть в ядро и действовать как репрессор транскрипции . В присутствии Ежа Patched больше не подавляет Smoothened. Тогда активный белок Smoothened способен ингибировать PKA и Slimb, так что белок Ci не расщепляется. Этот интактный белок Ci может проникать в ядро, связываться с белком CPB и действовать как активатор транскрипции , индуцируя экспрессию генов ответа Hedgehog. [23] [24] [25]
Сигнальный путь Hedgehog имеет решающее значение для правильного формирования и ориентации тканей во время нормального развития большинства животных. Белки Hedgehog индуцируют пролиферацию клеток в одних клетках и дифференцировку в других. Аберрантная активация пути Hedgehog связана с несколькими типами рака , в частности с базальноклеточной карциномой . Эта неконтролируемая активация белков Hedgehog может быть вызвана мутациями сигнального пути, которые будут независимыми от лигандов , или мутацией, вызывающей сверхэкспрессию белка Hedgehog, которая будет зависеть от лигандов. Кроме того, было показано, что индуцированная терапией активация пути Hedgehog необходима для прогрессирования опухолей простаты после андрогенной депривационной терапии . [26] Эта связь между сигнальным путем Hedgehog и раком человека может обеспечить возможность терапевтического вмешательства в качестве лечения таких видов рака. Сигнальный путь Hedgehog также участвует в нормальной регуляции популяций стволовых клеток и необходим для нормального роста и регенерации поврежденных органов. Это может обеспечить еще один возможный путь онкогенеза через путь Hedgehog. [27] [28] [29]

Семейство белков Wnt включает большое количество богатых цистеином гликопротеинов . Белки Wnt активируют каскады сигнальной трансдукции посредством трех различных путей: канонического пути Wnt , неканонического пути планарной клеточной полярности (PCP) и неканонического пути Wnt/Ca 2+ . Белки Wnt, по-видимому, контролируют широкий спектр процессов развития и считаются необходимыми для контроля ориентации веретена , полярности клеток, кадгерин-опосредованной адгезии и раннего развития эмбрионов у многих различных организмов. Текущие исследования показали, что дерегуляция передачи сигналов Wnt играет роль в формировании опухоли, поскольку на клеточном уровне белки Wnt часто регулируют пролиферацию клеток , морфологию клеток, подвижность клеток и судьбу клеток. [30]

В каноническом пути белки Wnt связываются со своим трансмембранным рецептором семейства белков Frizzled . Связывание Wnt с белком Frizzled активирует белок Disheveled . В активном состоянии белок Disheveled ингибирует активность фермента киназы гликогенсинтазы 3 ( GSK3 ). Обычно активный GSK3 предотвращает диссоциацию β-катенина с белком APC , что приводит к деградации β-катенина . Таким образом, ингибирование GSK3 позволяет β-катенину диссоциировать от APC, накапливаться и перемещаться в ядро. В ядре β-катенин связывается с транскрипционным фактором Lef/Tcf , который уже действует на ДНК как репрессор, ингибируя транскрипцию генов, с которыми он связывается. Связывание β-катенина с Lef/Tcf действует как активатор транскрипции, активируя транскрипцию Wnt-зависимых генов. [31] [32] [33]
Неканонические пути Wnt обеспечивают путь передачи сигнала для Wnt, который не включает β-катенин . В неканонических путях Wnt влияет на актин и микротрубочковый цитоскелет , а также на транскрипцию генов .

Неканонический путь PCP регулирует морфологию , деление и движение клеток . Белки Wnt снова связываются с Frizzled и активируют его, так что Frizzled активирует белок Disheveled, который привязан к плазматической мембране через белок Prickle и трансмембранный белок Stbm. Активный Disheveled активирует RhoA GTPase через связанный с Disheveled активатор морфогенеза 1 (Daam1) и белок Rac . Активный RhoA способен вызывать изменения цитоскелета путем активации Roh-ассоциированной киназы (ROCK) и напрямую влиять на транскрипцию генов. Active Rac может напрямую вызывать изменения цитоскелета и влиять на транскрипцию генов посредством активации JNK. [31] [32] [33]

Неканонический путь Wnt/Ca 2+ регулирует внутриклеточные уровни кальция . Wnt снова привязывается и активируется к Frizzled. Однако в этом случае активированный Frizzled заставляет связанный G-белок активировать фосфолипазу ( PLC), которая взаимодействует с PIP 2 и расщепляет его на DAG и IP 3 . Затем IP 3 может связываться с рецептором эндоплазматической сети , высвобождая внутриклеточные запасы кальция и индуцируя кальций-зависимую экспрессию генов. [31] [32] [33]
Сигнальные пути Wnt имеют решающее значение для передачи сигналов между клетками во время нормального развития и эмбриогенеза и необходимы для поддержания взрослой ткани, поэтому нетрудно понять, почему нарушение сигнальных путей Wnt может способствовать дегенеративным заболеваниям и раку человека .
Сигнальные пути Wnt сложны, включают множество различных элементов и, следовательно, имеют множество мишеней для неправильной регуляции. Мутации, которые вызывают конститутивную активацию сигнального пути Wnt, приводят к образованию опухолей и раку. Аберрантная активация пути Wnt может привести к усилению пролиферации клеток. Текущие исследования сосредоточены на действии сигнального пути Wnt, регулирующем выбор стволовых клеток для пролиферации и самообновления. Такое действие передачи сигналов Wnt в возможном контроле и поддержании стволовых клеток может обеспечить возможное лечение рака, демонстрирующего аберрантную передачу сигналов Wnt. [34] [35] [36]
« TGF » (трансформирующий фактор роста) представляет собой семейство белков, включающее 33 члена, которые кодируют димерные секретируемые полипептиды, регулирующие развитие. [37] Многие процессы развития находятся под его контролем, включая гаструляцию, осевую симметрию тела, морфогенез органов и гомеостаз тканей у взрослых. [38] Все лиганды TGF-β связываются с рецепторами типа I или типа II, образуя гетеротетрамические комплексы. [39]
Путь TGF-β регулирует многие клеточные процессы в развивающихся эмбрионах и взрослых организмах, включая рост клеток , дифференцировку , апоптоз и гомеостаз . У человека и других млекопитающих существует пять типов рецепторов типа II и семь типов рецепторов типа I. Эти рецепторы известны как «киназы двойной специфичности», поскольку их цитоплазматический киназный домен обладает слабой тирозинкиназной активностью, но сильной серин / треониновой киназной активностью. [40] Когда лиганд суперсемейства TGF-β связывается с рецептором типа II, он рекрутирует рецептор типа I и активирует его путем фосфорилирования остатков серина или треонина его «GS»-бокса. [41] При этом образуется активационный комплекс, который затем может фосфорилировать белки SMAD.

Существует три класса SMAD:
Примеры SMAD в каждом классе: [42] [43] [44]
Суперсемейство TGF-β активирует членов семейства SMAD , которые действуют как факторы транскрипции. В частности, рецептор типа I, активируемый рецептором типа II, фосфорилирует R-SMAD , которые затем связываются с ко-SMAD, SMAD4 . R-SMAD/Co-SMAD образует комплекс с импортином и поступает в ядро, где они действуют как факторы транскрипции и либо повышают, либо подавляют экспрессию целевого гена.
Специфические лиганды TGF-β приводят к активации SMAD2/3 или SMAD1/5 R-SMAD . Например, когда активин , Nodal или лиганд TGF-β связываются с рецепторами, фосфорилированный рецепторный комплекс может активировать SMAD2 и SMAD3 посредством фосфорилирования. Однако когда лиганд BMP связывается с рецепторами, фосфорилированный рецепторный комплекс активирует SMAD1 и SMAD5 . Затем комплексы Smad2/3 или Smad1/5 образуют димерный комплекс с SMAD4 и становятся факторами транскрипции . Хотя в этом пути участвует множество R-SMAD , есть только один ко-SMAD, SMAD4 . [45]
Сигнальные белки, не относящиеся к Smad, способствуют ответам пути TGF-β тремя способами. Во-первых, сигнальные пути, отличные от Smad, фосфорилируют Smad. Во-вторых, Smads напрямую передают сигналы другим путям, напрямую связываясь с другими сигнальными белками, такими как киназы. Наконец, рецепторы TGF-β напрямую фосфорилируют белки, не относящиеся к Smad. [46]
В это семейство входят TGF-β1 , TGF-β2 , TGF-β3 и TGF-β5. Они участвуют в положительной и отрицательной регуляции деления клеток , формировании внеклеточного матрикса между клетками, апоптозе и эмбриогенезе . Они связываются с рецептором TGF-β типа II (TGFBRII).
TGF-β1 стимулирует синтез коллагена и фибронектина и ингибирует деградацию внеклеточного матрикса . В конечном итоге он увеличивает выработку внеклеточного матрикса эпителиальными клетками . [39] Белки TGF-β регулируют эпителий, контролируя, где и когда они разветвляются, образуя протоки почек, легких и слюнных желез. [39]
Первоначально было обнаружено, что члены семейства BMP индуцируют костеобразование , как следует из их названия. Однако BMP очень многофункциональны и могут также регулировать апоптоз , миграцию клеток , деление и дифференцировку клеток . Они также определяют переднюю/заднюю ось, вызывают рост и регулируют гомеостаз . [37]
BMP связываются с рецептором костного морфогенетического белка типа II (BMPR2). Некоторыми белками семейства BMP являются BMP4 и BMP7 . BMP4 способствует образованию костей, вызывает гибель клеток или сигнализирует о формировании эпидермиса , в зависимости от ткани, на которую он действует. BMP7 имеет решающее значение для развития почек, синтеза сперматозоидов и поляризации нервной трубки. И BMP4 , и BMP7 регулируют стабильность и процессинг зрелых лигандов, включая деградацию лигандов в лизосомах. [37] BMP действуют путем диффузии из клеток, которые их создают. [47]
Фактор роста и факторы свертывания крови являются паракринными сигнальными агентами. Местное действие передачи сигналов факторов роста играет особенно важную роль в развитии тканей. Кроме того, ретиноевая кислота , активная форма витамина А , функционирует паракринным образом, регулируя экспрессию генов во время эмбрионального развития у высших животных. [49] У насекомых аллатостатин контролирует рост посредством паракринного действия на аллата. [ нужна цитата ]
У зрелых организмов паракринная передача сигналов участвует в реакциях на аллергены , восстановлении тканей, образовании рубцовой ткани и свертывании крови . [ нужна цитация ] Гистамин — это паракринный препарат, который выделяется иммунными клетками бронхиального дерева. Гистамин вызывает сокращение гладкомышечных клеток бронхов, сужая дыхательные пути. [50]