Биосенсор — это аналитическое устройство, используемое для обнаружения химического вещества, которое сочетает в себе биологический компонент с физико -химическим детектором. [1] [2] [3] [4] Чувствительный биологический элемент , например ткань, микроорганизмы, органеллы , клеточные рецепторы , ферменты , антитела , нуклеиновые кислоты и т. д., представляет собой биологически полученный материал или биомиметический компонент, который взаимодействует, связывает с исследуемым аналитом или распознает его. Биологически чувствительные элементы также могут быть созданы методами биологической инженерии . Преобразователь или детекторный элемент , который преобразует один сигнал в другой, работает физико-химическим способом: оптическим, пьезоэлектрическим , электрохимическим, электрохемилюминесцентным и т. д. в результате взаимодействия аналита с биологическим элементом, что позволяет легко измерить и количественно определить. Устройство считывания биосенсоров соединяется с соответствующей электроникой или сигнальными процессорами, которые в первую очередь отвечают за отображение результатов в удобной для пользователя форме. [5] Иногда это самая дорогая часть сенсорного устройства, однако можно создать удобный для пользователя дисплей, включающий преобразователь и чувствительный элемент ( голографический датчик ). Считыватели обычно разрабатываются и изготавливаются по индивидуальному заказу с учетом различных принципов работы биосенсоров.
Биосенсор обычно состоит из биорецептора (фермент/антитело/клетка/нуклеиновая кислота/аптамер), компонента преобразователя (полупроводниковый материал/наноматериал) и электронной системы , которая включает в себя усилитель сигнала , процессор и дисплей. [6] Преобразователи и электроника могут быть объединены, например, в микросенсорные системы на базе КМОП . [7] [8] Компонент распознавания, часто называемый биорецептором, использует биомолекулы организмов или рецепторы, смоделированные по образцу биологических систем, для взаимодействия с интересующим аналитом. Это взаимодействие измеряется биопреобразователем, который выдает измеримый сигнал, пропорциональный присутствию целевого аналита в образце. Основная цель конструкции биосенсора — обеспечить быстрое и удобное тестирование в месте, вызывающем беспокойство или уход, где был взят образец. [1] [9] [10]
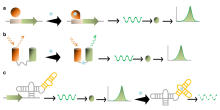
В биосенсоре биорецептор предназначен для взаимодействия с конкретным интересующим аналитом для получения эффекта, измеряемого датчиком. Высокая селективность аналита среди матрицы других химических или биологических компонентов является ключевым требованием биорецептора. Хотя тип используемых биомолекул может широко варьироваться, биосенсоры можно классифицировать в соответствии с общими типами взаимодействий биорецепторов, включающими: антитело/антиген, [11] ферменты/лиганды, нуклеиновые кислоты/ДНК, клеточные структуры/клетки или биомиметические материалы. [12] [13]
Иммуносенсор использует очень специфическую аффинность связывания антител с определенным соединением или антигеном . Специфическая природа взаимодействия антитело-антиген аналогична подгонке замка и ключа: антиген связывается с антителом только в том случае, если он имеет правильную конформацию. События связывания приводят к физико-химическим изменениям, которые в сочетании с индикатором, таким как флуоресцентные молекулы, ферменты или радиоизотопы, могут генерировать сигнал. Существуют ограничения при использовании антител в сенсорах: 1. Связывающая способность антител сильно зависит от условий анализа (например, pH и температуры) и 2. Взаимодействие антитело-антиген обычно устойчиво, однако связывание может быть нарушено хаотропными реагентами . органические растворители или даже ультразвуковое излучение. [14] [15]
Взаимодействие антитело-антиген также можно использовать для серологического тестирования или обнаружения циркулирующих антител в ответ на определенное заболевание. Важно отметить, что серологические тесты стали важной частью глобального ответа на пандемию COVID-19 . [16]
Использование антител в качестве компонента биораспознавания биосенсоров имеет ряд недостатков. Они имеют высокую молекулярную массу и ограниченную стабильность, содержат существенные дисульфидные связи и дороги в производстве. В одном из подходов к преодолению этих ограничений были созданы рекомбинантные связывающиеся фрагменты ( Fab , Fv или scFv ) или домены (VH, VHH ) антител. [17] В другом подходе были созданы небольшие белковые каркасы с благоприятными биофизическими свойствами для создания искусственных семейств антигенсвязывающих белков (AgBP), способных специфично связываться с различными целевыми белками, сохраняя при этом благоприятные свойства родительской молекулы. Элементы семейства, которые специфически связываются с данным целевым антигеном, часто отбираются in vitro с помощью методов дисплея: фагового дисплея , рибосомного дисплея , дрожжевого дисплея или дисплея мРНК . Искусственные связывающие белки намного меньше антител (обычно менее 100 аминокислотных остатков), обладают высокой стабильностью, лишены дисульфидных связей и могут экспрессироваться с высоким выходом при восстановлении клеточной среды, такой как бактериальная цитоплазма, в отличие от антител и их производных. . [18] [19] Таким образом, они особенно подходят для создания биосенсоров. [20] [21]
Специфические связывающие способности и каталитическая активность ферментов делают их популярными биорецепторами. Распознавание аналита осуществляется с помощью нескольких возможных механизмов: 1) фермент, превращающий аналит в продукт, который можно обнаружить сенсором, 2) обнаружение ингибирования или активации фермента аналитом или 3) мониторинг изменения свойств фермента в результате взаимодействия с аналитом. . [15] Основными причинами широкого использования ферментов в биосенсорах являются: 1) способность катализировать большое количество реакций; 2) возможность обнаружения группы аналитов (субстратов, продуктов, ингибиторов и модуляторов каталитической активности); и 3) совместимость с несколькими различными методами трансдукции для обнаружения аналита. Примечательно, что, поскольку ферменты не расходуются в реакциях, биосенсор можно легко использовать непрерывно. Каталитическая активность ферментов также позволяет снизить пределы обнаружения по сравнению с обычными методами связывания. Однако срок службы датчика ограничен стабильностью фермента.
Антитела имеют высокую константу связывания , превышающую 10^8 л/моль, что означает практически необратимую ассоциацию после образования пары антиген-антитело. Для некоторых аналитических молекул, таких как аффинно-связывающие белки с глюкозой , существуют белки, которые связывают свой лиганд с высокой специфичностью, как антитела, но с гораздо меньшей константой связывания, порядка от 10^2 до 10^4 л/моль. В этом случае ассоциация между аналитом и рецептором носит обратимый характер, и рядом с парой между ними также встречаются их свободные молекулы в измеримой концентрации. Например, в случае глюкозы конканавалин А может действовать как аффинный рецептор, демонстрируя константу связывания 4x10^2 л/моль. [22] Использование аффинно-связывающих рецепторов для целей биосенсорства было предложено Шульцем и Симсом в 1979 году [23] и впоследствии было использовано в флуоресцентном анализе для измерения глюкозы в соответствующем физиологическом диапазоне от 4,4 до 6,1 ммоль/л. [24] Преимущество сенсорного принципа состоит в том, что аналит не расходуется в химической реакции, как это происходит при ферментативных анализах.
Биосенсоры, использующие рецепторы на основе нуклеиновых кислот, могут быть основаны либо на взаимодействиях комплементарных пар оснований, называемых геносенсорами, либо на специфических имитаторах антител на основе нуклеиновых кислот (аптамерах) в качестве аптасенсоров. [25] В первом случае процесс распознавания основан на принципе комплементарного спаривания оснований аденин:тимин и цитозин:гуанин в ДНК . Если целевая последовательность нуклеиновой кислоты известна, комплементарные последовательности могут быть синтезированы, помечены и затем иммобилизованы на сенсоре. Событие гибридизации можно обнаружить оптически и установить наличие целевой ДНК/РНК. В последнем случае аптамеры, созданные против мишени, распознают ее посредством взаимодействия специфических нековалентных взаимодействий и индуцированной подгонки. Эти аптамеры можно легко пометить флуорофором/наночастицами металла для оптического обнаружения или можно использовать для безметочных электрохимических или кантилеверных платформ обнаружения для широкого спектра целевых молекул или сложных мишеней, таких как клетки и вирусы. [26] [27] Кроме того, аптамеры можно комбинировать с ферментами нуклеиновых кислот, такими как расщепляющие РНК ДНКзимы, обеспечивая как распознавание мишени, так и генерацию сигналов в одной молекуле, что показывает потенциальное применение при разработке множественных биосенсоров. [28]
Было предложено использовать должным образом оптимизированные интегрированные оптические резонаторы для обнаружения эпигенетических модификаций (например, метилирования ДНК, посттрансляционных модификаций гистонов) в жидкостях организма пациентов, страдающих раком или другими заболеваниями. [29] В настоящее время на исследовательском уровне разрабатываются сверхчувствительные фотонные биосенсоры, позволяющие легко обнаруживать раковые клетки в моче пациента. [30] Различные исследовательские проекты направлены на разработку новых портативных устройств, в которых используются дешевые, экологически чистые одноразовые картриджи, требующие лишь простого обращения без необходимости дальнейшей обработки, мытья или манипуляций со стороны опытных технических специалистов. [31]
Органеллы образуют отдельные отсеки внутри клеток и обычно выполняют функции самостоятельно. Различные виды органелл имеют разные метаболические пути и содержат ферменты, выполняющие свою функцию. Обычно используемые органеллы включают лизосомы, хлоропласты и митохондрии. Пространственно-временное распределение кальция тесно связано с повсеместным сигнальным путем. Митохондрии активно участвуют в метаболизме ионов кальция, контролируя эту функцию, а также модулируя сигнальные пути, связанные с кальцием. Эксперименты доказали, что митохондрии обладают способностью реагировать на высокие концентрации кальция, образующиеся вблизи них, открывая кальциевые каналы. [32] Таким образом, митохондрии можно использовать для определения концентрации кальция в среде, и обнаружение будет очень чувствительным из-за высокого пространственного разрешения. Другое применение митохондрий — обнаружение загрязнения воды. Токсичность моющих средств повреждает клетки и субклеточные структуры, включая митохондрии. Моющие средства вызывают эффект набухания, который можно измерить по изменению поглощения. Экспериментальные данные показывают, что скорость изменения пропорциональна концентрации моющего средства, что обеспечивает высокий стандарт точности обнаружения. [33]
Клетки часто используются в качестве биорецепторов, поскольку они чувствительны к окружающей среде и могут реагировать на все виды стимуляторов. Клетки имеют тенденцию прикрепляться к поверхности, поэтому их можно легко иммобилизовать. По сравнению с органеллами они остаются активными в течение более длительного периода, а воспроизводимость делает их пригодными для повторного использования. Они обычно используются для обнаружения глобальных параметров, таких как стрессовое состояние, токсичность и органические производные. Их также можно использовать для мониторинга лечебного эффекта лекарств. Одним из применений является использование клеток для определения гербицидов, которые являются основными загрязнителями воды. [34] Микроводоросли улавливаются кварцевым микроволокном , а флуоресценция хлорофилла, модифицированная гербицидами, собирается на кончике пучка оптических волокон и передается на флуориметр. Водоросли постоянно культивируются для оптимизации измерений. Результаты показывают, что предел обнаружения некоторых гербицидов может достигать уровня концентрации ниже миллиарда. Некоторые клетки также можно использовать для мониторинга микробной коррозии. [35] Pseudomonas sp. выделяют с поверхности корродированного материала и иммобилизуют на ацетилцеллюлозной мембране. Активность дыхания определяют путем измерения потребления кислорода. Существует линейная зависимость между создаваемым током и концентрацией серной кислоты . Время отклика связано с загрузкой клеток и окружающей среды и может регулироваться не более чем на 5 минут.
Ткани используются в качестве биосенсора обилия существующих ферментов. К преимуществам тканей как биосенсоров можно отнести следующее: [36]
Существуют также некоторые недостатки тканей, такие как отсутствие специфичности из-за вмешательства других ферментов и более длительное время ответа из-за транспортного барьера.
Микробные биосенсоры используют реакцию бактерий на определенное вещество. Например, мышьяк можно обнаружить с помощью оперона ars , обнаруженного в нескольких таксонах бактерий. [37]

Важной частью биосенсора является прикрепление биологических элементов (маленьких молекул/белков/клеток) к поверхности сенсора (будь то металл, полимер или стекло). Самый простой способ — функционализировать поверхность, чтобы покрыть ее биологическими элементами. Это можно сделать с помощью полилизина, аминосилана, эпоксисилана или нитроцеллюлозы в случае кремниевой крошки/силикатного стекла. В дальнейшем связанный биологический агент также можно зафиксировать, например, путем послойного нанесения альтернативно заряженных полимерных покрытий. [38]
Альтернативно, для их химического или физического захвата можно использовать трехмерные решетки ( гидрогель / ксерогель ) (при этом химический захват означает, что биологический элемент удерживается на месте благодаря прочной связи, в то время как физически они удерживаются на месте, будучи неспособными проходить через поры гелевой матрицы). Наиболее часто используемый гидрогель — это золь-гель , стеклообразный диоксид кремния, полученный путем полимеризации силикатных мономеров (добавленных в виде тетраалкилортосиликатов, таких как ТМОС или ТЭОС ) в присутствии биологических элементов (наряду с другими стабилизирующими полимерами, такими как ПЭГ ) в дело о физическом поимке. [39]
Другой группой гидрогелей, которые застывают в условиях, подходящих для клеток или белков, являются акрилатные гидрогели, полимеризующиеся при радикальном инициировании . Одним из типов радикального инициатора является пероксидный радикал, обычно образующийся путем объединения персульфата с TEMED ( полиакриламидный гель также широко используется для электрофореза белков ), [40] альтернативно можно использовать свет в сочетании с фотоинициатором, таким как DMPA ( 2, 2-диметокси-2-фенилацетофенон ). [41] Умные материалы, имитирующие биологические компоненты сенсора, также можно классифицировать как биосенсоры, используя только активный или каталитический сайт или аналогичные конфигурации биомолекулы. [42]

Биосенсоры можно классифицировать по типу биопреобразователя . Наиболее распространенными типами биопреобразователей, используемых в биосенсорах, являются:
Электрохимические биосенсоры обычно основаны на ферментативном катализе реакции образования или потребления электронов (такие ферменты справедливо называют окислительно-восстановительными ферментами). Подложка датчика обычно содержит три электрода ; электрод сравнения , рабочий электрод и противоэлектрод. Целевой аналит участвует в реакции, которая происходит на активной поверхности электрода, и реакция может вызывать либо перенос электронов через двойной слой (создавая ток), либо вносить вклад в потенциал двойного слоя (создавая напряжение). Мы можем либо измерить ток (скорость потока электронов теперь пропорциональна концентрации аналита) при фиксированном потенциале, либо потенциал можно измерить при нулевом токе (это дает логарифмический отклик). Обратите внимание, что потенциал рабочего или активного электрода чувствителен к объемному заряду, и это часто используется. Кроме того, прямое электрическое обнаружение небольших пептидов и белков без меток возможно по их собственным зарядам с использованием биофункционализированных ионно-чувствительных полевых транзисторов . [43]
Другой пример, потенциометрический биосенсор (потенциал, создаваемый при нулевом токе), дает логарифмический отклик с высоким динамическим диапазоном. Такие биосенсоры часто изготавливаются путем трафаретной печати рисунков электродов на пластиковой подложке, покрытой проводящим полимером, а затем прикрепляется некоторый белок (фермент или антитело). Они имеют всего два электрода, чрезвычайно чувствительны и надежны. Они позволяют обнаруживать аналиты на уровнях, которые ранее были достижимы только с помощью ВЭЖХ и ЖХ/МС, без тщательной подготовки проб. Все биосенсоры обычно требуют минимальной подготовки проб, поскольку биологический сенсорный компонент обладает высокой селективностью в отношении соответствующего аналита. Сигнал создается электрохимическими и физическими изменениями в проводящем полимерном слое вследствие изменений, происходящих на поверхности датчика. Такие изменения можно объяснить ионной силой, pH, гидратацией и окислительно-восстановительными реакциями, причем последние происходят из-за того, что метка фермента переворачивает субстрат. [44] Полевые транзисторы, в которых область затвора модифицирована ферментом или антителом, также могут обнаруживать очень низкие концентрации различных аналитов, поскольку связывание аналита с областью затвора полевого транзистора вызывает изменение стока- исходный ток.
В настоящее время разработка биосенсоров на основе импедансной спектроскопии набирает обороты, и многие такие устройства/разработки встречаются в научных кругах и промышленности. Было показано, что одно такое устройство, основанное на 4-электродной электрохимической ячейке и использующей нанопористую мембрану из оксида алюминия, обнаруживает низкие концентрации человеческого альфа-тромбина в присутствии высокого фона сывороточного альбумина. [45] Также встречно-штыревые электроды использовались для импедансных биосенсоров. [46]


Было показано, что использование ионных каналов обеспечивает высокочувствительное обнаружение целевых биологических молекул. [47] Путем внедрения ионных каналов в поддерживаемые или привязанные двухслойные мембраны (t-BLM), прикрепленные к золотому электроду, создается электрическая цепь. Молекулы-захватчики, такие как антитела, могут быть связаны с ионным каналом, так что связывание молекулы-мишени контролирует поток ионов через канал. Это приводит к измеримому изменению электропроводности, пропорциональному концентрации мишени.
Биосенсор переключения ионных каналов (ICS) может быть создан с использованием грамицидина, димерного пептидного канала, в привязанной двухслойной мембране. [48] Один пептид грамицидина с прикрепленным антителом подвижен, а другой фиксирован. Разрыв димера останавливает ионный ток через мембрану. Величина изменения электрического сигнала значительно увеличивается за счет отделения мембраны от металлической поверхности с помощью гидрофильной прокладки.
Количественное обнаружение обширного класса целевых видов, включая белки, бактерии, лекарства и токсины, было продемонстрировано с использованием различных конфигураций мембран и захвата. [49] [50] Европейский исследовательский проект Greensense разрабатывает биосенсор для проведения количественного скрининга наркотических веществ, таких как ТГК, морфин и кокаин [51] в слюне и моче.
Безреагентный биосенсор позволяет контролировать целевой аналит в сложной биологической смеси без дополнительного реагента. Поэтому он может функционировать непрерывно, если иммобилизован на твердой опоре. Флуоресцентный биосенсор реагирует на взаимодействие с целевым аналитом изменением своих флуоресцентных свойств. Безреагентный флуоресцентный биосенсор (РЧ-биосенсор) можно получить путем интеграции биологического рецептора, направленного против целевого аналита, и сольватохромного флуорофора, эмиссионные свойства которого чувствительны к природе его локального окружения, в одной макромолекуле. Флуорофор преобразует событие распознавания в измеримый оптический сигнал. Использование примесных флуорофоров, эмиссионные свойства которых сильно отличаются от свойств собственных флуорофоров белков триптофана и тирозина, позволяет немедленно обнаруживать и количественно определять аналит в сложных биологических смесях. Интеграция флуорофора должна осуществляться в месте, где он чувствителен к связыванию аналита, без нарушения сродства рецептора.
Антитела и искусственные семейства антигенсвязывающих белков (AgBP) хорошо подходят для обеспечения модуля распознавания радиочастотных биосенсоров, поскольку они могут быть направлены против любого антигена (см. раздел о биорецепторах). Описан общий подход к интеграции сольватохромного флуорофора в AgBP, когда известна атомная структура комплекса с его антигеном, и, таким образом, превращению его в радиочастотный биосенсор. [20] Остаток AgBP идентифицирован вблизи антигена в их комплексе. Этот остаток превращается в цистеин путем направленного мутагенеза. Флуорофор химически связан с мутантным цистеином. Если конструкция успешна, связанный флуорофор не предотвращает связывание антигена, это связывание защищает флуорофор от растворителя, и его можно обнаружить по изменению флуоресценции. Эта стратегия также действительна для фрагментов антител. [52] [53]
Однако при отсутствии конкретных структурных данных необходимо применять другие стратегии. Антитела и искусственные семейства AgBP состоят из набора гипервариабельных (или рандомизированных) положений остатков, расположенных в уникальной субобласти белка и поддерживаемых постоянным полипептидным каркасом. Остатки, образующие сайт связывания данного антигена, выбираются среди гипервариабельных остатков. Любой AgBP из этих семейств можно превратить в радиочастотный биосенсор, специфичный в отношении целевого антигена, просто соединив сольватохромный флуорофор с одним из гипервариабельных остатков, мало или вообще не имеющих значения для взаимодействия с антигеном, после замены этого остатка. в цистеин путем мутагенеза. Точнее, стратегия заключается в индивидуальной замене остатков гипервариабельных позиций на цистеин на генетическом уровне, химическом соединении сольватохромного флуорофора с мутантным цистеином, а затем в сохранении полученных конъюгатов, обладающих наибольшей чувствительностью (параметр, включающий в себя как сродство, так и изменение сигнала флуоресценции). [21] Этот подход также справедлив для семейств фрагментов антител. [54]
Апостериорные исследования показали, что лучшие безреагентные флуоресцентные биосенсоры получаются тогда, когда флуорофор не осуществляет нековалентных взаимодействий с поверхностью биорецептора, приводящих к увеличению фонового сигнала, и когда он взаимодействует с карманом связывания на поверхности биорецептора. целевой антиген. [55] Радиочастотные биосенсоры, полученные вышеуказанными методами, могут функционировать и обнаруживать целевые аналиты внутри живых клеток. [56]
Магнитные биосенсоры используют парамагнитные или супрапарамагнитные частицы или кристаллы для обнаружения биологических взаимодействий. Примерами могут быть индуктивность катушки, сопротивление или другие магнитные свойства. Обычно используют магнитные нано- или микрочастицы. На поверхности таких частиц находятся биорецепторы, которыми могут быть ДНК (комплементарные последовательности или аптамеры), антитела или другие. Связывание биорецептора повлияет на некоторые свойства магнитных частиц, которые можно измерить с помощью суссептометрии переменного тока, [57] датчика Холла, [58] гигантского магниторезистивного устройства [59] или других.
В пьезоэлектрических датчиках используются кристаллы, которые подвергаются упругой деформации при приложении к ним электрического потенциала. Переменный потенциал (AC) создает в кристалле стоячую волну характерной частоты. Эта частота сильно зависит от упругих свойств кристалла, так что, если кристалл покрыт элементом биологического распознавания, связывание (большого) целевого аналита с рецептором приведет к изменению резонансной частоты, что дает связывание сигнал. В режиме, использующем поверхностные акустические волны (ПАВ), чувствительность значительно увеличивается. Это специализированное применение кварцевых микровесов в качестве биосенсора.
Электрохемилюминесценция (ЭКЛ) в настоящее время является ведущим методом биосенсоров. [60] [61] [62] Поскольку возбужденные частицы производятся с помощью электрохимического стимула, а не с помощью источника светового возбуждения, ECL демонстрирует улучшенное соотношение сигнал/шум по сравнению с фотолюминесценцией, с минимальными эффектами из-за рассеяния света и фона люминесценции. . В частности, сореагент ECL, работающий в забуференном водном растворе в области положительных потенциалов (окислительно-восстановительный механизм), окончательно усилил ECL для иммуноанализа, что подтверждается многими исследовательскими приложениями и, более того, наличием важных компаний, которые разработали коммерческое оборудование для высокопроизводительный иммуноанализ на рынке стоимостью в миллиарды долларов каждый год.
Термометрические биосенсоры встречаются редко.
МОП -транзистор (полевой транзистор металл-оксид-полупроводник, или МОП-транзистор) был изобретен Мохамедом М. Аталлой и Давоном Кангом в 1959 году и продемонстрирован в 1960 году . [63] Два года спустя Леланд К. Кларк и Чемп Лайонс изобрели первый биосенсор был создан в 1962 году. [64] [65] Позже были разработаны биосенсорные МОП-транзисторы (BioFET), и с тех пор они широко используются для измерения физических , химических , биологических параметров и параметров окружающей среды . [66]
Первым BioFET был ионно-чувствительный полевой транзистор (ISFET), изобретенный Питом Бергвельдом для электрохимических и биологических применений в 1970 году . [67] [68] адсорбционный полевой транзистор (ADFET) был запатентован П.Ф. Чувствительный к водороду МОП-транзистор был продемонстрирован И. Лундстремом, М. С. Шивараманом, К. С. Свенсоном и Л. Лундквистом в 1975 году. [66] ISFET представляет собой особый тип MOSFET с затвором на определенном расстоянии [66] и металлическим затвором. заменяется ионочувствительной мембраной , раствором электролита и электродом сравнения . [69] ISFET широко используется в биомедицинских приложениях, таких как обнаружение гибридизации ДНК , обнаружение биомаркеров в крови , обнаружение антител , измерение уровня глюкозы , измерение pH и генетические технологии . [69]
К середине 1980-х годов были разработаны другие BioFET, в том числе полевой транзистор с датчиком газа (GASFET), полевой транзистор с датчиком давления (PRESSFET), химический полевой транзистор (ChemFET), эталонный ISFET (REFET), модифицированный ферментами полевой транзистор (ENFET). и иммунологически модифицированный полевой транзистор (IMFET). [66] К началу 2000-х годов были разработаны такие биополевые транзисторы, как полевой транзистор ДНК (DNAFET), генно-модифицированный полевой транзистор (GenFET) и биополевой транзистор клеточного потенциала (CPFET). [69]
Подходящее размещение биосенсоров зависит от области их применения, которую можно условно разделить на биотехнологию , сельское хозяйство , пищевую технологию и биомедицину .
В биотехнологии анализ химического состава культивационного бульона может проводиться в режиме онлайн, в режиме онлайн, в режиме онлайн и автономно. Как указано Управлением по контролю за продуктами и лекарствами США ( FDA ), образец не удаляется из технологического потока для встроенных датчиков, но выводится из производственного процесса для онлайн-измерений. Для встроенных датчиков пробу можно отбирать и анализировать в непосредственной близости от технологического потока. [70] Примером последнего является мониторинг лактозы на заводе по переработке молочной продукции. [71] Автономные биосенсоры можно сравнить с биоаналитическими методами , которые работают не в полевых условиях, а в лаборатории. Эти методы в основном используются в сельском хозяйстве, пищевых технологиях и биомедицине.
В медицинских целях биосенсоры обычно делятся на системы in vitro и in vivo . Измерения с помощью биосенсора in vitro проводятся в пробирке, культуральной чашке, микротитрационном планшете или где-либо еще вне живого организма. Датчик использует биорецептор и преобразователь, как описано выше. Примером биосенсора in vitro является ферментно-кондуктиметрический биосенсор для мониторинга уровня глюкозы в крови . Существует задача создания биосенсора, работающего по принципу тестирования на месте , то есть в том месте, где необходимо провести тест. [72] [73] Одним из таких исследований является разработка носимых биосенсоров. [74] Отказ от лабораторных исследований может сэкономить время и деньги. Биосенсор POCT может применяться для тестирования на ВИЧ в районах, где пациентам трудно пройти тестирование. Биосенсор можно отправить прямо на место и провести быстрый и простой тест.

Биосенсор in vivo — это имплантируемое устройство , которое работает внутри тела. Конечно, биосенсорные имплантаты должны соответствовать строгим правилам стерилизации , чтобы избежать первоначальной воспалительной реакции после имплантации. Вторая проблема связана с долгосрочной биосовместимостью , то есть безвредным взаимодействием с окружающей средой организма в течение предполагаемого периода использования. [76] Еще одна проблема, которая возникает, — это отказ. В случае неисправности устройство необходимо снять и заменить, что приведет к дополнительной операции. Примером применения биосенсора in vivo может быть мониторинг инсулина в организме, который пока недоступен.
Большинство современных биосенсорных имплантатов были разработаны для непрерывного мониторинга уровня глюкозы. [77] [78] На рисунке показано устройство, в котором используется титановый корпус и батарея, установленная для сердечно-сосудистых имплантатов, таких как кардиостимуляторы и дефибрилляторы . [75] Его размер определяется батареей в соответствии с требованиями на срок службы в один год. Данные измерений уровня глюкозы будут передаваться из организма по беспроводной сети в диапазоне MICS 402–405 МГц, одобренном для медицинских имплантатов.
Биосенсоры также могут быть интегрированы в системы мобильных телефонов, что делает их удобными и доступными для большого числа пользователей. [79]

Существует множество потенциальных применений биосенсоров различных типов. Основными требованиями, чтобы биосенсорный подход был ценным с точки зрения исследований и коммерческого применения, являются идентификация целевой молекулы, наличие подходящего элемента биологического распознавания и возможность того, что одноразовые портативные системы обнаружения будут предпочтительнее чувствительных лабораторных методов. в некоторых ситуациях. Некоторые примеры:
Типичным примером коммерческого биосенсора является биосенсор глюкозы в крови , который использует фермент глюкозооксидазу для расщепления глюкозы в крови. При этом он сначала окисляет глюкозу и использует два электрона для восстановления FAD (компонента фермента) до FADH 2 . Он, в свою очередь, окисляется электродом в несколько этапов. Результирующий ток является мерой концентрации глюкозы. В этом случае электрод является преобразователем, а фермент – биологически активным компонентом.
Канарейку в клетке , которую шахтеры используют для предупреждения о газе, можно считать биосенсором. Многие из сегодняшних применений биосенсоров аналогичны тем, что они используют организмы, которые реагируют на токсичные вещества в гораздо более низких концентрациях, чем люди могут обнаружить, чтобы предупредить об их присутствии. Такие устройства могут использоваться для мониторинга окружающей среды , [81] обнаружения газовых примесей и на водоочистных сооружениях.
Коммерчески доступные мониторы глюкозы основаны на амперометрическом измерении глюкозы с помощью глюкозооксидазы , которая окисляет глюкозу с образованием перекиси водорода, которая обнаруживается электродом. Чтобы преодолеть ограничения амперометрических датчиков, проводится множество исследований в области новых методов измерения, таких как флуоресцентные биосенсоры глюкозы . [83]
Датчик изображения интерферометрического отражения (IRIS) основан на принципах оптической интерференции и состоит из кремниево-оксидной подложки, стандартной оптики и маломощных когерентных светодиодов. Когда свет освещается через объектив с малым увеличением на многослойную подложку из оксида кремния-кремния, создается интерферометрическая сигнатура. Поскольку биомасса, которая имеет такой же показатель преломления , как и оксид кремния, накапливается на поверхности подложки, происходит изменение интерферометрической сигнатуры, и это изменение можно соотнести с поддающейся количественной оценке массой. Даабул и др. использовали IRIS, чтобы получить чувствительность без метки примерно 19 нг/мл. [84] Ан и др. улучшили чувствительность IRIS за счет метода массового мечения. [85]
С момента первой публикации IRIS был адаптирован для выполнения различных функций. Во-первых, IRIS интегрировала функцию флуоресцентной визуализации в прибор для интерферометрической визуализации в качестве потенциального способа решения проблемы изменчивости микрочипов флуоресцентных белков. [86] Вкратце, изменения флуоресцентных микрочипов в основном происходят из-за непостоянной иммобилизации белков на поверхностях и могут вызывать ошибочный диагноз при использовании микрочипов аллергии. [87] Чтобы скорректировать любые изменения в иммобилизации белка, данные, полученные в режиме флуоресценции, затем нормализуются по данным, полученным в режиме без метки. [87] IRIS также был адаптирован для подсчета одиночных наночастиц путем простого переключения объектива с низким увеличением, используемого для количественного определения биомассы без меток, на более высокое увеличение объектива. [88] [89] Этот метод позволяет различать размеры сложных биологических образцов человека. Монро и др. использовали IRIS для количественной оценки уровней белка, добавленного в цельную кровь и сыворотку человека, и определили сенсибилизацию аллергена в охарактеризованных образцах крови человека, используя нулевую обработку образцов. [90] Другие практические применения этого устройства включают обнаружение вирусов и патогенов. [91]
Существует несколько применений биосенсоров в анализе пищевых продуктов. [92] [93] [94] [95] В пищевой промышленности оптика, покрытая антителами, обычно используется для обнаружения патогенов и пищевых токсинов. Обычно световая система в этих биосенсорах представляет собой флуоресценцию, поскольку этот тип оптических измерений может значительно усиливать сигнал.
Для использования в сенсорных системах на основе SPR был разработан ряд иммуно- и лиганд-связывающих анализов для обнаружения и измерения малых молекул, таких как водорастворимые витамины и химические примеси ( остатки лекарств ), такие как сульфонамиды и бета-агонисты . адаптирован на основе существующего ИФА или другого иммунологического анализа. Они широко используются в пищевой промышленности.
Биосенсоры можно использовать для мониторинга загрязнителей воздуха , воды и почвы, таких как пестициды, потенциально канцерогенные, мутагенные и/или токсичные вещества, а также химические вещества, нарушающие работу эндокринной системы. [96] [97]
Например, бионанотехнологи разработали жизнеспособный биосенсор ROSALIND 2.0 , который может определять уровни различных загрязнителей воды . [98] [99]
Поскольку озон отфильтровывает вредное ультрафиолетовое излучение, открытие дыр в озоновом слое земной атмосферы вызвало обеспокоенность по поводу того, сколько ультрафиолетового света достигает земной поверхности. Особое беспокойство вызывают вопросы о том, насколько глубоко в морскую воду проникает ультрафиолетовое излучение и как оно влияет на морские организмы , особенно на планктон (плавающие микроорганизмы) и вирусы , поражающие планктон. Планктон составляет основу морских пищевых цепей и, как полагают, влияет на температуру и погоду на нашей планете, поглощая CO 2 для фотосинтеза.
Денеб Каренц, исследователь из Лаборатории радиобиологии и гигиены окружающей среды ( Калифорнийский университет, Сан-Франциско ) разработал простой метод измерения проникновения и интенсивности ультрафиолета. Работая в Антарктическом океане, она погружала на разную глубину тонкие пластиковые пакеты, содержащие особые штаммы кишечной палочки , которые почти полностью неспособны восстанавливать повреждения своей ДНК, вызванные ультрафиолетовым излучением. Уровень бактериальной смертности в этих мешках сравнивали с показателями в неэкспонированных контрольных мешках с тем же организмом. Бактериальные «биосенсоры» обнаруживали постоянное значительное повреждение ультрафиолетом на глубинах 10 м, а часто и на 20 и 30 м. Каренц планирует провести дополнительные исследования того, как ультрафиолет может повлиять на сезонное цветение планктона (всплески роста) в океанах. [100]
Метастазирование – это распространение рака из одной части тела в другую через систему кровообращения или лимфатическую систему. [101] В отличие от рентгенологических методов визуализации (маммографии), которые посылают различные виды энергии (рентгеновские лучи, магнитные поля и т. д.) через тело, чтобы сделать только внутренние снимки, биосенсоры могут напрямую проверять злокачественную силу опухоли. Комбинация биологического и детекторного элемента обеспечивает небольшую потребность в образце, компактную конструкцию, быстрые сигналы, быстрое обнаружение, высокую селективность и высокую чувствительность к исследуемому аналиту. По сравнению с обычными рентгенологическими визуализирующими тестами биосенсоры имеют преимущество: они не только позволяют определить, насколько далеко распространился рак, и проверить эффективность лечения, но также являются более дешевыми и эффективными (по времени, затратам и производительности) способами оценки метастазирования на ранних стадиях. рак.
Исследователи биологической инженерии создали онкологические биосенсоры для рака молочной железы. [102] Рак молочной железы является наиболее распространенным раком среди женщин во всем мире. [103] Примером могут служить микровесы трансферрин-кварц (QCM). В качестве биосенсора кварцевые микровесы производят колебания частоты стоячей волны кристалла под действием переменного потенциала для обнаружения изменений массы нанограммов. Эти биосенсоры специально разработаны для взаимодействия и обладают высокой селективностью в отношении рецепторов на поверхности клеток (раковых и нормальных). В идеале это обеспечивает количественное обнаружение клеток с этим рецептором на площади поверхности вместо качественного обнаружения изображения, даваемого маммографией.
Седа Атай, исследователь биотехнологий из Университета Хаджеттепе, экспериментально наблюдала эту специфичность и селективность между QCM и клетками молочной железы MDA-MB 231 , клетками MCF 7 и голодавшими клетками MDA-MB 231 in vitro. [102] Вместе с другими исследователями она разработала метод промывания этих клеток с различным метастатическим уровнем над датчиками, чтобы измерить сдвиг массы из-за различного количества рецепторов трансферрина. В частности, метастатическая сила клеток рака молочной железы может быть определена с помощью кварцевых микровесов с наночастицами и трансферрином, которые потенциально могут прикрепляться к рецепторам трансферрина на поверхности раковых клеток. Рецепторы трансферрина обладают очень высокой селективностью, поскольку они сверхэкспрессируются в раковых клетках. Если клетки имеют высокую экспрессию рецепторов трансферрина, что свидетельствует об их высокой метастатической способности, они имеют более высокое сродство и больше связываются с QCM, который измеряет увеличение массы. В зависимости от величины изменения массы нанограммов можно определить метастатическую силу.
Кроме того, в последние годы значительное внимание было сосредоточено на выявлении биомаркеров рака легких без биопсии. В этом отношении биосенсоры являются очень привлекательными и применимыми инструментами для обеспечения быстрого, чувствительного, специфичного, стабильного, экономически эффективного и неинвазивного обнаружения рака легких на ранней стадии. Таким образом, биосенсоры рака состоят из специфических молекул биораспознавания, таких как антитела, зонды комплементарных нуклеиновых кислот или другие иммобилизованные биомолекулы на поверхности преобразователя. Молекулы биораспознавания специфически взаимодействуют с биомаркерами (мишенями), и генерируемые биологические ответы преобразуются преобразователем в измеримый аналитический сигнал. В зависимости от типа биологической реакции при изготовлении биосенсоров рака используются различные датчики, такие как электрохимические, оптические и массовые датчики. [104]
Биосенсоры могут использоваться для обнаружения патогенных организмов. [97]
Были разработаны встраиваемые носимые биосенсоры для выявления патогенных сигнатур, таких как SARS-CoV-2 , например, маски для лица со встроенными тестами . [105] [106] См. также: НИОКР в области общественного транспорта в связи с COVID-19.
Новые типы биосенсорных чипов могут позволить использовать новые методы, «такие как датчики патогенов, устанавливаемые с помощью дронов, активно исследующие воздух или сточные воды». Белковые аптамеры можно использовать для тестирования на возбудители инфекционных заболеваний. [107] Системы электронных скинов (или скинов роботов) со встроенными биосенсорами (или химическими сенсорами) и человеко-машинным интерфейсом могут обеспечить возможность носимого, а также дистанционного или роботизированного обнаружения патогенов (а также некоторых опасных материалы и тактильные ощущения ). [108] [ необходимы дополнительные ссылки ]
Многие оптические биосенсоры основаны на явлении поверхностного плазмонного резонанса (ППР). [109] [110] Здесь используются свойства золота и других материалов (металлов); В [111] в частности, тонкий слой золота на поверхности стекла с высоким показателем преломления может поглощать лазерный свет, создавая электронные волны (поверхностные плазмоны) на поверхности золота. Это происходит только при определенном угле и длине волны падающего света и сильно зависит от поверхности золота, так что связывание целевого аналита с рецептором на поверхности золота дает измеримый сигнал.
Датчики поверхностного плазмонного резонанса работают с использованием сенсорного чипа, состоящего из пластиковой кассеты, несущей стеклянную пластину, одна сторона которой покрыта микроскопическим слоем золота. Эта сторона контактирует с оптическим детектором прибора. Противоположная сторона затем контактирует с микрофлюидной системой потока. Контакт с проточной системой создает каналы, по которым реагенты могут проходить в растворе. Эту сторону стеклянного сенсорного чипа можно модифицировать разными способами, чтобы обеспечить легкое прикрепление интересующих молекул. Обычно он покрыт карбоксиметилдекстраном или аналогичным соединением.
Показатель преломления на проточной стороне поверхности чипа оказывает прямое влияние на поведение света, отраженного от золотой стороны. Связывание с проточной стороной чипа влияет на показатель преломления , и таким образом биологические взаимодействия могут быть измерены с высокой степенью чувствительности с использованием той или иной энергии. Показатель преломления среды вблизи поверхности изменяется, когда биомолекулы прикрепляются к поверхности, и угол ППР меняется в зависимости от этого изменения.
Свет фиксированной длины волны отражается от золотой стороны чипа под углом полного внутреннего отражения и обнаруживается внутри прибора. Угол падающего света варьируется, чтобы согласовать скорость распространения затухающей волны со скоростью распространения поверхностных плазмонных поляритонов. [112] Это заставляет затухающую волну проникать через стеклянную пластину и на некоторое расстояние в жидкость, текущую по поверхности.
Другие оптические биосенсоры в основном основаны на изменении поглощения или флуоресценции соответствующего индикаторного соединения и не требуют геометрии полного внутреннего отражения. Например, был изготовлен полностью работоспособный прототип устройства для обнаружения казеина в молоке. Устройство основано на обнаружении изменений в поглощении золотого слоя. [113] Широко используемый исследовательский инструмент — микрочип — также можно считать биосенсором.
Биологические биосенсоры, также известные как оптогенетические сенсоры , часто включают в себя генетически модифицированную форму нативного белка или фермента. Белок настроен на обнаружение конкретного аналита, а полученный сигнал считывается прибором обнаружения, таким как флуорометр или люминометр. Примером недавно разработанного биосенсора является биосенсор для определения цитозольной концентрации аналита цАМФ (циклического аденозинмонофосфата), вторичного мессенджера, участвующего в клеточной передаче сигналов, запускаемой лигандами, взаимодействующими с рецепторами на клеточной мембране. [114] Подобные системы были созданы для изучения клеточных ответов на нативные лиганды или ксенобиотики (токсины или низкомолекулярные ингибиторы). Такие «анализы» обычно используются фармацевтическими и биотехнологическими компаниями при разработке лекарств. Большинство используемых в настоящее время анализов цАМФ требуют лизиса клеток перед измерением цАМФ. Биосенсор живых клеток для цАМФ можно использовать в нелизированных клетках с дополнительным преимуществом многократного чтения для изучения кинетики ответа рецептора.
В нанобиосенсорах используется иммобилизованный биорецепторный зонд, избирательно реагирующий на целевые молекулы аналита. Наноматериалы являются чрезвычайно чувствительными химическими и биологическими сенсорами. Наноразмерные материалы демонстрируют уникальные свойства. Их большое соотношение площади поверхности к объему позволяет добиться быстрых и недорогих реакций за счет использования различных конструкций. [115]
Другие биосенсоры затухающих волн были коммерциализированы с использованием волноводов, в которых константа распространения по волноводу изменяется за счет поглощения молекул поверхностью волновода. Одним из таких примеров является интерферометрия с двойной поляризацией , в которой в качестве эталона используется заглубленный волновод, по которому измеряется изменение постоянной распространения. Другие конфигурации, такие как Маха – Цендер, имеют опорные плечи, литографически определенные на подложке. Более высокий уровень интеграции может быть достигнут при использовании геометрии резонатора, при которой резонансная частота кольцевого резонатора изменяется при поглощении молекул. [116] [117]
Недавно массивы из множества различных молекул-детекторов были применены в так называемых устройствах «электронный нос» , где образец отклика детекторов используется для определения отпечатков веществ. [118] В детекторе запаха Wasp Hound механическим элементом является видеокамера, а биологическим элементом — пять ос-паразитов, которые были приучены роиться в ответ на присутствие определенного химического вещества. [119] Однако современные коммерческие электронные носы не используют биологические элементы.
ДНК может быть аналитом биосенсора, обнаруживаемая специальными средствами, но ее также можно использовать как часть биосенсора или, теоретически, даже как целый биосенсор.
Существует множество методов обнаружения ДНК, что обычно является средством обнаружения организмов, имеющих эту конкретную ДНК. Последовательности ДНК также можно использовать, как описано выше. Но существуют более дальновидные подходы, при которых можно синтезировать ДНК, чтобы удерживать ферменты в биологическом, стабильном геле. [120] Другие применения — создание аптамеров, последовательностей ДНК, которые имеют специфическую форму для связывания желаемой молекулы. Самые инновационные процессы используют для этого ДНК-оригами , создавая последовательности, которые складываются в предсказуемую структуру, полезную для обнаружения. [121] [122]
Ученые создали прототип датчиков для обнаружения ДНК животных из всасываемого воздуха, «воздушной эДНК». [123]
«Наноантенны», сделанные из ДНК – новый тип наноразмерной оптической антенны – могут быть прикреплены к белкам и генерировать сигнал посредством флуоресценции , когда они выполняют свои биологические функции, в частности, при определенных конформационных изменениях . [124] [125]
Графен — это двумерное вещество на основе углерода с превосходными оптическими, электрическими, механическими, термическими и механическими свойствами. Способность поглощать и иммобилизовать различные белки, особенно некоторые из которых имеют структуру углеродного кольца, доказала, что графен является отличным кандидатом в качестве биосенсорного преобразователя. В результате в последнее время были исследованы и разработаны различные биосенсоры на основе графена. [14] [126] Графен использовался в качестве биосенсора в различных форматах, особенно в электрохимических сенсорах и полевых транзисторах. Среди них графеновые полевые транзисторы (GFET) особенно показали отличные характеристики в качестве быстрой диагностики на месте оказания медицинской помощи (PoC), о чем свидетельствует резкое увеличение числа исследовательских статей, в которых сообщается о диагностике COVID-19 с использованием GFET. Сообщается, что они имеют один из самых низких пределов обнаружения, но при этом имеют быстрое время оборота в несколько секунд и возможности мультиплексирования. [127] Эти возможности позволяют немедленно выявлять заболевания, особенно в случаях с перекрывающимися симптомами, которые трудно различить на начальном этапе, что позволяет улучшить результаты лечения пациентов, особенно в медицинских учреждениях с ограниченными ресурсами.
{{cite web}}: CS1 maint: архивная копия в заголовке ( ссылка )(по состоянию на 30 января 2013 г.).