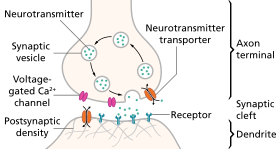
Нейротрансмиссия (лат. transmissio «прохождение, пересечение» от « трансмиттере » «отправлять, пропускать») — это процесс, посредством которого сигнальные молекулы, называемые нейротрансмиттерами , высвобождаются окончанием аксона нейрона ( пресинаптическим нейроном), связываются с ним и реагируют с ним. рецепторы на дендритах другого нейрона (постсинаптического нейрона), находящегося на небольшом расстоянии. Аналогичный процесс происходит при ретроградной нейротрансмиссии , когда дендриты постсинаптического нейрона высвобождают ретроградные нейротрансмиттеры (например, эндоканнабиноиды ; синтезируются в ответ на повышение внутриклеточных уровней кальция ), которые передают сигналы через рецепторы, расположенные на окончаниях аксонов пресинаптического нейрона. главным образом в ГАМКергических и глутаматергических синапсах . [1] [2] [3] [4]
Нейротрансмиссия регулируется несколькими различными факторами: доступностью и скоростью синтеза нейромедиатора, высвобождением этого нейромедиатора, базовой активностью постсинаптической клетки, количеством доступных постсинаптических рецепторов, с которыми нейромедиатор может связываться, и последующими удаление или дезактивация нейромедиатора ферментами или пресинаптическим обратным захватом. [5] [6]
В ответ на пороговый потенциал действия или градуированный электрический потенциал в пресинаптическом терминале высвобождается нейромедиатор . Высвобожденный нейротрансмиттер может затем перемещаться через синапс, чтобы быть обнаруженным и связываться с рецепторами постсинаптического нейрона. Связывание нейротрансмиттеров может влиять на постсинаптический нейрон как тормозным , так и возбуждающим образом. Связывание нейротрансмиттеров с рецепторами постсинаптического нейрона может вызвать либо краткосрочные изменения, такие как изменения мембранного потенциала , называемые постсинаптическими потенциалами , либо долгосрочные изменения за счет активации сигнальных каскадов .
Нейроны образуют сложные биологические нейронные сети, по которым проходят нервные импульсы (потенциалы действия). Нейроны не соприкасаются друг с другом (за исключением случая электрического синапса через щелевой переход ); вместо этого нейроны взаимодействуют в точках тесного контакта, называемых синапсами. Нейрон передает информацию посредством потенциала действия. Когда нервный импульс достигает синапса, он может вызвать высвобождение нейромедиаторов, которые влияют на другой (постсинаптический) нейрон. Постсинаптический нейрон может получать входные сигналы от многих дополнительных нейронов, как возбуждающих, так и тормозных. Возбуждающее и тормозящее влияния суммируются, и если суммарный эффект является тормозящим, то нейрон с меньшей вероятностью «сработает» (т. е. создаст потенциал действия), а если суммарный эффект является возбуждающим, нейрон с большей вероятностью сработает. огонь. Насколько вероятно, что нейрон сработает, зависит от того, насколько далеко его мембранный потенциал находится от порогового потенциала , напряжения, при котором срабатывает потенциал действия, поскольку активируется достаточно зависимых от напряжения натриевых каналов , так что чистый внутренний натриевый ток превышает все внешние токи. [7] Возбуждающие входы приближают нейрон к порогу, тогда как тормозящие входы приближают нейрон к порогу. Потенциал действия — это событие «все или ничего»; нейроны, мембраны которых не достигли порога, не сработают, а те, которые достигли порога, должны сработать. Как только потенциал действия инициируется (традиционно в бугорке аксона ), он распространяется вдоль аксона, что приводит к высвобождению нейротрансмиттеров в синаптическом бутоне для передачи информации еще одному соседнему нейрону.
Нейромедиаторы спонтанно упаковываются в везикулы и высвобождаются отдельными квантовыми пакетами независимо от пресинаптических потенциалов действия. Это медленное высвобождение заметно и оказывает микротормозное или микровозбуждающее действие на постсинаптический нейрон. Потенциал действия кратковременно усиливает этот процесс. Нейротрансмиттеры, содержащие везикулы, группируются вокруг активных центров и после высвобождения могут быть переработаны с помощью одного из трех предложенных механизмов. Первый предложенный механизм включает частичное открытие, а затем повторное закрытие пузырька. Вторые два предусматривают полное слияние пузырька с мембраной с последующей рециркуляцией или рециркуляцией в эндосому. Везикулярное слияние во многом обусловлено концентрацией кальция в микродоменах, расположенных вблизи кальциевых каналов, что обеспечивает высвобождение нейротрансмиттера всего лишь в течение микросекунд, тогда как возвращение к нормальной концентрации кальция занимает пару сотен микросекунд. Считается, что экзоцитоз везикул управляется белковым комплексом под названием SNARE , который является мишенью для ботулинических токсинов . После высвобождения нейромедиатор попадает в синапс и встречает рецепторы. Рецепторы нейромедиаторов могут быть либо ионотропными, либо связанными с g-белком. Ионотропные рецепторы пропускают ионы при воздействии лиганда. Основная модель включает в себя рецептор, состоящий из нескольких субъединиц, которые позволяют координировать предпочтение ионов. Рецепторы, связанные с G-белком, также называемые метаботропными рецепторами, при связывании с лигандом претерпевают конформационные изменения, приводящие к внутриклеточному ответу. Прекращение активности нейромедиатора обычно осуществляется транспортером, однако возможна и ферментативная дезактивация. [9]
Каждый нейрон соединяется с множеством других нейронов, получая от них множество импульсов. Суммирование – это сложение этих импульсов на аксонном бугорке. Если нейрон получает только возбуждающие импульсы, он генерирует потенциал действия. Если вместо этого нейрон получит столько же тормозных импульсов, сколько и возбуждающих, торможение нейтрализует возбуждение, и нервный импульс на этом остановится. [10] Генерация потенциала действия пропорциональна вероятности и характеру высвобождения нейротрансмиттера, а также сенсибилизации постсинаптических рецепторов. [11] [12] [13]
Пространственное суммирование означает, что эффекты импульсов, полученных в разных местах нейрона, суммируются, так что нейрон может сработать, когда такие импульсы получены одновременно, даже если каждого импульса по отдельности будет недостаточно, чтобы вызвать срабатывание.
Временное суммирование означает, что эффекты импульсов, полученных в одном и том же месте, могут суммироваться, если импульсы получены в тесной временной последовательности. Таким образом, нейрон может сработать при получении нескольких импульсов, даже если каждого импульса по отдельности будет недостаточно, чтобы вызвать срабатывание. [14]
Нейротрансмиссия предполагает как конвергенцию, так и расхождение информации. Сначала на один нейрон влияют многие другие, что приводит к конвергенции входных данных. Когда нейрон срабатывает, сигнал отправляется многим другим нейронам, что приводит к расхождению выходных сигналов. Многие другие нейроны находятся под влиянием этого нейрона. [ нужна цитата ]
Котрансмиссия — это высвобождение нескольких типов нейромедиаторов из одного нервного окончания .
В нервном окончании нейротрансмиттеры присутствуют в мембранных везикулах размером 35–50 нм, называемых синаптическими везикулами . Чтобы высвободить нейромедиаторы, синаптические пузырьки временно стыкуются и сливаются у основания специализированных липопротеиновых структур чашеобразной формы размером 10–15 нм на пресинаптической мембране, называемых поросомами . [15] Протеом нейрональной поросомы был решен, обеспечивая молекулярную архитектуру и полный состав механизмов. [16]
Недавние исследования множества систем показали, что большинство, если не все, нейроны выделяют несколько различных химических посланников. [17] Котрансмиссия позволяет оказывать более сложные эффекты на постсинаптические рецепторы и, таким образом, обеспечивает более сложную связь между нейронами.
В современной нейробиологии нейроны часто классифицируются по их котрансмиттеру. Например, стриарные «ГАМКергические нейроны» используют опиоидные пептиды или вещество Р в качестве основного котрансмиттера.
Некоторые нейроны могут высвобождать по крайней мере два нейротрансмиттера одновременно, причем другой является котрансмиттером, чтобы обеспечить стабилизирующую отрицательную обратную связь, необходимую для значимого кодирования, в отсутствие тормозных интернейронов . [18] Примеры:
Норадреналин и АТФ являются симпатическими комедиаторами. Обнаружено, что эндоканнабиноид анадамид и каннабиноид WIN 55,212-2 могут изменять общий ответ на стимуляцию симпатических нервов и указывают на то, что пресинаптические рецепторы CB1 опосредуют симпато -ингибирующее действие. Таким образом, каннабиноиды могут ингибировать как норадренергический, так и пуринергический компоненты симпатической нейротрансмиссии. [19]
Одной из необычных пар котрансмиттеров являются ГАМК и глутамат, которые высвобождаются из одних и тех же окончаний аксонов нейронов, происходящих из вентральной покрышки (ВТА), внутреннего бледного шара и супрамаммилярного ядра . [20] Первые два выступают на хабенулу , тогда как известно, что проекции супрамаммилярного ядра нацелены на зубчатую извилину гиппокампа. [20]
Нейротрансмиссия генетически связана с другими характеристиками или особенностями. Например, анализ обогащения различных сигнальных путей привел к открытию генетической связи с внутричерепным объемом. [21]
Таким образом, вполне возможно, что низкие уровни рецепторов CB1 расположены на глутаматергических и ГАМКергических окончаниях, воздействующих на DA-нейроны [127, 214], где они могут точно регулировать высвобождение тормозного и возбуждающего нейротрансмиттера и регулировать активацию DA-нейронов.
Таким образом, электрофизиологические эксперименты in vitro, проведенные независимыми лабораториями, предоставили доказательства локализации рецептора CB1 на глутаматергических и ГАМКергических окончаниях аксонов в VTA и SNc.
Прямое взаимодействие CB1-HcrtR1 было впервые предложено в 2003 году (Hilairet et al., 2003).
Действительно, 100-кратное увеличение способности гипокретина-1 активировать передачу сигналов ERK наблюдалось при совместной экспрессии CB1 и HcrtR1... В этом исследовании более высокая способность гипокретина-1 регулировать гетеромер CB1-HcrtR1 по сравнению с с гомомером HcrtR1-HcrtR1 сообщалось (Ward et al., 2011b).
Эти данные позволяют однозначно идентифицировать гетеромеризацию CB1-HcrtR1, имеющую существенное функциональное значение.
... Существование перекрестных помех между гипокретинергической и эндоканнабиноидной системами убедительно подтверждается их частично перекрывающимся анатомическим распределением и общей ролью в нескольких физиологических и патологических процессах.
Однако мало что известно о механизмах, лежащих в основе этого взаимодействия.
... Действуя как ретроградный мессенджер, эндоканнабиноиды модулируют глутаматергические возбуждающие и ГАМКергические тормозные синаптические входы в дофаминергические нейроны VTA и передачу глутамата в NAc.
Таким образом, активация рецепторов CB1, присутствующих на окончаниях аксонов ГАМКергических нейронов в ВТА, ингибирует передачу ГАМК, устраняя это ингибирующее воздействие на дофаминергические нейроны (Riegel and Lupica, 2004).
Глутаматная синаптическая передача в VTA и NAc, преимущественно от нейронов PFC, аналогичным образом модулируется активацией рецепторов CB1 (Melis et al., 2004).