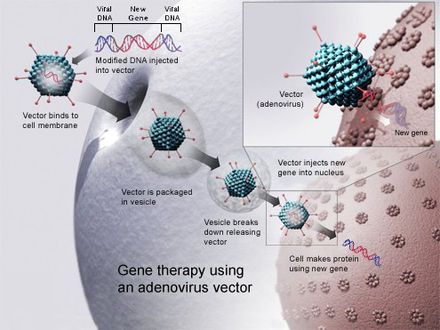
Генный допинг – это гипотетическое нетерапевтическое использование генной терапии спортсменами с целью улучшения своих результатов в тех спортивных соревнованиях , которые запрещают такое применение технологии генетической модификации [1] [2] и по причинам, не связанным с лечением заболевания. По состоянию на апрель 2015 года [update]нет никаких доказательств того, что генный допинг использовался для улучшения спортивных результатов на каких-либо спортивных мероприятиях. [1] Генное допинг будет включать использование переноса генов для увеличения или уменьшения экспрессии генов и биосинтеза белка конкретного человеческого белка; это можно сделать путем прямой инъекции генного носителя человеку или путем взятия клеток у человека, трансфекции клеток и введения клеток обратно человеку. [1]
Историческое развитие интереса спортсменов к генному допингу и обеспокоенность по поводу рисков генного допинга и способов его обнаружения развивались параллельно с развитием области генной терапии, особенно с публикацией в 1998 году работы о трансгенных мышах, сверхэкспрессирующих инсулин . -подобный фактор роста 1 , который был намного сильнее, чем у нормальных мышей, даже в пожилом возрасте, в 2002 году были опубликованы доклинические исследования способа доставки эритропоэтина (ЭПО) с помощью генной терапии, а в 2004 году — публикация о создании «марафонской мыши» с гораздо большую выносливость, чем у обычных мышей, что достигается за счет доставки мышам гена, экспрессирующего гамма-PPAR . Со всеми учеными, создавшими эти публикации, напрямую связались спортсмены и тренеры, ищущие доступ к этой технологии. Общественность узнала об этой деятельности в 2006 году, когда подобные усилия стали частью доказательств, представленных в суде над немецким тренером.
Сами ученые, а также организации, в том числе Всемирное антидопинговое агентство (ВАДА), Международный олимпийский комитет и Американская ассоциация содействия развитию науки , начали обсуждать риск генного допинга в 2001 году, а к 2003 году ВАДА добавило генный допинг. допинг в список запрещенных допинговых практик и вскоре после этого начал финансировать исследования методов выявления генного допинга.
Генетическое улучшение включает в себя манипулирование генами или перенос генов здоровыми спортсменами с целью физического улучшения их результатов. Генетическое улучшение включает в себя генный допинг и потенциально может стать предметом злоупотреблений среди спортсменов, одновременно открывая двери для политических и этических разногласий. [3]
История беспокойства по поводу возможности генного допинга следует за историей генной терапии — медицинского использования генов для лечения заболеваний, которая впервые была клинически протестирована в 1990-х годах. [4] Интерес спортивного сообщества был особенно вызван созданием в университетской лаборатории «могучей мыши», созданной путем введения мышам вируса, несущего ген, экспрессирующий инсулиноподобный фактор роста 1 ; мыши были сильнее и оставались сильными даже с возрастом, без физических упражнений. [4] Лаборатория искала методы лечения заболеваний, связанных с атрофией мышц , но когда их работа была обнародована, лабораторию завалили звонками от спортсменов, ищущих лечение, причем один тренер предлагал всю свою команду. [5] В 2007 году учёный рассказал The New York Times : «Должен признаться, я был весьма удивлён. Люди пытались соблазнить меня, говоря что-то вроде: «Это поможет продвинуть ваши исследования». Некоторые предлагали мне заплатить». Он также рассказал Times , что каждый раз, когда публикуется подобное исследование, ему звонят и объясняют, что даже если лечение будет готово к использованию на людях, что займет годы, возникнут серьезные риски, включая смерть; он также сказал, что даже после того, как он это объяснит, спортсмены все равно этого хотят. [5]
В 1999 году область генной терапии была отброшена назад, когда Джесси Гелсингер умер во время клинических испытаний генной терапии, страдая от массивной воспалительной реакции на препарат. [4] [6] Это побудило регулирующие органы в США и Европе ужесточить требования к безопасности в клинических испытаниях даже за пределами первоначальных ограничений, которые были установлены в начале эры биотехнологий для борьбы с рисками, связанными с рекомбинантной ДНК . [7]
В июне 2001 года Теодор Фридман, один из пионеров генной терапии, и Иоганн Олав Косс , олимпийский чемпион по конькобежному спорту, опубликовали статью, которая стала первым публичным предупреждением о генном допинге. [7] [8] Также в июне 2001 года Рабочая группа по генной терапии, созванная Медицинской комиссией Международного олимпийского комитета, отметила, что «мы осознаем, что существует потенциал злоупотребления лекарствами для генной терапии, и мы начнем устанавливать процедуры и современные методы тестирования для выявления спортсменов, которые могут злоупотреблять такой технологией». [7]
В 2002 году было опубликовано исследование о доклинической генной терапии под названием Repoxygen , которая доставила ген, кодирующий эритропоэтин (ЭПО), в качестве потенциального средства лечения анемии . [4] Ученым из этой компании также звонили спортсмены и тренеры. [4] В том же году Всемирное антидопинговое агентство провело свое первое заседание, чтобы обсудить риск генного допинга, [7] [9] и Совет президента США по биоэтике на нескольких сессиях обсуждал генный допинг в контексте улучшения человека. . [10] [11] [12]
В 2003 году область генной терапии сделала шаг вперед и шаг назад; был одобрен первый препарат генной терапии, Гендицин , который был одобрен в Китае для лечения некоторых видов рака, [13] но у детей во Франции, которые, по-видимому, эффективно лечились генной терапией от тяжелого комбинированного иммунодефицита (нечеловеческого происхождения), начали заболевать лейкемией. [6] В 2003 году стал достоянием общественности скандал BALCO , в ходе которого химики, тренеры и спортсмены сговорились уклониться от допинг-контроля с помощью новых и необнаруживаемых допинговых веществ. [7] В 2003 году Всемирное допинговое агентство активно добавило генный допинг в список запрещенных допинговых практик. [4] Также в 2003 году этому вопросу был посвящен симпозиум, созванный Американской ассоциацией содействия развитию науки . [14]
Исследования, опубликованные в 2004 году, показали, что мыши, получавшие генную терапию, кодирующую белок под названием PPAR гамма, имели примерно вдвое большую выносливость, чем необработанные мыши, и их прозвали «мышами-марафонцами»; этим ученым звонили спортсмены и тренеры. [4] Также в 2004 году Всемирное антидопинговое агентство начало финансировать исследования по выявлению генного допинга и сформировало постоянную группу экспертов, которая консультировала его по рискам и руководила финансированием. [4] [9]
В 2006 году интерес спортсменов к генному допингу получил широкое освещение в средствах массовой информации благодаря его упоминанию во время суда над немецким тренером, который был обвинен и признан виновным в том, что давал своим спортсменам допинг без их ведома; Электронное письмо, в котором тренер пытался получить Repoxygen, было зачитано прокурором в открытом судебном заседании. [4] [5] Это было первое публичное раскрытие интереса спортсменов к генному допингу. [4]
В 2011 году был одобрен второй препарат генной терапии; Неоваскулген , доставляющий ген, кодирующий VEGF , одобрен в России для лечения заболеваний периферических артерий . [15] [16]
В 2012 году Glybera , препарат для лечения редкого наследственного заболевания , стал первым препаратом, одобренным для клинического использования в Европе и США. [17] [18]
По мере развития области генной терапии увеличивался и риск того, что генный допинг станет реальностью. [6]
Существует множество генов, представляющих интерес в качестве агентов генного допинга. [1] [19] [7] Они включают эритропоэтин , инсулиноподобный фактор роста 1 , гормон роста человека , миостатин , фактор роста эндотелия сосудов , фактор роста фибробластов , эндорфин , энкефалин и альфа-актинин-3 . [1] [19]
Риски генного допинга будут аналогичны рискам генной терапии: иммунная реакция на нативный белок приводит к эквиваленту генетического заболевания , массивной воспалительной реакции, раку и смерти, и во всех случаях эти риски будут предприниматься в течение короткого времени. -срочная выгода в отличие от лечения серьезного заболевания. [6] [7]
Альфа-актинин-3 обнаружен только в скелетных мышцах человека, и в нескольких генетических исследованиях было выявлено, что он имеет другой полиморфизм у спортсменов мирового класса по сравнению с нормальными людьми. Одна форма, которая заставляет этот ген производить больше белка, обнаружена у спринтеров и связана с увеличением мощности; Другая форма, которая заставляет ген производить меньше белка, обнаружена у спортсменов, занимающихся выносливостью. [19] [20] Агенты для генного допинга могут быть созданы либо с полиморфизмом, либо для спортсменов, занимающихся выносливостью, с некоторой конструкцией ДНК, которая мешает экспрессии, например, небольшая интерферирующая РНК . [19]
Миостатин – это белок, ответственный за ингибирование дифференцировки и роста мышц . Удаление гена миостатина или иное ограничение его экспрессии приводит к увеличению размера и силы мышц. [6] Это было продемонстрировано на мышах, лишенных гена, которых назвали « мышами Шварценеггера ». [21] Люди, рожденные с дефектными генами, также могут служить «нокаут-моделями»; немецкий мальчик с мутацией обеих копий гена миостатина родился с хорошо развитой мускулатурой. [22] Ускоренный рост мышц продолжился после рождения, и в возрасте 4 лет мальчик мог поднимать тяжести до 3 кг. [6] В работе, опубликованной в 2009 году, ученые вводили фоллистатин с помощью генной терапии в квадрицепсы нечеловекообразных приматов, что приводит к локальному росту мышц, как у мышей. [6]
Эритропоэтин – это гликопротеин , который действует как гормон , контролирующий выработку эритроцитов. Спортсмены в течение многих лет вводили белок ЭПО в качестве вещества, повышающего спортивные результаты ( допинг крови ). Когда дополнительный ЭПО увеличивает выработку эритроцитов в кровообращении, это увеличивает количество кислорода, доступного мышцам, повышая выносливость спортсмена. [6] [23] Недавние исследования показывают, что возможно ввести животному еще один ген ЭПО, чтобы эндогенно увеличить выработку ЭПО . [22] Гены ЭПО были успешно вставлены мышам и обезьянам , и было обнаружено, что они повышают гематокрит у этих животных на целых 80 процентов. [22] Однако эндогенный и трансгенный ЭПО вызывал у некоторых животных аутоиммунные реакции в виде тяжелой анемии . [22]
Инсулиноподобный фактор роста 1 представляет собой белок, участвующий в выработке гормона роста . Введение IGF-1 мышам привело к большему росту мышц и более быстрой регенерации мышц и нервов. [19] [6] Если бы спортсмены использовали это, устойчивое производство IGF-1 могло бы вызвать болезни сердца и рак. [19]
Модулирование уровней белков, влияющих на психологию, также является потенциальной целью генного допинга; например, восприятие боли зависит от эндорфинов и энкефалинов , реакция на стресс зависит от BDNF , а увеличение синтеза моноаминов может улучшить настроение спортсменов. [19] Препроэнкефалин вводили мышам посредством генной терапии с использованием вируса простого герпеса с дефицитом репликации , поражающего нервы, с результатами, достаточно хорошими, чтобы оправдать фазу I клинических испытаний на людях с терминальной стадией рака и неконтролируемой болью. [6] Принятие такого подхода для спортсменов будет проблематичным, поскольку ослабление боли, вероятно, будет постоянным. [6]
VEGF был протестирован в клинических испытаниях на предмет увеличения кровотока и рассматривался как потенциальный агент генного допинга; однако долгосрочное наблюдение за участниками клинических испытаний показало плохие результаты. [6] То же самое относится и к фактору роста фибробластов . [6] Глюкагоноподобный пептид-1 увеличивает количество глюкозы в печени. Его вводили с помощью генной терапии в печень мышиных моделей диабета. Было показано, что он увеличивает глюконеогенез у спортсменов, что позволит получить больше энергии и снизить накопление молочной кислоты . [6]
Всемирное антидопинговое агентство ( ВАДА) является основной регулирующей организацией, занимающейся проблемой выявления генного допинга. [9] Организация исследует как прямые, так и косвенные методы тестирования. Непосредственное обнаружение использования генной терапии обычно требует открытия рекомбинантных белков или векторов вставки генов , тогда как большинство косвенных методов включают обследование спортсмена в попытке обнаружить изменения в организме или структурные различия между эндогенными и рекомбинантными белками. [6] [24] [25]
Косвенные методы по своей природе более субъективны, поскольку становится очень сложно определить, какие аномалии являются доказательством генного допинга, а какие просто естественными, хотя и необычными, биологическими свойствами. [6] Например, Ээро Мянтюранта , олимпийский лыжник , имел мутацию, которая заставила его организм производить аномально большое количество эритроцитов. Было бы очень сложно определить, был ли уровень эритроцитов Мянтюранта обусловлен врожденным генетическим преимуществом или искусственным. [26]
Идея обнаружения генного допинга возникла в 2004 году, когда ВАДА поместило генный допинг в запрещенный список и начало исследовать новый метод, позволяющий обнаруживать вставленные трансгены.
Первое поколение методов обнаружения генного допинга использовало ПЦР- тесты, нацеленные на последовательности трансгенов. Его можно получить из образца крови, который будет содержать эндогенную и трансгенную ДНК, поскольку небольшое количество трансгена попадет в кровоток. Его легко отличить от эндогенной ДНК, поскольку в нем отсутствуют интроны, поскольку трансген, скорее всего, будет использовать кДНК, полученную с помощью обратной транскриптазы из РНК, которая удалила свои интонации в результате сплайсинга РНК , оставив только экзон-экзонное соединение, включающее только кодирующие последовательности и некоторые важные последовательности, такие как промоторы, поскольку вирусные победители обладают ограниченной способностью. Следовательно, ПЦР может нацеливаться на эти экзон-экзонные соединения как на уникальную последовательность, которой нет в гДНК [27].
ПЦР имеет множество применений в области молекулярной биологии, включая анализ ДНК . Основная цель ПЦР — экспоненциальная амплификация и удвоение последовательностей ДНК.
При обнаружении допинга гена: если последовательность начала амплифицироваться, образуя экспоненциальный график, то тест положительный и указывает на присутствие гена в образце, полученном от этого человека. Но если последовательность не амплифицирована и получен линейный график, то тест считается отрицательным и целевая последовательность ДНК не присутствует в образце этого человека. [28]
Учитывая ограничения методов обнаружения первого поколения, было важно разработать новый метод, который преодолевает предыдущие неудачи с высокой точностью и может обнаруживать манипуляции с последовательностями ДНК, которые можно было бы избежать обнаружения методами ПЦР.
Решением стало использование метода секвенирования следующего поколения (NGS), который может определять порядок нуклеотидов во всем геноме или нацеливаться на соединения экзон-экзон в трансгене и сравнивать его с последовательностью эталонного гена. Этот метод очень точен, со временем становится все дешевле и открыл новую область науки, которая раньше была невозможна, например, секвенирование всего генома. [29]
Секвенирование ДНК было создано в 1970-х годах с помощью двумерной хроматографии и продолжало совершенствоваться до 2001 года, когда был завершен проект генома человека , который стоил около трех миллиардов долларов и требовал 15 лет для завершения секвенирования всего генома. Однако с учетом современных технологий секвенирования полногеномное секвенирование (WGS) занимает всего один день и стоит около тысячи долларов. Более того, разрабатывается новая технология секвенирования, которая будет стоить WGS всего 100 долларов. [30]
Существует множество методов NGS, которые используются при секвенировании ДНК, но наиболее часто используемый метод — метод, используемый Illumina [31].
Обзор 2016 года показал, что в литературе было выявлено около 120 полиморфизмов ДНК, связанных с некоторыми аспектами спортивных результатов: 77 — с выносливостью и 43 — с силой. 11 были воспроизведены в трех или более исследованиях, шесть были выявлены в исследованиях полногеномных ассоциаций , но 29 не были воспроизведены по крайней мере в одном исследовании. [20]
11 реплицированных маркеров были: [20]
Шестью маркерами GWAS были: [20]
Всемирное антидопинговое агентство (ВАДА) установило, что любая нетерапевтическая форма генетических манипуляций для улучшения спортивных результатов запрещена его кодексом. Существуют руководящие принципы, позволяющие определить, следует ли запрещать указанную технологию в спорте: если соблюдены два из трех условий, то технология запрещена в спорте (наносит вред здоровью, повышает результативность и/или противоречит «духу спорта»). . [32]
Кайзер и др. утверждают, что генный допинг может уравнять правила игры , если все спортсмены получат равный доступ. Критики утверждают, что любое терапевтическое вмешательство в нетерапевтических целях ставит под угрозу этические основы медицины и спорта. [33]
Высокие риски, связанные с генной терапией, могут быть перевешены потенциалом спасения жизней людей с заболеваниями: по словам Алена Фишера, который участвовал в клинических испытаниях генной терапии у детей с тяжелым комбинированным иммунодефицитом , «только умирающие люди будут иметь разумные основания для ее использования. Использование генной терапии для допинга неприемлемо с этической точки зрения и глупо с научной точки зрения». [34] Как видно из прошлых случаев, в том числе со стероидом тетрагидрогестриноном ( THG ), спортсмены могут решить включить рискованные генетические технологии в свои тренировочные режимы. [3]
Основная точка зрения заключается в том, что генный допинг опасен и неэтичен, как и любое применение терапевтического вмешательства в нетерапевтических или улучшающих целях, и что он ставит под угрозу этические основы медицины и дух спорта. [4] [35] [36] [7] [37] Другие, которые поддерживают улучшение человеческого потенциала на более широких основаниях, [38] или которые видят ложную дихотомию между «естественным» и «искусственным» или отрицание роли технологий. для улучшения спортивных результатов не противодействуйте и не поддерживайте генный допинг. [39]
атрибуция содержит текст из раздела «Генетическое улучшение человека» по состоянию на 17:03 26 октября 2020 г.