ДНК -полимераза является членом семейства ферментов , которые катализируют синтез молекул ДНК из нуклеозидтрифосфатов , молекулярных предшественников ДНК. Эти ферменты необходимы для репликации ДНК и обычно работают группами, создавая два идентичных дуплекса ДНК из одного исходного дуплекса ДНК. Во время этого процесса ДНК-полимераза «читает» существующие цепи ДНК, чтобы создать две новые цепи, соответствующие существующим. [1] [2] [3] [4] [5] [6] Эти ферменты катализируют химическую реакцию .
ДНК-полимераза добавляет нуклеотиды к трем штриховым (3') -концам цепи ДНК, по одному нуклеотиду за раз. Каждый раз , когда клетка делится , ДНК-полимеразы дублируют ДНК клетки, чтобы копию исходной молекулы ДНК можно было передать каждой дочерней клетке. Таким образом, генетическая информация передается из поколения в поколение.
Прежде чем начнется репликация, фермент, называемый хеликазой , раскручивает молекулу ДНК из ее плотно сплетенной формы, разрывая при этом водородные связи между нуклеотидными основаниями . Это открывает или «расстегивает» двухцепочечную ДНК, образуя две одиночные цепи ДНК, которые можно использовать в качестве шаблонов для репликации в вышеуказанной реакции.
В 1956 году Артур Корнберг и его коллеги обнаружили ДНК-полимеразу I (Pol I) в Escherichia coli . Они описали процесс репликации ДНК, при котором ДНК-полимераза копирует базовую последовательность цепи матрицы ДНК. Позднее в 1959 году за эту работу Корнберг был удостоен Нобелевской премии по физиологии и медицине . [7] ДНК-полимераза II была открыта Томасом Корнбергом (сыном Артура Корнберга ) и Малкольмом Э. Гефтером в 1970 году, что позволило дополнительно выяснить роль Pol I в репликации ДНК E. coli . [8] Еще три ДНК-полимеразы были обнаружены в E. coli , включая ДНК-полимеразу III (обнаруженную в 1970-х годах) и ДНК-полимеразы IV и V (открытую в 1999 году). [9]

Основная функция ДНК-полимеразы — синтез ДНК из дезоксирибонуклеотидов , строительных блоков ДНК. Копии ДНК создаются путем спаривания нуклеотидов с основаниями, присутствующими на каждой цепи исходной молекулы ДНК. Это спаривание всегда происходит в определенных комбинациях: цитозин вместе с гуанином и тимин вместе с аденином образуют две отдельные пары соответственно. Напротив, РНК-полимеразы синтезируют РНК из рибонуклеотидов либо из РНК, либо из ДНК. [ нужна цитата ]
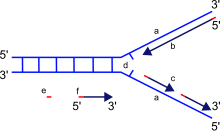
При синтезе новой ДНК ДНК-полимераза может добавлять свободные нуклеотиды только к 3'-концу вновь образующейся цепи. Это приводит к удлинению вновь образующейся цепи в направлении 5’–3’. [ нужна цитата ]
Важно отметить, что направленность вновь образующейся цепи (дочерней цепи) противоположна направлению движения ДНК-полимеразы вдоль матричной цепи. Поскольку ДНК-полимераза требует свободной 3'-ОН-группы для инициации синтеза, она может синтезировать только в одном направлении, удлиняя 3'-конец ранее существовавшей нуклеотидной цепи. Следовательно, ДНК-полимераза движется вдоль цепи матрицы в направлении 3'-5', а дочерняя цепь формируется в направлении 5'-3'. Это различие позволяет образовавшейся двухцепочечной ДНК состоять из двух нитей ДНК, антипараллельных друг другу. [ нужна цитата ]
Функция ДНК-полимеразы не совсем идеальна: фермент допускает примерно одну ошибку на каждый миллиард копируемых пар оснований. Исправление ошибок — свойство некоторых, но не всех ДНК-полимераз. Этот процесс исправляет ошибки во вновь синтезированной ДНК. Когда распознается неправильная пара оснований, ДНК-полимераза перемещается назад на одну пару оснований ДНК. 3'-5'- экзонуклеазная активность фермента позволяет удалить неправильную пару оснований (эта активность известна как корректура ). После удаления основания полимераза может повторно вставить правильное основание, и репликация может продолжиться вперед. Это сохраняет целостность исходной цепи ДНК, которая передается дочерним клеткам.
Верность очень важна при репликации ДНК. Несоответствия в спаривании оснований ДНК потенциально могут привести к дисфункции белков и раку. Многие ДНК-полимеразы содержат экзонуклеазный домен, который обнаруживает несовпадения пар оснований, а затем удаляет неправильный нуклеотид для замены правильным. [10] Форма и взаимодействие пары оснований Уотсона и Крика в первую очередь способствуют обнаружению или ошибке. Водородные связи играют ключевую роль в связывании и взаимодействии пар оснований. Считается, что потеря взаимодействия, которая происходит при несовпадении, вызывает сдвиг баланса связывания матрицы-праймера с полимеразы на экзонуклеазный домен. Кроме того, включение неправильного нуклеотида приводит к замедлению полимеризации ДНК. Эта задержка дает время для переключения ДНК с сайта полимеразы на сайт экзонуклеазы. Различные конформационные изменения и потеря взаимодействия происходят при разных несовпадениях. При несоответствии пурина и пиримидина происходит смещение пиримидина в сторону большой бороздки, а пурина - в сторону малой бороздки. Что касается формы связывающего кармана ДНК-полимеразы, между пурином и остатками в малой бороздке происходят стерические столкновения, а пиримидин теряет важные ван-дер-ваальсовые и электростатические взаимодействия. [11] Несовпадения пиримидин:пиримидин и пурин:пурин вызывают менее заметные изменения, поскольку основания смещаются в сторону большой бороздки и возникают меньшие стерические препятствия. Однако, хотя различные несоответствия приводят к различным стерическим свойствам, ДНК-полимераза все же способна обнаруживать и дифференцировать их столь единообразно и поддерживать точность репликации ДНК. [12] Полимеризация ДНК также имеет решающее значение для многих процессов мутагенеза и широко используется в биотехнологиях.
Известные ДНК-полимеразы имеют высококонсервативную структуру, а это означает, что их общие каталитические субъединицы очень мало различаются от вида к виду, независимо от структуры их доменов. Консервативные структуры обычно указывают на важные, незаменимые функции клетки, поддержание которых обеспечивает эволюционные преимущества. Форму можно описать как правую руку с большим пальцем, указательным пальцем и ладонью. Пальмовый домен, по-видимому, катализирует перенос фосфорильных групп в реакции переноса фосфорила. ДНК прикрепляется к ладони, когда фермент активен. Считается, что эта реакция катализируется по двухионному механизму. Функция пальцевого домена связывает нуклеозидтрифосфаты с основанием матрицы. Домен большого пальца играет потенциальную роль в процессивности, транслокации и позиционировании ДНК. [13]
Быстрый катализ ДНК-полимеразы обусловлен ее процессивным характером. Процессивность – характеристика ферментов, функционирующих на полимерных субстратах. В случае ДНК-полимеразы степень процессивности относится к среднему количеству нуклеотидов, добавляемых каждый раз, когда фермент связывает матрицу. В среднем ДНК-полимеразе требуется около одной секунды для обнаружения и связывания соединения праймер/матрица. После связывания непроцессивная ДНК-полимераза добавляет нуклеотиды со скоростью один нуклеотид в секунду. [14] : 207–208 Однако процессивные ДНК-полимеразы добавляют несколько нуклеотидов в секунду, резко увеличивая скорость синтеза ДНК. Степень процессивности прямо пропорциональна скорости синтеза ДНК. Скорость синтеза ДНК в живой клетке впервые была определена как скорость удлинения ДНК фага Т4 в инфицированной фагом E. coli . В период экспоненциального роста ДНК при 37°С скорость составляла 749 нуклеотидов в секунду. [15]
Способность ДНК-полимеразы скользить по матрице ДНК позволяет повысить процессивность. Процессивность репликационной вилки резко возрастает . Этому увеличению способствует ассоциация ДНК-полимеразы с белками, известная как скользящий зажим ДНК . Зажимы представляют собой несколько белковых субъединиц, связанных в форме кольца. Используя гидролиз АТФ, класс белков, известных как белки, загружающие скользящие зажимы, открывают кольцевую структуру скользящих зажимов ДНК, позволяя связываться с цепью ДНК и высвобождаться из нее. Белково-белковое взаимодействие с зажимом предотвращает диффузию ДНК-полимеразы из ДНК-матрицы, тем самым гарантируя, что фермент связывается с тем же соединением праймер/матрица и продолжает репликацию. [14] : 207–208 ДНК-полимераза изменяет конформацию, увеличивая сродство к зажиму, когда она связана с ним, и уменьшая сродство, когда она завершает репликацию участка ДНК, чтобы обеспечить освобождение от зажима. [ нужна цитата ]
Процессивность ДНК-полимеразы была изучена с помощью экспериментов с одиночными молекулами in vitro (а именно, с помощью оптических пинцетов и магнитных пинцетов ), которые выявили синергизм между ДНК-полимеразами и другими молекулами реплисомы ( геликазы и SSB ), а также с вилкой репликации ДНК. [16] Эти результаты привели к разработке синергетических кинетических моделей репликации ДНК, описывающих результирующее увеличение процессивности ДНК-полимеразы. [16]
На основании гомологии последовательностей ДНК-полимеразы можно разделить на семь различных семейств: A, B, C, D, X, Y и RT.
Некоторые вирусы также кодируют специальные ДНК-полимеразы, такие как ДНК-полимераза вируса гепатита В. Они могут избирательно реплицировать вирусную ДНК с помощью различных механизмов. Ретровирусы кодируют необычную ДНК-полимеразу, называемую обратной транскриптазой , которая представляет собой РНК-зависимую ДНК-полимеразу (RdDp). Он полимеризует ДНК из матрицы РНК .
Прокариотические полимеразы существуют в двух формах: кор-полимераза и голофермент. Core-полимераза синтезирует ДНК из матрицы ДНК, но она не может инициировать синтез самостоятельно или точно. Голофермент точно инициирует синтез.
Прокариотические полимеразы семейства А включают фермент ДНК-полимеразу I (Pol I), который кодируется геном polA и повсеместно распространен среди прокариот . Эта репарационная полимераза участвует в эксцизионной репарации, обладая как 3'-5'-, так и 5'-3'-экзонуклеазной активностью, а также процессингом фрагментов Оказаки, образующихся во время синтеза отстающей цепи. [21] Pol I является наиболее распространенной полимеразой, на которую приходится >95% полимеразной активности в E. coli ; тем не менее, было обнаружено, что в клетках отсутствует Pol I, что позволяет предположить, что активность Pol I может быть заменена другими четырьмя полимеразами. Pol I добавляет ~15-20 нуклеотидов в секунду, демонстрируя тем самым плохую процессивность. Вместо этого Pol I начинает добавлять нуклеотиды в месте соединения праймер:матрица РНК, известном как точка начала репликации (ori). Примерно на 400 п.н. ниже источника голофермент Pol III собирается и берет на себя репликацию с высокой процессивной скоростью и характером. [22]
Taq -полимераза — термостабильный фермент этого семейства, не обладающий способностью к корректуре. [23]
ДНК-полимераза II представляет собой полимеразу семейства B, кодируемую геном polB. Pol II обладает 3'-5'-экзонуклеазной активностью и участвует в репарации ДНК , перезапуске репликации в обход повреждений, а его присутствие в клетках может прыгать от ~ 30-50 копий на клетку до ~ 200-300 во время индукции SOS. Считается также, что Pol II является резервной копией Pol III, поскольку он может взаимодействовать с голоферментными белками и приобретать высокий уровень процессивности. Считается, что основная роль Pol II заключается в способности направлять активность полимеразы на репликационную вилку и помогать остановленному Pol III обходить терминальные несовпадения. [24]
ДНК-полимераза Pfu — термостабильный фермент этого семейства, обнаруженный у гипертермофильных архей Pyrococcus Furiosus . [25] Подробная классификация делит семейство B у архей на B1, B2, B3, в котором B2 представляет собой группу псевдоферментов . Pfu принадлежит к семейству B3. Другие PolB, обнаруженные у архей, входят в состав «Каспозонов», Cas1 -зависимых транспозонов. [26] Некоторые вирусы (включая ДНК-полимеразу Φ29 ) и митохондриальные плазмиды также несут polB. [27]
Холофермент ДНК-полимеразы III является основным ферментом, участвующим в репликации ДНК в E. coli , и принадлежит к полимеразам семейства C. Он состоит из трех узлов: ядра pol III, фактора процессивности скользящего зажима бета и комплекса зажима-нагрузки. Ядро состоит из трех субъединиц: α, концентратора полимеразной активности, ɛ, экзонуклеолитического корректора и θ, который может действовать как стабилизатор ɛ. Фактор процессивности бета-скользящего зажима также присутствует в двух экземплярах, по одному для каждого ядра, для создания зажима, который окружает ДНК, обеспечивая высокую процессивность. [28] Третья сборка представляет собой семисубъединичный (τ2γδδ ′ χψ) комплекс зажима-загрузчика.
В старом учебнике «модель тромбона» изображен комплекс элонгации с двумя эквивалентами основного фермента в каждой репликационной вилке (RF), по одному на каждую цепь, отстающему и ведущему. [24] Однако недавние данные исследований одиночных молекул указывают в среднем на три стехиометрических эквивалента основного фермента в каждом RF как для Pol III, так и для его аналога в B. subtilis, PolC. [29] Внутриклеточная флуоресцентная микроскопия показала, что синтез ведущей цепи не может быть полностью непрерывным, а Pol III* (т.е. субъединицы холофермента α, ε, τ, δ и χ без скользящего зажима β2) имеет высокую частоту диссоциация от активных РФ. [30] В этих исследованиях скорость оборота репликационной вилки составляла около 10 с для Pol III*, 47 с для скользящего зажима ß2 и 15 м для геликазы DnaB. Это предполагает, что хеликаза DnaB может оставаться стабильно связанной с RF и служить точкой зародышеобразования компетентного холофермента. Исследования одиночных молекул in vitro показали, что Pol III* имеет высокую скорость оборота RF при избытке, но остается стабильно связанным с репликационными вилками, когда концентрация ограничена. [30] Другое исследование одиночных молекул показало, что активность хеликазы DnaB и удлинение цепи могут происходить с развязанной стохастической кинетикой. [30]
В E. coli ДНК -полимераза IV (Pol IV) представляет собой склонную к ошибкам ДНК-полимеразу, участвующую в ненаправленном мутагенезе. [31] Pol IV представляет собой полимеразу семейства Y, экспрессируемую геном dinB , который включается посредством SOS-индукции, вызванной остановкой полимераз в репликационной вилке. Во время индукции SOS продукция Pol IV увеличивается в десять раз, и одной из функций в это время является вмешательство в процессивность голофермента Pol III. Это создает контрольную точку, останавливает репликацию и дает время на восстановление повреждений ДНК соответствующим путем восстановления. [32] Другая функция Pol IV заключается в осуществлении синтеза трансфузии на остановленной репликационной вилке, например, в обход аддуктов N2-дезоксигуанина с более высокой скоростью, чем при пересечении неповрежденной ДНК. Клетки, лишенные гена dinB , имеют более высокую скорость мутагенеза, вызванного агентами, повреждающими ДНК. [33]
ДНК-полимераза V (Pol V) представляет собой ДНК-полимеразу Y-семейства, которая участвует в SOS-ответе и механизмах репарации ДНК в синтезе транслейкоза . [34] Транскрипция Pol V через гены umuDC строго регулируется, чтобы производить только Pol V, когда в клетке присутствует поврежденная ДНК, вызывающая SOS-ответ. Остановка полимераз заставляет RecA связываться с оцДНК, что приводит к самоперевариванию белка LexA . Затем LexA теряет способность подавлять транскрипцию оперона umuDC. Тот же нуклеопротеин RecA-ssDNA посттрансляционно модифицирует белок UmuD в белок UmuD'. UmuD и UmuD' образуют гетеродимер, который взаимодействует с UmuC, который, в свою очередь, активирует каталитическую полимеразную активность umuC в отношении поврежденной ДНК. [35] В E. coli была предложена полимеразная модель «пояса с инструментами» для переключения pol III на pol IV в остановленной репликационной вилке, где обе полимеразы одновременно связываются с β-зажимом. [36] Однако участие более чем одной TLS-полимеразы, работающей последовательно, чтобы обойти повреждение, еще не было показано в E. coli . Более того, Pol IV может с высокой эффективностью катализировать как вставку, так и удлинение, тогда как pol V считается основной SOS-полимеразой TLS. Одним из примеров является обход внутрицепочечной сшивки гуанин-тимином, где на основе разницы в мутационных сигнатурах двух полимераз было показано, что pol IV и pol V конкурируют за TLS внутрицепочечной сшивки. [36]

В 1998 году семейство ДНК-полимераз D было обнаружено у Pyrococcus Furiosus и Methanococcus jannaschii . [38] Комплекс PolD представляет собой гетеродимер из двух цепей, каждая из которых кодируется DP1 (малая корректура) и DP2 (большая каталитическая). В отличие от других ДНК-полимераз, структура и механизм каталитического ядра DP2 напоминают таковые у многосубъединичных РНК-полимераз . Интерфейс DP1-DP2 напоминает интерфейс цинкового пальца эукариотической полимеразы класса B и ее небольшой субъединицы. [18] DP1, Mre11 -подобная экзонуклеаза, [39] вероятно является предшественником небольшой субъединицы Pol α и ε , обеспечивающей возможности корректуры, ныне утраченные у эукариот. [26] Его N-концевой домен HSH по структуре подобен белкам AAA , особенно субъединице δ Pol III и RuvB . [40] DP2 имеет домен класса II KH . [18] Pyrococcus abyssi polD более термостабилен и более точен, чем Taq- полимераза, но еще не поступил в продажу. [41] Было высказано предположение, что ДНК-полимераза семейства D была первой, развившейся в клеточных организмах, и что репликативная полимераза Последнего универсального клеточного предка (LUCA) принадлежала семейству D. [42]
Полимеразы семейства X содержат хорошо известную эукариотическую полимеразу pol β (бета) , а также другие эукариотические полимеразы, такие как Pol σ (сигма), Pol λ (лямбда) , Pol μ (mu) и терминальную дезоксинуклеотидилтрансферазу (TdT) . Полимеразы семейства X обнаружены в основном у позвоночных животных, а некоторые - у растений и грибов. Эти полимеразы имеют высококонсервативные области, которые включают два мотива спираль-шпилька-спираль, которые необходимы во взаимодействиях ДНК-полимеразы. Один мотив расположен в домене 8 кДа, который взаимодействует с нижележащей ДНК, и один мотив расположен в домене большого пальца, который взаимодействует с цепью праймера. Pol β, кодируемый геном POLB, необходим для репарации вырезаемых оснований с короткими участками , пути репарации ДНК, который необходим для восстановления алкилированных или окисленных оснований, а также абазиновых участков . Pol λ и Pol μ, кодируемые генами POLL и POLM соответственно, участвуют в негомологичном соединении концов — механизме воссоединения двухцепочечных разрывов ДНК, вызванных перекисью водорода и ионизирующим излучением соответственно. TdT экспрессируется только в лимфоидной ткани и добавляет «n нуклеотидов» к двухцепочечным разрывам, образующимся во время рекомбинации V(D)J , чтобы способствовать иммунологическому разнообразию. [43]
Pol α (альфа) , Pol δ (дельта) и Pol ε (эпсилон) являются членами полимераз семейства B и являются основными полимеразами, участвующими в репликации ядерной ДНК. Комплекс Pol α (комплекс pol α-ДНК-примазы) состоит из четырех субъединиц: каталитической субъединицы POLA1 , регуляторной субъединицы POLA2 , а также малой и большой субъединиц PRIM1 и PRIM2 соответственно. Как только примаза создала праймер для РНК, Pol α начинает репликацию, удлиняя праймер примерно на 20 нуклеотидов. [44] Благодаря своей высокой процессивности Pol δ берет на себя синтез ведущей и отстающей цепи от Pol α. [14] : 218–219 Pol δ экспрессируется генами POLD1 , создавая каталитическую субъединицу, POLD2 , POLD3 и POLD4 создают другие субъединицы, которые взаимодействуют с ядерным антигеном пролиферирующих клеток (PCNA), который представляет собой зажим ДНК , который позволяет Pol δ обладать процессивностью. [45] Pol ε кодируется генами POLE1 , каталитической субъединицей POLE2 и POLE3 . Сообщалось, что функция Pol ε заключается в удлинении ведущей цепи во время репликации, [46] [47], тогда как Pol δ в первую очередь реплицирует отстающую цепь; однако недавние данные показали, что Pol δ может также играть роль в репликации ведущей цепи ДНК. [48] С-концевая «полимеразная» область Pol ε, несмотря на то, что она не требуется для полимеразной активности, [49] считается важной для жизнеспособности клеток. Считается, что С-концевая область обеспечивает контрольную точку перед входом в анафазу, обеспечивает стабильность голофермента и добавляет к голоферменту белки, необходимые для инициации репликации. [50] Pol ε имеет более крупный «пальмовый» домен, который обеспечивает высокую процессивность независимо от PCNA. [49]
По сравнению с другими полимеразами семейства B, семейство экзонуклеаз DEDD, ответственное за корректуру, инактивировано в Pol α. [26] Pol ε уникален тем, что имеет два домена с цинковыми пальцами и неактивную копию полимеразы другого семейства B на С-конце. Наличие этого цинкового пальца имеет значение для происхождения эукариот, которые в данном случае помещаются в группу Асгарда с архейной полимеразой B3. [51]
Pol η (эта) , Pol ι (йота) и Pol κ (каппа) представляют собой ДНК-полимеразы семейства Y, участвующие в репарации ДНК путем трансляционного синтеза и кодируемые генами POLH, POLI и POLK соответственно. Члены семейства Y имеют пять общих мотивов, помогающих связывать субстрат и конец праймера, и все они включают типичные домены большого пальца правой руки, ладони и пальца с добавленными доменами, такими как мизинец (LF), домен, связанный с полимеразой (PAD) или запястье. Однако активный сайт у разных членов семьи различается из-за разных заживляемых повреждений. Полимеразы семейства Y представляют собой полимеразы низкой точности, но доказано, что они приносят больше пользы, чем вреда, поскольку мутации, влияющие на полимеразу, могут вызывать различные заболевания, такие как рак кожи и пигментная ксеродерма (XPS). О важности этих полимераз свидетельствует тот факт, что ген, кодирующий ДНК-полимеразу η, называется XPV, поскольку потеря этого гена приводит к заболеванию пигментной ксеродерма. Pol η особенно важен для обеспечения точного транслезного синтеза повреждений ДНК, возникающих в результате ультрафиолетового излучения . Функциональность Pol κ до конца не изучена, но исследователи нашли две вероятные функции. Считается, что Pol κ действует как удлинитель или вставка определенного основания при определенных повреждениях ДНК. Все три полимеразы синтеза трансформ, наряду с Rev1, рекрутируются в поврежденные очаги посредством остановленных репликативных ДНК-полимераз. Существует два пути восстановления повреждений, что позволяет исследователям прийти к выводу, что выбранный путь зависит от того, какая цепь содержит повреждение: ведущая или отстающая. [52]
Pol ζ, еще одна полимераза семейства B, состоит из двух субъединиц Rev3 , каталитической субъединицы, и Rev7 ( MAD2L2 ), которая увеличивает каталитическую функцию полимеразы и участвует в синтезе трансфункции. Pol ζ не обладает 3'-5'-экзонуклеазной активностью и уникален тем, что может удлинять праймеры с несоответствиями по концам. Rev1 имеет три представляющие интерес области в домене BRCT , убиквитин-связывающем домене и C-концевом домене и обладает способностью к трансферазе dCMP, которая добавляет дезоксицитидин-противоположные повреждения, которые останавливают репликативные полимеразы Pol δ и Pol ε. Эти остановившиеся полимеразы активируют убиквитиновые комплексы, которые, в свою очередь, диссоциируют репликативные полимеразы и рекрутируют Pol ζ и Rev1. Вместе Pol ζ и Rev1 добавляют дезоксицитидин, и Pol ζ выходит за пределы поражения. Посредством еще невыясненного процесса Pol ζ диссоциирует, а репликационные полимеразы повторно связываются и продолжают репликацию. Pol ζ и Rev1 не необходимы для репликации, но потеря гена REV3 у почкующихся дрожжей может вызвать повышенную чувствительность к агентам, повреждающим ДНК, из-за коллапса репликационных вилок, где репликация полимеразы остановилась. [53]
Теломераза — это рибонуклеопротеин , функция которого заключается в репликации концов линейных хромосом, поскольку нормальная ДНК-полимераза не может реплицировать концы или теломеры . Одноцепочечный 3'-выступ двухцепочечной хромосомы с последовательностью 5'-TTAGGG-3' рекрутирует теломеразу. Теломераза действует так же, как и другие ДНК-полимеразы, удлиняя 3'-конец, но, в отличие от других ДНК-полимераз, теломераза не требует матрицы. Субъединица TERT, пример обратной транскриптазы , использует субъединицу РНК для формирования соединения праймер-матрица, которое позволяет теломеразе удлинять 3'-конец концов хромосомы. Считается, что постепенное уменьшение размера теломер в результате множества репликаций в течение жизни связано с эффектами старения. [14] : 248–249.
Pol γ (гамма), Pol θ (тета) и Pol ν (nu) представляют собой полимеразы семейства A. Долгое время считалось , что Pol γ, кодируемая геном POLG , является единственной митохондриальной полимеразой. Однако недавние исследования показывают, что по крайней мере Pol β (бета) , полимераза семейства X, также присутствует в митохондриях. [54] [55] Любая мутация, которая приводит к ограничению или нефункционированию Pol γ, оказывает значительное влияние на мтДНК и является наиболее распространенной причиной аутосомно-наследственных митохондриальных нарушений. [56] Pol γ содержит С-концевой полимеразный домен и N-концевой 3'-5' экзонуклеазный домен, которые соединены через линкерную область, которая связывает вспомогательную субъединицу. Акцессорная субъединица связывает ДНК и необходима для процессивности Pol γ. Точечная мутация A467T в линкерной области ответственна за более трети всех митохондриальных нарушений, связанных с Pol γ. [57] Хотя многие гомологи Pol θ, кодируемые геном POLQ , обнаружены у эукариот, его функция до конца не изучена. Последовательность аминокислот на С-конце - это то, что классифицирует Pol θ как полимеразу семейства A, хотя частота ошибок для Pol θ более тесно связана с полимеразами семейства Y. Pol θ удлиняет несовпадающие концы праймера и может обходить абазические сайты путем добавления нуклеотида. Он также обладает дезоксирибофосфодиэстеразной (dRPase) активностью в полимеразном домене и может проявлять АТФазную активность в непосредственной близости от оцДНК. [58] Pol ν (nu) считается наименее эффективным из ферментов-полимераз. [59] Однако ДНК-полимераза nu играет активную роль в восстановлении гомологии во время клеточных ответов на сшивки, выполняя свою роль в комплексе с хеликазой . [59]
Растения используют две полимеразы семейства А для копирования как митохондриального, так и пластидного генома. Они больше похожи на бактериальный Pol I, чем на Pol γ млекопитающих. [60]
Ретровирусы кодируют необычную ДНК-полимеразу, называемую обратной транскриптазой , которая представляет собой РНК-зависимую ДНК-полимеразу (RdDp), которая синтезирует ДНК из матрицы РНК. Семейство обратных транскриптаз содержит как функциональность ДНК-полимеразы, так и функциональность РНКазы H, которая разрушает основания РНК, спаренные с ДНК. Примером ретровируса является ВИЧ . [14] Обратная транскриптаза обычно используется для амплификации РНК в исследовательских целях. Используя матрицу РНК, ПЦР может использовать обратную транскриптазу, создавая матрицу ДНК. Эту новую матрицу ДНК затем можно использовать для типичной ПЦР-амплификации. Таким образом, продуктами такого эксперимента являются амплифицированные продукты ПЦР из РНК. [9]
Каждая частица ретровируса ВИЧ содержит два генома РНК , но после заражения каждый вирус генерирует только один провирус . [61] После заражения обратная транскрипция сопровождается переключением матрицы между двумя копиями генома (рекомбинация выбора копии). [61] В каждом цикле репликации происходит от 5 до 14 событий рекомбинации на геном. [62] Переключение шаблонов (рекомбинация), по-видимому, необходимо для поддержания целостности генома и как механизм восстановления поврежденных геномов. [63] [61]
Бактериофаг (фаг) Т4 кодирует ДНК-полимеразу, которая катализирует синтез ДНК в направлении от 5' к 3'. [64] Фаговая полимераза также обладает экзонуклеазной активностью, которая действует в направлении от 3' к 5', [65] и эта активность используется при корректуре и редактировании вновь вставленных оснований. [66] Было обнаружено, что мутант фага с термочувствительной ДНК-полимеразой при выращивании при пермиссивных температурах подвергается рекомбинации с частотами, которые примерно в два раза выше, чем у фага дикого типа. [67]
Было высказано предположение, что мутационные изменения в ДНК-полимеразе фага могут стимулировать переключение цепи матрицы (рекомбинацию выбора копии) во время репликации . [67]