Сурьма — химический элемент ; он имеет символ Sb (от латинского stibium ) и атомный номер 51. Блестящий серый металлоид , встречается в природе главным образом в виде сульфидного минерала антимонита (Sb 2 S 3 ). Соединения сурьмы известны с древних времен и превращаются в порошок для использования в медицине и косметике, часто известный под арабским названием « коль» . [7] Самое раннее известное описание металлоида на Западе было написано в 1540 году Ванноччо Бирингуччо .
Китай является крупнейшим производителем сурьмы и ее соединений, причем большая часть продукции приходится на рудник Сикуаншань в провинции Хунань . Промышленные методы очистки сурьмы от антимонита — обжиг с последующим восстановлением углеродом или прямое восстановление антимонита железом.
Наибольшее применение металлическая сурьма находит в сплавах со свинцом и оловом , которые имеют улучшенные свойства для припоев , пуль и подшипников скольжения . Улучшает жесткость пластин из свинцового сплава в свинцово-кислотных аккумуляторах . Триоксид сурьмы является известной добавкой к галогенсодержащим антипиренам . Сурьма используется в качестве легирующей примеси в полупроводниковых приборах .


Сурьма является членом 15-й группы периодической таблицы, одним из элементов, называемых пниктогенами , и имеет электроотрицательность 2,05. В соответствии с периодическими тенденциями он более электроотрицательен, чем олово или висмут , и менее электроотрицательен, чем теллур или мышьяк . Сурьма стабильна на воздухе при комнатной температуре, но при нагревании реагирует с кислородом с образованием триоксида сурьмы Sb 2 O 3 . [8]
Сурьма представляет собой серебристый, блестящий серый металлоид с твердостью по шкале Мооса 3, который слишком мягок, чтобы оставлять следы на твердых предметах. Монеты из сурьмы были выпущены в китайской провинции Гуйчжоу в 1931 году; долговечность была плохой, и вскоре чеканка была прекращена. [9] Сурьма устойчива к воздействию кислот.
Единственный стабильный аллотроп сурьмы в стандартных условиях [10] — металлический, хрупкий , серебристо-белый и блестящий. Он кристаллизуется в тригональной ячейке, изоморфной висмуту и серому аллотропу мышьяка , и образуется при медленном охлаждении расплавленной сурьмы . Аморфная черная сурьма образуется при быстром охлаждении паров сурьмы и стабильна только в виде тонкой пленки (толщина в нанометрах); более толстые образцы самопроизвольно переходят в металлическую форму. [11] Он окисляется на воздухе и может самопроизвольно воспламениться. При 100 °С он постепенно переходит в стабильную форму. Предполагаемый желтый аллотроп сурьмы, полученный только путем окисления стибина (SbH 3 ) при -90 °C, также является нечистым и не является настоящим аллотропом; [12] [13] выше этой температуры и при окружающем освещении он превращается в более стабильный черный аллотроп. [14] [15] [16] Редкая взрывчатая форма сурьмы может быть образована в результате электролиза трихлорида сурьмы , но она всегда содержит значительное количество хлора и на самом деле не является аллотропом сурьмы. [12] При царапинах острым предметом происходит экзотермическая реакция и выделяются белые пары в виде металлической сурьмы; при растирании пестиком в ступке возникает сильная детонация.
Элементарная сурьма имеет слоистую структуру ( пространственная группа R 3 м № 166), слои которой состоят из сросшихся, гофрированных шестичленных колец. Ближайшие и следующие за ними соседи образуют неправильный октаэдрический комплекс, в котором три атома в каждом двойном слое немного ближе, чем три атома в следующем. Такая относительно плотная упаковка приводит к высокой плотности 6,697 г/см 3 , но слабая связь между слоями приводит к низкой твердости и хрупкости сурьмы. [8]
Сурьма имеет два стабильных изотопа : 121 Sb с естественным содержанием 57,36% и 123 Sb с естественным содержанием 42,64%. Он также имеет 35 радиоизотопов, из которых самый долгоживущий — 125 Sb с периодом полураспада 2,75 года. Кроме того, охарактеризовано 29 метастабильных состояний. Наиболее стабильным из них является 120m1 Sb с периодом полураспада 5,76 суток. Изотопы, которые легче стабильного 123 Sb, имеют тенденцию к распаду путем β + распада , а более тяжелые, за некоторыми исключениями, имеют тенденцию к распаду через β − распад . [17] Сурьма — самый легкий элемент, имеющий изотоп с альфа-ветвью распада, за исключением 8 Be и других легких нуклидов с бета-замедленным альфа-излучением. [18]

Содержание сурьмы в земной коре оценивается в 0,2 части на миллион , [19] что сопоставимо с таллием - 0,5 частей на миллион и серебром - 0,07 частей на миллион. Несмотря на то, что этот элемент не является распространенным, он содержится более чем в 100 минеральных видах. [20] Сурьма иногда встречается в природе (например, на Пике Сурьмы ), но чаще всего она встречается в сульфидном антимоните (Sb 2 S 3 ), который является преобладающим рудным минералом . [19]
Соединения сурьмы часто классифицируют по степени окисления: Sb(III) и Sb(V). Степень окисления +5 встречается чаще. [21]
Триоксид сурьмы образуется при сжигании сурьмы на воздухе. [22] В газовой фазе молекула соединения представляет собой Sb.
4О
6, но полимеризуется при конденсации. [8] Пятиокись сурьмы ( Sb
4О
10) могут образовываться только при окислении концентрированной азотной кислотой . [23] Сурьма также образует оксид смешанной валентности, четырехокись сурьмы ( Sb
2О
4), в котором присутствуют как Sb(III), так и Sb(V). [23] В отличие от оксидов фосфора и мышьяка , эти оксиды амфотерны , не образуют четко определенных оксокислот и реагируют с кислотами с образованием сурьмы.
Сурьмяная кислота Sb(OH)
3неизвестно, но сопряженное основание антимонит натрия ( [Na
3СбО
3]
4) образуется при сплавлении оксида натрия и Sb
4О
6. [24] Известны также антимониты переходных металлов. [25] : 122 Сурьма существует только в виде гидрата HSb(OH).
6, образуя соли в виде антимонатного аниона Sb(OH)−
6. При дегидратации раствора, содержащего этот анион, в осадке появляются смешанные оксиды. [25] : 143
Важнейшая сурьмяная руда — антимонит ( Sb
2С
3). Другие сульфидные минералы включают пираргирит ( Ag
3СбС
3), цинкенит , джемесонит и буланжерит . [ 26] Пентасульфид сурьмы нестехиометричен и содержит сурьму в степени окисления +3 и связях S–S. [27] Известно несколько тиоантимонидов, таких как [Sb
6С
10]2-
и [Сб
8С
13]2-
. [28]
Сурьма образует две серии галогенидов : SbX.
3и SbX
5. Тригалогениды SbF3, SbCl
3, СбБр
3и СбИ3Все молекулярные соединения имеют тригонально-пирамидальную молекулярную геометрию .
Трифторид SbF3получают по реакции Sb
2О
3с ВЧ : [29]
Он кислый по Льюису и легко принимает ионы фтора с образованием комплексных анионов SbF.−
4и СбФ2−
5. Расплавленный СбФ3является слабым электрическим проводником . Трихлорид SbCl
3получают растворением Sb
2С
3в соляной кислоте : [30]
Сульфиды мышьяка плохо подвергаются воздействию соляной кислоты, поэтому этот метод открывает путь к получению Sb, не содержащего мышьяк.

Пентагалогениды SbF5и SbCl
5имеют тригонально-бипирамидальную молекулярную геометрию в газовой фазе, но в жидкой фазе SbF5является полимерным , тогда как SbCl
5является мономерным. [31] СбФ5представляет собой мощную кислоту Льюиса, используемую для получения суперкислоты фторантимоновой кислоты («H 2 SbF 7 »).
Оксигалогениды более характерны для сурьмы, чем для мышьяка и фосфора. Триоксид сурьмы растворяется в концентрированной кислоте с образованием оксоантимонильных соединений, таких как SbOCl и (SbO).
2ТАК
4. [32]
Соединения этого класса обычно описываются как производные Sb 3- . Сурьма образует антимониды с металлами, такими как антимонид индия (InSb) и антимонид серебра ( Ag
3Сб ). [33] Антимониды щелочных металлов и цинка, такие как Na 3 Sb и Zn 3 Sb 2 , более реакционноспособны. Обработка этих антимонидов кислотой приводит к образованию крайне нестабильного газа стибина SbH .
3: [34]
Стибин также можно получить обработкой Sb.3+
соли с гидридными реагентами, такими как боргидрид натрия . Стибин самопроизвольно разлагается при комнатной температуре. Поскольку стибин имеет положительную теплоту образования , он термодинамически нестабилен , и поэтому сурьма не реагирует напрямую с водородом . [35]
Сурьмяорганические соединения обычно получают алкилированием галогенидов сурьмы реактивами Гриньяра . [36] Известно большое разнообразие соединений как с центрами Sb(III), так и с Sb(V), включая смешанные хлорорганические производные, анионы и катионы. Примеры включают трифенилстибин (Sb(C 6 H 5 ) 3 ) и пентафенилсурьму (Sb(C 6 H 5 ) 5 ). [37]

Сульфид сурьмы(III) , Sb 2 S 3 , был известен в додинастическом Египте как косметическое средство для глаз ( коль ) еще около 3100 г. до н. э. , когда была изобретена косметическая палитра . [38]
Артефакт, предположительно часть вазы, сделанной из сурьмы и датируемой примерно 3000 г. до н. э., был найден в Теллохе , Халдея (часть современного Ирака ), а медный предмет, покрытый сурьмой, датируемый между 2500 г. до н. э. найден в Египте . [14] Остин на лекции Герберта Гладстона в 1892 году отметила, что «в настоящее время мы знаем о сурьме только как о очень хрупком и кристаллическом металле, из которого вряд ли можно сделать полезную вазу, и поэтому эта замечательная «находка» (артефакт, упомянутый выше), должно быть, представляет собой утраченное искусство делать сурьму пластичной». [39]
Британский археолог Роджер Мури не был убежден, что артефакт действительно является вазой, отметив, что Селимханов после анализа объекта Телло (опубликованного в 1975 году) «попытался связать этот металл с закавказской природной сурьмой» (т.е. самородным металлом) и что « сурьмяные предметы из Закавказья — все мелкие личные украшения». [39] Это ослабляет доказательства утраченного искусства «придания сурьмы пластичности». [39]
Римский ученый Плиний Старший описал несколько способов получения сульфида сурьмы для медицинских целей в своем трактате «Естественная история» , около 77 года нашей эры. [40] Плиний Старший также проводил различие между «мужскими» и «женскими» формами сурьмы; мужская форма, вероятно, представляет собой сульфид, тогда как женская форма, более тяжелая, более тяжелая и менее рыхлая, предположительно представляет собой самородную металлическую сурьму. [41]
Греческий натуралист Педаний Диоскорид отмечал, что сульфид сурьмы можно поджарить, нагревая током воздуха. Считается, что при этом образовалась металлическая сурьма. [40]

Сурьма часто описывалась в алхимических рукописях, в том числе в «Summa Perfectionis » Псевдо-Гебера , написанном примерно в 14 веке. [42] Описание процедуры выделения сурьмы позже дано в книге 1540 года « De la pirotechnia» Ванноччо Бирингуччо , [43] предшествующей более известной книге 1556 года Агриколы « De re Metallica ». В этом контексте Агриколе часто ошибочно приписывают открытие металлической сурьмы. Книга Currus Triumphalis Antimonii («Триумфальная колесница сурьмы»), описывающая приготовление металлической сурьмы, была опубликована в Германии в 1604 году. Предполагалось, что она была написана бенедиктинским монахом , писавшим под именем Василий Валентин в 15 веке; если бы оно было подлинным, а это не так, оно было бы раньше Бирингуччо. [примечание 1] [15] [45] [46]
Металлическая сурьма была известна немецкому химику Андреасу Либавиусу в 1615 году, который получил ее путем добавления железа к расплавленной смеси сульфида сурьмы, соли и тартрата калия . В результате этой процедуры была получена сурьма с кристаллической или звездчатой поверхностью. [40]
С появлением вызовов теории флогистона было признано, что сурьма, как и другие металлы, является элементом, образующим сульфиды, оксиды и другие соединения. [40]
Первое открытие природной чистой сурьмы в земной коре было описано шведским ученым и местным горным инженером Антоном фон Свабом в 1783 году; Типовой образец был собран на серебряном руднике Сала в горнодобывающем районе Бергслаген в Сале , Вестманланд , Швеция. [47] [48]
Средневековая латинская форма, от которой современные языки и поздневизантийский греческий язык получили название сурьмы, — antimonium . [ нужна цитация ] Происхождение этого неясно; все предложения имеют некоторые трудности с формой или интерпретацией. Популярная этимология , от ἀντίμοναχός anti-monachos или французского antimoine , до сих пор имеет приверженцев; [ нужна цитация ] это означало бы «убийца монахов», и объясняется тем, что многие ранние алхимики были монахами, а сурьма была ядовитой. [49] Однако низкая токсичность сурьмы (см. ниже) делает это маловероятным. [ нужна ссылка ] [ оригинальное исследование? ]
Другая популярная этимология - гипотетическое греческое слово ἀντίμόνος antimonos , «против одиночества», объясняемое как «не найденное как металл» или «не найденное в чистом виде». [14] [50] Эдмунд Оскар фон Липпманн предположил гипотетическое греческое слово ανθήμόνιον anthemonion , которое означало бы «цветок», и приводит несколько примеров родственных греческих слов (но не того), которые описывают химическое или биологическое выцветание . [51]
Раннее использование сурьмы включает переводы Константином Африканским арабских медицинских трактатов в 1050–1100 годах. [51] Некоторые авторитетные источники считают, что сурьма — это искажение писцов какой-то арабской формы; Мейергоф выводит его от ithmid ; [52] другие возможности включают атимар , арабское название металлоида, и гипотетический ас-стимми , происходящий от греческого или параллельный ему. [53] [54]
Стандартный химический символ сурьмы (Sb) приписан Йонсу Якобу Берцелиусу , который получил аббревиатуру от сурьмы . [55]
Древние слова, обозначающие сурьму, в основном имеют основное значение « коль» , сульфид сурьмы. [ нужна цитата ]
Египтяне называли сурьму mśdmt [56] [57] или stm . [58]
Арабское слово, обозначающее вещество, в отличие от косметического средства, может звучать как إثمد ithmid, athmoud, othmod или uthmod . Литтре предполагает, что первая форма, которая является самой ранней, происходит от stimmida , винительного падежа от stimmi . [53] [59] Греческое слово στίμμι (стимми) используется аттическими трагическими поэтами V века до нашей эры и, возможно, является заимствованным словом из арабского или египетского stm . [58]
Извлечение сурьмы из руд зависит от качества и состава руды. Большая часть сурьмы добывается в виде сульфида; Руды более низкого качества концентрируются пенной флотацией , а руды более высокого качества нагреваются до 500–600 ° C - температуры, при которой антимонит плавится и отделяется от пустой породы. Сурьму можно выделить из сырого сульфида сурьмы восстановлением железным ломом: [60]
Сульфид преобразуется в оксид при обжиге. Продукт дополнительно очищают путем выпаривания летучего оксида сурьмы(III), который выделяют. [30] Этот сублимат часто используется непосредственно для основных целей, примесями являются мышьяк и сульфид. [61] [62] Сурьму выделяют из оксида карботермическим восстановлением: [60] [61]
Руды более низкого качества восстанавливаются в доменных печах , а руды более высокого качества – в отражательных печах . [60]
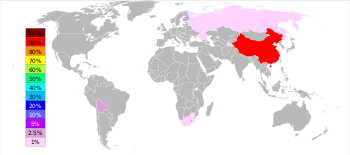

В 2022 году, по данным Геологической службы США , на долю Китая пришлось 54,5% общего производства сурьмы, на втором месте следовали Россия с 18,2% и Таджикистан с 15,5%. [63]
Ожидается, что в будущем производство сурьмы в Китае сократится, поскольку правительство закрывает шахты и металлургические заводы в рамках борьбы с загрязнением. В частности, в связи с вступлением в силу в январе 2015 года закона об охране окружающей среды [64] и вступлением в силу пересмотренных «Норматов выбросов загрязняющих веществ для олова, сурьмы и ртути» препятствия для экономического производства становятся выше.
Согласно отчету Roskill, зарегистрированное производство сурьмы в Китае сократилось и вряд ли увеличится в ближайшие годы. В Китае уже около десяти лет не разрабатываются значительные месторождения сурьмы, а оставшиеся экономические запасы быстро истощаются. [65]
Для регионов-импортеров сурьмы, таких как Европа и США, сурьма считается важнейшим минералом для промышленного производства, которое находится под угрозой нарушения цепочки поставок. Поскольку мировое производство поступает в основном из Китая (74%), Таджикистана (8%) и России (4%), эти источники имеют решающее значение для поставок. [66] [67]
Примерно 48% сурьмы расходуется в антипиренах , 33% в свинцово-кислотных аккумуляторах и 8% в пластмассах. [60]
Сурьма в основном используется в качестве триоксида для огнезащитных составов , всегда в сочетании с галогенированными антипиренами, за исключением галогенсодержащих полимеров. Огнезамедляющий эффект триоксида сурьмы обусловлен образованием галогенированных соединений сурьмы, [72] которые реагируют с атомами водорода, а также, вероятно, с атомами кислорода и радикалами ОН, подавляя таким образом огонь. [73] Рынки этих огнезащитных материалов включают детскую одежду, игрушки, чехлы для самолетов и автомобильных сидений. Их также добавляют в полиэфирные смолы в композитах из стекловолокна для таких изделий, как крышки двигателей легких самолетов. Смола горит при наличии внешнего пламени, но гаснет, когда внешнее пламя удаляется. [30] [74]
Сурьма образует очень полезный сплав со свинцом , повышая его твердость и механическую прочность. В большинстве случаев применения свинца в качестве легирующего металла используются различные количества сурьмы. В свинцово-кислотных аккумуляторах это дополнение улучшает прочность пластин и зарядные характеристики. [30] [75] На парусных лодках свинцовые кили используются для обеспечения восстанавливающего момента в диапазоне от 600 фунтов до более 200 тонн для крупнейших парусных суперяхт; Для повышения твердости и прочности свинцового киля сурьму смешивают со свинцом в количестве от 2 до 5% по объему. Сурьма используется в антифрикционных сплавах (таких как баббитовый металл ), [76] в пулях и свинцовой дроби , оболочке электрических кабелей , печатном металле (например, для линотипных печатных машин [77] ), припое (некоторые « бессвинцовые » припои содержат 5% Sb), [78] в олове , [79] и в затвердевающих сплавах с низким содержанием олова при изготовлении органных труб .

Три других приложения потребляют почти все остальные мировые ресурсы. [60] Одним из применений является стабилизатор и катализатор для производства полиэтилентерефталата . [60] Другой вариант — в качестве осветляющего агента для удаления микроскопических пузырьков в стекле , в основном для экранов телевизоров [80] — ионы сурьмы взаимодействуют с кислородом, подавляя склонность последнего к образованию пузырьков. [81] Третье применение — пигменты. [60]
В 1990-х годах сурьма все чаще использовалась в полупроводниках в качестве легирующей примеси в кремниевых пластинах n-типа [82] для диодов , инфракрасных детекторов и устройств на эффекте Холла . В 1950-х годах эмиттеры и коллекторы транзисторов с переходом из сплава npn были легированы крошечными шариками из сплава свинца и сурьмы. [83] Антимонид индия (InSb) используется в качестве материала для детекторов среднего инфракрасного диапазона . [84] [85] [86]
В биологии и медицине сурьма имеет мало применений. Препараты, содержащие сурьму, известные как препараты сурьмы , используются в качестве рвотного средства . [87] Соединения сурьмы используются в качестве противопротозойных препаратов. Антимонилтартрат калия , или рвотный камень, когда-то использовался в качестве противошистосомального препарата с 1919 года. Впоследствии он был заменен празиквантелом . [88] Сурьма и ее соединения используются в нескольких ветеринарных препаратах, таких как антиомалин и тиомалат лития-сурьмы, в качестве кондиционера для кожи жвачных животных . [89] Сурьма оказывает питательное или кондиционирующее действие на ороговевшие ткани животных.
Препараты на основе сурьмы, такие как сурьма меглюмина , также считаются препаратами выбора для лечения лейшманиоза у домашних животных . Помимо низких терапевтических показателей , препараты имеют минимальное проникновение в костный мозг , где обитают некоторые амастиготы Leishmania , и вылечить заболевание, особенно висцеральную форму, очень сложно. [90] Элементарная сурьма в виде таблетки сурьмы когда-то использовалась в качестве лекарства. Он может быть повторно использован другими после проглатывания и выведения. [91]
Сульфид сурьмы(III) используется в головках некоторых безопасных спичек . [92] [93] Сульфиды сурьмы помогают стабилизировать коэффициент трения в материалах автомобильных тормозных колодок. [94] Сурьма используется в пулях, трассерах пуль, [95] красках, изделиях из стекла и в качестве глушителя в эмали . Сурьма-124 используется вместе с бериллием в источниках нейтронов ; Гамма -лучи, испускаемые сурьмой-124, инициируют фотораспад бериллия . [96] [97] Испускаемые нейтроны имеют среднюю энергию 24 кэВ. [98] Природная сурьма используется в пусковых источниках нейтронов .
Исторически порошок, полученный из измельченной сурьмы ( коль ), наносили на глаза с помощью металлического стержня и слюны, что, по мнению древних, помогало в лечении глазных инфекций. [99] Такая практика до сих пор наблюдается в Йемене и других мусульманских странах. [100]
Сурьма и многие ее соединения токсичны , а последствия отравления сурьмой аналогичны отравлению мышьяком . Токсичность сурьмы намного ниже, чем у мышьяка; это может быть вызвано значительными различиями в поглощении, метаболизме и выведении мышьяка и сурьмы. Поглощение сурьмы(III) или сурьмы(V) в желудочно-кишечном тракте составляет не более 20%. Сурьма(V) количественно не восстанавливается в сурьме(III) в клетке (на самом деле сурьма(III) вместо этого окисляется до сурьмы(V) [101] ).
Поскольку метилирования сурьмы не происходит, основным путем элиминации является выведение сурьмы(V) с мочой. [102] Как и мышьяк, наиболее серьезным последствием острого отравления сурьмой является кардиотоксичность и возникающий в результате миокардит , однако он также может проявляться как синдром Адамса-Стокса , которого нет у мышьяка. Сообщалось о случаях интоксикации сурьмой, эквивалентной 90 мг тартрата калия сурьмы, растворенного в эмали, с кратковременными эффектами. Сообщалось, что отравление 6 г тартрата сурьмы и калия привело к смерти через три дня. [103]
Вдыхание пыли сурьмы вредно и в некоторых случаях может привести к летальному исходу; в малых дозах сурьма вызывает головные боли , головокружение и депрессию . Большие дозы, такие как длительный контакт с кожей, могут вызвать дерматит или повредить почки и печень, вызывая сильную и частую рвоту , приводящую к смерти через несколько дней. [104]
Сурьма несовместима с сильными окислителями , сильными кислотами , галогеновыми кислотами , хлором и фтором . Его следует хранить вдали от источников тепла. [105]
Сурьма выщелачивается из бутылок из полиэтилентерефталата (ПЭТ) в жидкости. [106] Хотя уровни, наблюдаемые для бутилированной воды , ниже нормативов для питьевой воды , [107] концентраты фруктовых соков (для которых не установлены нормативы), производимые в Великобритании, содержат до 44,7 мкг/л сурьмы, что значительно превышает нормы ЕС. пределы для водопроводной воды – 5 мкг/л. [108] Руководящие принципы таковы:
Допустимая суточная доза (TDI), предложенная ВОЗ, составляет 6 мкг сурьмы на килограмм массы тела. [109] Непосредственно опасное для жизни и здоровья значение (IDLH) для сурьмы составляет 50 мг/м 3 . [112]
Некоторые соединения сурьмы оказываются токсичными, особенно триоксид сурьмы и тартрат калия сурьмы. [113] Эффекты могут быть аналогичны отравлению мышьяком . [114] Профессиональное воздействие может вызвать раздражение дыхательных путей, пневмокониоз , пятна сурьмы на коже, желудочно-кишечные симптомы и сердечные аритмии. Кроме того, триоксид сурьмы потенциально канцерогенен для человека. [115]
Неблагоприятные последствия для здоровья наблюдались у людей и животных после ингаляционного, перорального или кожного воздействия сурьмы и соединений сурьмы. [113] Токсичность сурьмы обычно возникает либо из-за профессионального воздействия, во время терапии, либо из-за случайного проглатывания. Неясно, может ли сурьма проникать в организм через кожу. [113] Наличие низкого уровня сурьмы в слюне также может быть связано с кариесом . [116]