Бимолекулярное нуклеофильное замещение ( SN 2 ) — тип механизма реакции , распространенный в органической химии . В реакции S N 2 сильный нуклеофил образует новую связь с sp 3 -гибридизированным атомом углерода посредством атаки с обратной стороны, в то время как уходящая группа отрывается от реакционного центра согласованным (т.е. одновременным) образом.
Название SN 2 относится к символу Хьюза-Ингольда механизма: «SN » указывает, что реакция представляет собой нуклеофильное замещение , а «2» — что она протекает по бимолекулярному механизму, что означает, что в реакции участвуют обе реагирующие частицы. этап, определяющий скорость . Что отличает S N 2 от другого основного типа нуклеофильного замещения, реакции S N 1 , так это то, что замещение уходящей группы, которое является стадией, определяющей скорость, отделено от нуклеофильной атаки в S N 1.
Реакцию S N 2 можно рассматривать как аналог ассоциативного замещения в области неорганической химии .
Реакция чаще всего происходит в алифатическом углеродном центре sp 3 с прикрепленной к нему электроотрицательной стабильной уходящей группой, которая часто представляет собой галоген (часто обозначаемый X). Образование связи C–Nu в результате атаки нуклеофила (обозначенного Nu) происходит синхронно с разрывом связи C–X. Реакция протекает через переходное состояние, в котором реакционный центр является пятикоординированным и примерно sp 2 -гибридизированным.

Реакцию S N 2 можно рассматривать как взаимодействие ВЗМО-НСМО между нуклеофилом и субстратом. Реакция происходит только тогда, когда занятая неподеленная парная орбиталь нуклеофила отдает электроны незаполненной разрыхляющей орбитали σ* между центральным углеродом и уходящей группой . В ходе реакции в реакционном центре образуется ап-орбиталь в результате перехода от молекулярных орбиталей реагентов к молекулярным орбиталям продуктов. [1]

Чтобы достичь оптимального перекрытия орбиталей, нуклеофил атакует под углом 180 ° относительно уходящей группы, в результате чего уходящая группа отталкивается от противоположной стороны и образуется продукт с инверсией тетраэдрической геометрии в центральном атоме.
Например, синтез макроцидина А, грибкового метаболита , включает стадию внутримолекулярного замыкания кольца посредством реакции S N 2 с феноксидной группой в качестве нуклеофила и галогенидом в качестве уходящей группы, образуя простой эфир . [2] Подобные реакции с алкоксидом в качестве нуклеофила известны как синтез эфира Вильямсона .

Если субстрат, подвергающийся реакции S N 2 , имеет хиральный центр , то может произойти инверсия конфигурации ( стереохимии и оптической активности ); это называется инверсией Вальдена . Например, 1-бром-1-фторэтан может подвергаться нуклеофильной атаке с образованием 1-фторэтан-1-ола, при этом нуклеофилом является группа HO - . В этом случае, если реагент левовращающий, то и продукт будет правовращающим, и наоборот. [3]

Четыре фактора, влияющие на скорость реакции, в порядке убывания важности: [4] [5]
Субстрат играет наиболее важную роль в определении скорости реакции. Чтобы реакция S N 2 протекала быстрее, нуклеофил должен легко получить доступ к сигма-разрыхляющей орбитали между центральным углеродом и уходящей группой.
S N 2 происходит быстрее с субстратами, которые более стерически доступны по центральному углероду, т.е. с теми, которые не имеют поблизости столь стерически затрудняющих заместителей. Быстрее всего реагируют метил и первичные субстраты, за ними следуют вторичные субстраты. Третичные субстраты не реагируют по пути S N 2 , поскольку большее стерическое препятствие между нуклеофилом и близлежащими группами субстрата приводит к тому, что реакция S N 1 происходит первой.

Субстраты с соседними системами pi C=C могут благоприятствовать реакциям как S N 1, так и S N 2. В S N 1 аллильные и бензильные карбокатионы стабилизируются за счет делокализации положительного заряда. Однако в S N 2 сопряжение реакционного центра с соседней пи-системой стабилизирует переходное состояние. Поскольку электроноакцепторные группы дестабилизируют положительный заряд промежуточного карбокатиона, они благоприятствуют реакции S N 2 . Электронодонорные группы способствуют смещению уходящей группы и с большей вероятностью будут реагировать по пути S N 1. [1]

Как и субстрат, стерические препятствия влияют на силу нуклеофила. Например, метоксид-анион является одновременно сильным основанием и нуклеофилом, поскольку он является метил-нуклеофилом, и поэтому его реакция практически беспрепятственна . С другой стороны, трет -бутоксид является сильным основанием, но плохим нуклеофилом, поскольку три его метильные группы препятствуют его приближению к углероду. На силу нуклеофила также влияют заряд и электроотрицательность : нуклеофильность увеличивается с увеличением отрицательного заряда и уменьшением электроотрицательности. Например, OH – лучший нуклеофил, чем вода, а I – лучший нуклеофил, чем Br – (в полярных протонных растворителях). В полярном апротонном растворителе нуклеофильность увеличивается вверх по столбцу таблицы Менделеева, поскольку между растворителем и нуклеофилом нет водородной связи; в этом случае нуклеофильность отражает основность. Следовательно, я - будет более слабым нуклеофилом, чем Br - потому что это более слабое основание. Вердикт: сильный/анионный нуклеофил всегда отдает предпочтение типу нуклеофильного замещения S N 2.
Хорошие уходящие группы на субстрате приводят к более быстрым реакциям S N 2 . Хорошая уходящая группа должна быть способна стабилизировать электронную плотность , возникающую в результате разрыва связи с углеродным центром. Эта тенденция способности уходящей группы хорошо соответствует p K a кислоты, сопряженной с уходящей группой (p K aH ); чем ниже значение p K aH , тем быстрее вытесняется уходящая группа.
Уходящие группы, которые нейтральны, такие как вода , спирты ( R-OH ) и амины ( R-NH 2 ), являются хорошими примерами из-за их положительного заряда при связывании с углеродным центром до нуклеофильной атаки. Галогениды ( Cl- , Br- и I- ), за исключением F- ) , служат хорошими анионными уходящими группами, поскольку электроотрицательность стабилизирует дополнительную электронную плотность ; исключение фторида связано с его прочной связью с углеродом.
Реакционная способность спиртов по уходящей группе может быть увеличена с помощью сульфонатов , таких как тозилат ( -OTs ), трифлат ( -OTf ) и мезилат ( -OMs ) . К плохим уходящим группам относятся гидроксиды ( - OH ), алкоксиды ( - OR ) и амиды ( - NR 2 ).

Реакция Финкельштейна — это реакция S N 2, в которой уходящая группа также может действовать как нуклеофил. В этой реакции в субстрате атом галогена заменен на другой галоген. Поскольку отрицательный заряд более или менее стабилизирован на обоих галогенидах, реакция протекает в равновесии.

Растворитель влияет на скорость реакции, поскольку растворители могут окружать нуклеофил, а могут и не окружать его, тем самым препятствуя или не препятствуя его приближению к атому углерода. [6] Полярные апротонные растворители, такие как тетрагидрофуран , являются лучшими растворителями для этой реакции, чем полярные протонные растворители , поскольку полярные протонные растворители образуют водородную связь с нуклеофилом, препятствуя ему атаковать углерод уходящей группой. Полярный апротонный растворитель с низкой диэлектрической проницаемостью или затрудненным дипольным концом будет способствовать реакции нуклеофильного замещения по типу S N 2 . Примеры: диметилсульфоксид , диметилформамид , ацетон и т. д. Параллельно сольватация также оказывает значительное влияние на внутреннюю силу нуклеофила, при этом сильные взаимодействия между растворителем и нуклеофилом, обнаруженные для полярных протонных растворителей , приводят к образованию более слабого нуклеофила. Напротив, полярные апротонные растворители могут лишь слабо взаимодействовать с нуклеофилом и, следовательно, в меньшей степени способны снижать силу нуклеофила. [7] [8]
Скорость реакции S N 2 имеет второй порядок , поскольку определяющая скорость стадия зависит от концентрации нуклеофила [Nu - ], а также концентрации субстрата [RX]. [1]
В этом ключевое различие между механизмами S N 1 и S N 2. В реакции S N 1 нуклеофил атакует после завершения лимитирующей стадии, тогда как в реакции S N 2 нуклеофил отталкивает уходящую группу на лимитирующей стадии. Другими словами, скорость реакции S N 1 зависит только от концентрации субстрата, а скорость реакции S N 2 зависит от концентрации как субстрата, так и нуклеофила. [1]
Было показано [9] , что за исключением редких (но предсказуемых случаев) первичные и вторичные субстраты реагируют исключительно по механизму S N 2, а третичные субстраты - по реакции S N 1. Существуют два фактора, которые затрудняют определение механизма реакций нуклеофильного замещения при вторичном атоме углерода:
Примеры в учебниках, в которых вторичные субстраты действуют по механизму S N 1, неизменно включают использование бромида (или другого хорошего нуклеофила) в качестве уходящей группы, что запутало понимание реакций алкилнуклеофильного замещения у вторичных атомов углерода на 80 лет [3] . Работа Шлейера и соавторов с 2-адамантильной системой (SN 2 невозможна), [11] использование азида (отличный нуклеофил, но очень плохая уходящая группа) Вейнером и Снином, [ 12] [13] разработка сульфонатных уходящих групп (ненуклеофильных хороших уходящих групп) и демонстрация значительных экспериментальных проблем в первоначальном заявлении о механизме S N 1 в сольволизе оптически активного 2-бромоктана Хьюзом и др. [14] [3] убедительно продемонстрировали, что вторичные субстраты действуют исключительно (за исключением необычных, но предсказуемых случаев) по механизму S N 2 .
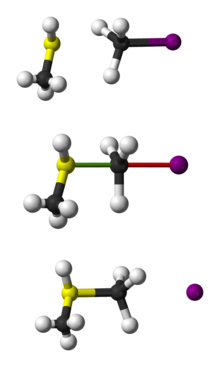
Обычной побочной реакцией, происходящей в реакциях S N 2 , является отщепление E2 : поступающий анион может действовать как основание, а не как нуклеофил, отрывая протон и приводя к образованию алкена . Этот путь предпочтителен для стерически затрудненных нуклеофилов. Реакции элиминирования обычно протекают при повышенных температурах [15] из-за увеличения энтропии . Этот эффект можно продемонстрировать в газофазной реакции между фенолятом и простым алкилбромидом , происходящей внутри масс-спектрометра : [16] [17]
В случае бромистого этила продуктом реакции является преимущественно продукт замещения. По мере увеличения стерических затруднений вокруг электрофильного центра, как и в случае с изобутилбромидом , замещение становится невыгодным, и преобладающей реакцией является элиминирование. Другими факторами, способствующими выбыванию, являются сила базы. С менее основным бензоатным субстратом изопропилбромид реагирует с 55%-ным замещением. В общем, реакции в газовой фазе и реакции в фазе раствора этого типа следуют одним и тем же тенденциям, хотя в первом случае эффекты растворителя устраняются.
Развитие, привлекшее внимание в 2008 году, касается обходного механизма S N 2 , наблюдаемого в газофазной реакции между ионами хлорида и йодидом метила с помощью специального метода, называемого визуализацией скрещенных молекулярных лучей . Когда ионы хлорида имеют достаточную скорость, первоначальное столкновение их с молекулой йодистого метила заставляет йодистый метил совершить один оборот, прежде чем сработает реальный механизм смещения S N 2 . [18] [19] [20]
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка )