Теория отталкивания электронных пар валентной оболочки ( VSEPR ) ( / ˈ v ɛ s p ər , v ə ˈ s ɛ p ər / VESP -ər , [1] : 410 və- SEP -ər [2] ) — модель , используемая в химии предсказывать геометрию отдельных молекул по числу электронных пар , окружающих их центральные атомы. [3] Ее также называют теорией Гиллеспи-Нихолма в честь двух ее главных разработчиков, Рональда Гиллеспи и Рональда Нихолма .
Предпосылка VSEPR заключается в том, что пары валентных электронов , окружающие атом, имеют тенденцию отталкивать друг друга. Чем больше отталкивание, тем выше энергия (менее стабильна) молекула. Следовательно, предсказанная VSEPR молекулярная геометрия молекулы — это такая геометрия молекулы, в которой это отталкивание минимально возможно. Гиллеспи подчеркивал, что электрон-электронное отталкивание, обусловленное принципом Паули , более важно в определении молекулярной геометрии, чем электростатическое отталкивание . [4]
Идея теории VSEPR основана на топологическом анализе электронной плотности молекул. К таким методам квантово-химической топологии (ККТ) относятся функция локализации электрона (ELF) и квантовая теория атомов в молекулах (AIM или QTAIM). [4] [5]
Идея корреляции между молекулярной геометрией и числом пар валентных электронов (как общих, так и неподеленных) была первоначально предложена в 1939 году Рютаро Цучида в Японии [6] и независимо представлена в Бейкеровской лекции в 1940 году Невилом Сиджвиком и Гербертом. Пауэлл из Оксфордского университета . [7] В 1957 году Рональд Гиллеспи и Рональд Сидней Нихолм из Университетского колледжа Лондона усовершенствовали эту концепцию до более подробной теории, позволяющей выбирать между различными альтернативными геометриями. [8] [9]
Теория VSEPR используется для предсказания расположения электронных пар вокруг центральных атомов в молекулах, особенно в простых и симметричных молекулах. Центральный атом определяется в этой теории как атом, который связан с двумя или более другими атомами, тогда как концевой атом связан только с одним другим атомом. [1] : 398 Например, в молекуле метилизоцианата (H 3 C-N=C=O) два углерода и один азот являются центральными атомами, а три водорода и один кислород - концевыми атомами. [1] : 416 Геометрия центральных атомов и их несвязывающих электронных пар, в свою очередь, определяет геометрию более крупной молекулы.
Число электронных пар в валентной оболочке центрального атома определяется после рисования структуры Льюиса молекулы и ее расширения, чтобы показать все связывающие группы и неподеленные пары электронов. [1] : 410–417 В теории VSEPR двойная или тройная связь рассматривается как одинарная связующая группа. [1] Сумма числа атомов, связанных с центральным атомом, и количества неподеленных пар , образованных его несвязывающими валентными электронами , известна как стерическое число центрального атома.
Предполагается, что электронные пары (или группы, если присутствуют кратные связи) лежат на поверхности сферы с центром в центральном атоме и стремятся занять положения, которые минимизируют их взаимное отталкивание за счет максимального увеличения расстояния между ними. [1] : 410–417 [10] Таким образом, количество электронных пар (или групп) определяет общую геометрию, которую они примут. Например, когда центральный атом окружают две пары электронов, их взаимное отталкивание минимально, когда они лежат на противоположных полюсах сферы. Следовательно, ожидается, что центральный атом примет линейную геометрию. Если центральный атом окружают 3 пары электронов, их отталкивание минимизируется за счет размещения их в вершинах равностороннего треугольника с центром на атоме. Следовательно, предсказанная геометрия является тригональной . Аналогично, для 4 пар электронов оптимальным расположением является тетраэдрическое . [1] : 410–417
В качестве инструмента прогнозирования геометрии, принятой с заданным количеством электронных пар, часто используемая физическая демонстрация принципа минимального отталкивания электронных пар использует надутые воздушные шары. В результате манипуляций воздушные шары приобретают небольшой поверхностный электростатический заряд, что приводит к принятию примерно той же геометрии, когда они связаны вместе на своих ножках, как и соответствующее количество электронных пар. Например, пять связанных вместе шариков принимают тригонально-бипирамидальную геометрию, как и пять связующих пар молекулы PCl 5 .

Стерическое число центрального атома в молекуле — это количество атомов, связанных с этим центральным атомом, называемое его координационным числом , плюс количество неподеленных пар валентных электронов на центральном атоме. [11] В молекуле SF 4 , например, центральный атом серы имеет четыре лиганда ; координационное число серы равно четырем. Помимо четырех лигандов, сера в этой молекуле имеет еще одну неподеленную пару. Таким образом, стерическое число равно 4 + 1 = 5.
Общая геометрия дополнительно уточняется за счет разделения связывающих и несвязывающих электронных пар. Связывающая пара электронов, образующая сигма-связь с соседним атомом, находится дальше от центрального атома, чем несвязывающая (неподеленная) пара этого атома, которая удерживается близко к его положительно заряженному ядру. Таким образом, теория VSEPR считает, что отталкивание неподеленной пары больше, чем отталкивание связывающей пары. Таким образом, когда молекула имеет два взаимодействия с разной степенью отталкивания, теория VSEPR предсказывает структуру, в которой неподеленные пары занимают положения, которые позволяют им испытывать меньшее отталкивание. Отталкивания одинокая пара-неподеленная пара (lp-lp) считаются более сильными, чем отталкивания одинокая пара-связывающая пара (lp-bp), которые, в свою очередь, считаются более сильными, чем отталкивания связывающая пара-связывающая пара (bp-bp), различия, которые затем определяют решения относительно общей геометрии, когда возможны 2 или более неэквивалентных позиций. [1] : 410–417 Например, когда 5 пар валентных электронов окружают центральный атом, они принимают тригонально-бипирамидальную молекулярную геометрию с двумя коллинеарными осевыми положениями и тремя экваториальными положениями. Электронная пара в аксиальном положении имеет трех близких экваториальных соседей, находящихся всего на расстоянии 90°, и четвертого, намного дальше, на расстоянии 180°, в то время как экваториальная электронная пара имеет только две соседние пары на расстоянии 90° и две на расстоянии 120°. Отталкивание от ближайших соседей под углом 90° более важно, так что осевые положения испытывают большее отталкивание, чем экваториальные; следовательно, когда есть неподеленные пары, они имеют тенденцию занимать экваториальные положения, как показано на диаграммах следующего раздела для стерического номера пять. [10]
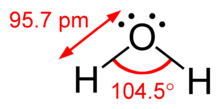
Разницу между неподеленными парами и связующими парами также можно использовать для объяснения отклонений от идеализированной геометрии. Например, молекула H 2 O имеет в своей валентной оболочке четыре пары электронов: две неподеленные пары и две пары связей. Четыре пары электронов разбросаны так, что они направлены примерно к вершинам тетраэдра. Однако валентный угол между двумя связями O–H составляет всего 104,5 °, а не 109,5 °, как в правильном тетраэдре, поскольку две неподеленные пары (чьи оболочки плотности или вероятности лежат ближе к ядру кислорода) оказывают большее взаимное отталкивание. чем две пары облигаций. [1] : 410–417 [10]
Связь более высокого порядка также оказывает большее отталкивание, поскольку вносят свой вклад электроны пи-связи . [10] Например, в изобутилене (H 3 C) 2 C=CH 2 угол H 3 C-C=C (124°) больше, чем угол H 3 C-C-CH 3 (111,5°). Однако в карбонат- ионе CO2−
3, все три связи C-O эквивалентны с углами 120 ° из-за резонанса .
«Метод AXE» подсчета электронов обычно используется при применении теории VSEPR. Электронные пары вокруг центрального атома представлены формулой AX n E m , где A представляет центральный атом и всегда имеет подразумеваемый нижний индекс. Каждый X представляет собой лиганд (атом, связанный с A). Каждый E представляет собой неподеленную пару электронов центрального атома. [1] : 410–417 Общее количество X и E известно как стерическое число. Например, в молекуле AX 3 E 2 атом A имеет стерическое число 5.
Когда атомы заместителя (X) не все одинаковы, геометрия все еще приблизительно верна, но валентные углы могут немного отличаться от тех, где все внешние атомы одинаковы. Например, атомы углерода двойной связи в алкенах, таких как C 2 H 4 , имеют вид AX 3 E 0 , но не все валентные углы составляют точно 120°. Аналогично SOCl 2 представляет собой AX 3 E 1 , но поскольку заместители X не идентичны, углы X-A-X не все равны.
На основании стерического числа и распределения X и E теория VSEPR делает предсказания в следующих таблицах.
Для элементов основной группы существуют стереохимически активные неподеленные пары E , число которых может варьироваться от 0 до 3. Обратите внимание, что геометрия названа только в соответствии с положениями атомов, а не расположением электронов. Например, описание AX 2 E 1 как изогнутой молекулы означает, что три атома AX 2 не расположены на одной прямой, хотя неподеленная пара помогает определить геометрию.
Неподеленные пары атомов переходных металлов обычно стереохимически неактивны, а это означает, что их присутствие не меняет геометрию молекулы. Например, все гексааквокомплексы M(H 2 O) 6 являются октаэдрическими для M = V 3+ , Mn 3+ , Co 3+ , Ni 2+ и Zn 2+ , несмотря на то, что электронные конфигурации центрального металла ионы d 2 , d 4 , d 6 , d 8 и d 10 соответственно. [13] : 542 Модель Кеперта игнорирует все неподеленные пары атомов переходных металлов, так что геометрия вокруг всех таких атомов соответствует геометрии VSEPR для AX n с 0 неподеленными парами E. [15] [13] : 542 Это часто пишется ML n , где M = металл и L = лиганд. Модель Кеперта предсказывает следующую геометрию для координационных чисел от 2 до 9:
Молекула метана (CH 4 ) тетраэдрическая, поскольку имеет четыре пары электронов. Четыре атома водорода расположены в вершинах тетраэдра , а валентный угол составляет cos -1 (- 1 ⁄ 3 ) ≈ 109°28′. [16] [17] Это называется молекулой типа AX 4 . Как упоминалось выше, A представляет собой центральный атом, а X представляет собой внешний атом. [1] : 410–417
Молекула аммиака (NH 3 ) имеет три пары электронов, участвующих в связывании, но на атоме азота имеется неподеленная пара электронов. [1] : 392–393 Он не связан с другим атомом; однако он влияет на общую форму посредством отталкивания. Как и в случае с метаном, описанным выше, существует четыре области электронной плотности. Следовательно, общая ориентация областей электронной плотности тетраэдрическая. С другой стороны, внешних атомов всего три. Ее называют молекулой типа AX 3 E, потому что неподеленная пара представлена буквой E. [1] : 410–417. По определению, форма или геометрия молекулы описывает только геометрическое расположение атомных ядер, которое является тригональным. пирамидальная для NH 3 . [1] : 410–417
Возможны стерические числа 7 и выше, но они встречаются реже. Стерическое число 7 встречается в гептафториде йода (IF 7 ); базовая геометрия для стерического числа 7 — пятиугольная бипирамида. [10] Наиболее распространенной геометрией для стерического числа 8 является квадратная антипризматическая геометрия. [18] : 1165 Примеры включают октацианомолибдат ( Mo(CN)4−
8) и октафторцирконат ( ZrF4−
8) анионы. [18] : 1165 Нонагидридорренат-ион ( ReH2−
9) в нонагидридоренате калия представляет собой редкий пример соединения со стерическим числом 9, имеющего трехглавую тригонально-призматическую геометрию. [13] : 254 [18]
Стерические числа больше 9 очень редки, и неясно, какая геометрия обычно предпочтительнее. [19] Возможными геометриями для стерических чисел 10, 11, 12 или 14 являются двуглавый квадратный антипризматический (или двуглавый додекадельтаэдр ), октадекаэдр , икосаэдр и двуглавый шестиугольный антипризматический соответственно. Соединений с таким высоким стерическим числом, включающих монодентатные лиганды, не существует, а соединения, включающие мультидентатные лиганды, часто можно анализировать более просто как комплексы с более низкими стерическими числами, когда некоторые полидентатные лиганды рассматриваются как единое целое. [18] : 1165, 1721 г.
Существуют группы соединений, в которых VSEPR не может предсказать правильную геометрию.
Было рассчитано, что формы более тяжелых аналогов алкинов элемента 14-й группы (RM≡MR, где M = Si, Ge, Sn или Pb) изогнуты. [20] [21] [22]
Одним из примеров геометрии AX 2 E 2 является молекулярный оксид лития Li 2 O, линейная, а не изогнутая структура, которая объясняется тем, что его связи являются по существу ионными и что приводит к сильному отталкиванию лития-лития. [23] Другим примером является O(SiH 3 ) 2 с углом Si-O-Si 144,1°, что сравнимо с углами в Cl 2 O (110,9°), (CH 3 ) 2 O (111,7°) и N(CH 3 ) 3 (110,9°). [24] Гиллеспи и Робинсон рационализируют валентный угол Si-O-Si на основе наблюдаемой способности неподеленной пары лиганда наиболее сильно отталкивать другие электронные пары, когда электроотрицательность лиганда больше или равна электроотрицательности центрального атома. [24] В O(SiH 3 ) 2 центральный атом более электроотрицательен, а неподеленные пары менее локализованы и менее отталкивающи. Больший валентный угол Si-O-Si является результатом этого, а также сильного отталкивания лиганд-лиганд со стороны относительно большого лиганда -SiH 3 . [24] Берфорд и др. показали с помощью рентгеновских дифракционных исследований, что Cl 3 Al-O-PCl 3 имеет линейный валентный угол Al-O-P и, следовательно, не является молекулой VSEPR. [ нужна цитата ]

Некоторые молекулы AX 6 E 1 , например гексафторид ксенона (XeF 6 ) и анионы Te(IV) и Bi(III), TeCl2−
6, ТеБр2−
6, БиСл3−
6, БиБр3−
6и БИИ3−
6, представляют собой октаэдрические, а не пятиугольные пирамиды, и неподеленная пара не влияет на геометрию в той степени, которую предсказывает VSEPR. [25] Аналогично октафтороксенат-ион ( XeF2−
8) в октафтороксенате(VI) нитрозония [13] : 498 [26] [27] представляет собой квадратную антипризму с минимальной дисторсией, несмотря на наличие неподеленной пары. Одно из объяснений состоит в том, что стерическое скучивание лигандов практически не оставляет места для несвязывающей неподеленной пары; [24] Еще одним объяснением является эффект инертной пары . [13] : 214
Модель Кеперта предсказывает, что молекулы переходного металла ML 4 имеют тетраэдрическую форму и не может объяснить образование плоских квадратных комплексов. [13] : 542 Большинство таких комплексов имеют конфигурацию ad 8 , как и тетрахлорплатинат ( PtCl2−
4) ион. Объяснение формы плоских квадратных комплексов связано с электронными эффектами и требует использования теории кристаллического поля . [13] : 562–4

Некоторые комплексы переходных металлов с низким числом d-электронов имеют необычную геометрию, которую можно объяснить связующим взаимодействием d-подоболочки. [28] Гиллеспи обнаружил, что это взаимодействие создает пары связей, которые также занимают соответствующие антиподальные точки (лиганды противоположны) сферы. [29] [4] Это явление представляет собой электронный эффект, возникающий в результате двухдольной формы лежащих в основе sd x гибридных орбиталей . [30] [31] Отталкивание этих связывающих пар приводит к различному набору форм.
Газофазные структуры трехатомных галогенидов более тяжелых членов группы 2 (т.е. галогениды кальция, стронция и бария, MX 2 ) не являются линейными, как предполагалось, а изогнуты (приблизительные углы X–M–X: CaF 2 , 145°, SrF 2 , 120°, BaF 2 , 108°, SrCl 2 , 130°, BaCl 2 , 115°, BaBr 2 , 115°, BaI 2 , 105°). [35] Гиллеспи предположил , что это также вызвано связывающим взаимодействием лигандов с подоболочкой d атома металла, что влияет, таким образом, на молекулярную геометрию. [24] [36]
Предполагается, что релятивистские эффекты на электронных орбиталях сверхтяжелых элементов будут влиять на молекулярную геометрию некоторых соединений. Например, электроны 6d 5/2 в нихонии играют неожиданно сильную роль в связывании, поэтому NhF 3 должен принять Т-образную геометрию, а не тригональную плоскую геометрию, как у его более легкого родственника BF 3 . [37] Напротив, согласно прогнозам, дополнительная стабильность 7p 1/2 электронов в теннессине делает TsF 3 тригонально-планарным, в отличие от Т-образной геометрии, наблюдаемой для IF 3 и предсказанной для At F 3 ; [38] аналогично, Og F 4 должен иметь тетраэдрическую геометрию, в то время как XeF 4 имеет плоскую квадратную геометрию, и Rn F 4 , по прогнозам, будет иметь такую же геометрию. [39]
Теорию VSEPR можно распространить на молекулы с нечетным числом электронов, рассматривая неспаренный электрон как «полуэлектронную пару» — например, Гиллеспи и Найхолм [8] : 364–365 предположили, что уменьшение валентного угла в серия НЕТ+
2(180°), НЕТ 2 (134°), НЕТ−
2(115 °) указывает на то, что данный набор пар связывающих электронов оказывает более слабое отталкивание на один несвязывающий электрон, чем на пару несвязывающих электронов. По сути, они рассматривали диоксид азота как молекулу AX 2 E 0,5 с промежуточной геометрией между NO и NO.+
2и нет−
2. Точно так же диоксид хлора (ClO 2 ) представляет собой молекулу AX 2 E 1,5 с промежуточной геометрией между ClO+
2и ClO−
2. [ нужна цитата ]
Наконец, прогнозируется, что метильный радикал (CH 3 ) будет тригонально-пирамидальным, как и метиловый анион ( CH−
3), но с большим валентным углом (как в тригональном плоском метил-катионе ( CH+
3)). Однако в этом случае предсказание VSEPR не совсем верно, поскольку CH 3 на самом деле является плоским, хотя его искажение до пирамидальной геометрии требует очень мало энергии. [40]
основанный на систематическом количественном применении общих представлений об отталкивании электронных пар.