Фосфорорганическая химия — научное исследование синтеза и свойств фосфорорганических соединений — органических соединений , содержащих фосфор . [1] Они используются в основном для борьбы с вредителями в качестве альтернативы хлорированным углеводородам , которые сохраняются в окружающей среде. Некоторые фосфорорганические соединения являются высокоэффективными инсектицидами , хотя некоторые из них чрезвычайно токсичны для человека, в том числе зарин и нервно-паралитические вещества VX . [2]
Фосфор, как и азот , находится в 15-й группе периодической таблицы, поэтому соединения фосфора и соединения азота имеют много схожих свойств. [3] [4] [5] Определение фосфорорганических соединений варьируется, что может привести к путанице. В промышленной химии и химии окружающей среды фосфорорганические соединения должны содержать только органический заместитель , но не обязательно иметь прямую связь фосфор-углерод (PC). [ нужна цитация ] Таким образом, большая часть пестицидов (например, малатион ) часто включается в этот класс соединений.
Фосфор может принимать различные степени окисления , и обычно фосфорорганические соединения классифицируются на основе того, что они являются производными фосфора (V) и фосфора (III), которые являются преобладающими классами соединений. В описательной, но редко используемой номенклатуре соединения фосфора идентифицируются по их координационному числу σ и валентности λ . В этой системе фосфин представляет собой соединение σ 3 λ 3 .
Эфиры фосфорной кислоты имеют общую структуру P(=O)(OR) 3 с особенностью P(V). Такие вещества имеют технологическое значение как антипирены и пластификаторы . Не имея связи P-C, эти соединения в техническом смысле являются не фосфорорганическими соединениями, а эфирами фосфорной кислоты. В природе встречается множество производных, например фосфатидилхолин . Эфиры фосфорной кислоты синтезируют алкоголизом оксихлорида фосфора. Известно множество смешанных производных амидо-алкоксо, одним из важных с медицинской точки зрения примером является противораковый препарат циклофосфамид . Также к производным, содержащим тиофосфорильную группу (P=S), относится пестицид малатион . Органофосфаты, получаемые в больших масштабах, представляют собой дитиофосфаты цинка в качестве присадок к моторному маслу. Несколько миллионов килограммов этого координационного комплекса ежегодно образуется при реакции пентасульфида фосфора со спиртами. [6]

В окружающей среде эти соединения расщепляются посредством гидролиза , в конечном итоге образуя фосфат и органический спирт или амин, из которого они получены.
Фосфонаты представляют собой сложные эфиры фосфоновой кислоты и имеют общую формулу RP(=O)(OR') 2 . Фосфонаты имеют множество технических применений, наиболее известным из которых является глифосат , более известный как Раундап. Это производное глицина с формулой (HO) 2 P(O)CH 2 NHCH 2 CO 2 H является одним из наиболее широко используемых гербицидов. Бисфосфонаты представляют собой класс препаратов для лечения остеопороза . Газ нервно-паралитического действия зарин , содержащий связи C–P и F–P, представляет собой фосфонат.
Фосфинаты содержат две связи P–C общей формулы R 2 P(=O)(OR'). Коммерчески значимым представителем является гербицид глюфосинат . Подобно упомянутому выше глифосату, он имеет структуру CH 3 P(O)(OH)CH 2 CH 2 CH(NH 2 )CO 2 H.
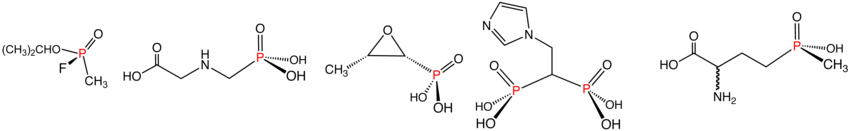
Реакция Михаэлиса -Арбузова является основным методом синтеза этих соединений. Например, диметилметилфосфонат (см. рисунок выше) возникает в результате перегруппировки триметилфосфита , катализируемой йодистым метилом . В реакции Хорнера-Уодсворта-Эммонса и омологации Сейферта-Гилберта фосфонаты используются в реакциях с карбонильными соединениями. Реакция Кабачника-Филдса — метод получения аминофосфонатов. Эти соединения содержат очень инертную связь между фосфором и углеродом. Следовательно, они гидролизуются с образованием производных фосфоновой и фосфиновой кислоты, но не с образованием фосфата.
Оксиды фосфина (обозначение σ 4 λ 5 ) имеют общую структуру R 3 P=O с формальной степенью окисления V. Оксиды фосфина образуют водородные связи и поэтому некоторые из них растворимы в воде. Связь P=O очень полярна с дипольным моментом 4,51 Д для оксида трифенилфосфина .
К соединениям, родственным фосфиноксидам, относятся фосфинимиды (R 3 PNR') и родственные им халькогениды (R 3 PE, где E = S , Se , Te ). Эти соединения являются одними из наиболее термически стабильных фосфорорганических соединений.
Соединения формулы [PR 4 + ]X − включают фосфониевые соли . Эти виды представляют собой тетраэдрические соединения фосфора (V). С коммерческой точки зрения наиболее важным представителем является хлорид тетракис(гидроксиметил)фосфония , [P(CH 2 OH) 4 ]Cl, который используется в качестве антипирена в текстиле . Ежегодно производится около 2 млн кг хлоридов и связанных с ними сульфатов. [6] Они образуются в результате реакции фосфина с формальдегидом в присутствии минеральной кислоты:
Путем алкилирования и арилирования органофосфинов можно получить различные фосфониевые соли :
Метилирование трифенилфосфина является первым этапом получения реактива Виттига.

Исходный фосфоран (σ 5 λ 5 ) представляет собой PH 5 , который неизвестен. [ нужна цитация ] Родственные соединения, содержащие как галогениды, так и органические заместители фосфора, довольно распространены. Те, что имеют пять органических заместителей, встречаются редко, хотя известен P(C 6 H 5 ) 5 , полученный из P(C 6 H 5 ) 4 + по реакции с фениллитием .
Илиды фосфора представляют собой ненасыщенные фосфораны, известные как реагенты Виттига , например CH 2 P(C 6 H 5 ) 3 . Эти соединения содержат тетраэдрический фосфор (V) и считаются родственниками оксидов фосфина. Они также получаются из солей фосфония, но путем депротонирования, а не алкилирования.
Фосфиты, иногда называемые фосфитными эфирами , имеют общую структуру P(OR) 3 со степенью окисления +3. Такие виды возникают в результате алкоголиза трихлорида фосфора:
Реакция общая, поэтому известно огромное количество таких видов. Фосфиты используются в реакции Перкова и реакции Михаэлиса-Арбузова . Они также служат лигандами в металлоорганической химии.
Промежуточными между фосфитами и фосфинами являются фосфониты (P(OR) 2 R') и фосфиниты (P(OR)R' 2 ). Такие соединения возникают в результате реакций алкоголиза соответствующих хлоридов фосфоновой и фосфиновой кислот ((PCl 2 R') и (PClR' 2 ) соответственно).
Исходным соединением фосфинов является PH 3 , который в США и Британском Содружестве называется фосфином , а в других странах – фосфаном. [7] Замена одного или нескольких водородных центров органическими заместителями (алкилом, арилом) дает PH 3-x R x , органофосфин, обычно называемый фосфинами.
С коммерческой точки зрения наиболее важным фосфином является трифенилфосфин , ежегодно производится несколько миллионов килограммов. Его получают реакцией хлорбензола , PCl 3 и натрия. [6] Фосфины более специализированной природы обычно получают другими способами. [8] Галогениды фосфора подвергаются нуклеофильному замещению металлоорганическими реагентами, такими как реактивы Гриньяра . Органофосфины являются нуклеофилами и лигандами . Двумя основными применениями являются реагенты в реакции Виттига и поддержка фосфиновых лигандов в гомогенном катализе .
Об их нуклеофильности свидетельствует их реакция с алкилгалогенидами с образованием фосфониевых солей . Фосфины являются нуклеофильными катализаторами в органическом синтезе , например, в реакции Раухута-Кюрриера и реакции Бэйлиса-Хиллмана . Фосфины являются восстановителями , как показано в восстановлении Штаудингера для превращения органических азидов в амины и в реакции Мицунобу для превращения спиртов в сложные эфиры. В этих процессах фосфин окисляется до фосфора(V). Также было обнаружено, что фосфины восстанавливают активированные карбонильные группы, например, восстановление α-кетоэфира до α-гидроксиэфира. [9]
Соединения с кратными связями углерода и фосфора(III) называются фосфаалкенами (R 2 C=PR) и фосфаалкинами (RC≡P). По структуре, но не по реакционной способности они сходны с иминами (R 2 C=NR) и нитрилами (RC≡N) соответственно. В соединении фосфорина один атом углерода в бензоле заменен фосфором. Виды этого типа относительно редки, но по этой причине представляют интерес для исследователей. Общий метод синтеза фосфаалкенов заключается в 1,2-отщеплении подходящих предшественников, инициируемом термически или основанием, таким как DBU , DABCO или триэтиламин :
При термолизе Me 2 PH образуется CH 2 =PMe, нестабильная разновидность в конденсированной фазе.
Соединения, в которых фосфор существует в формальной степени окисления ниже III, встречаются редко, но примеры известны для каждого класса. Фосфорорганические(0) соединения спорно иллюстрируются аддуктами карбена, [P(NHC)] 2 , где NHC представляет собой N-гетероциклический карбен . [10] По формулам (RP) n и (R 2 P) 2 соответственно соединения фосфора(I) и (II) образуются восстановлением родственных фосфорорганических(III) хлоридов:
Дифосфены с формулой R 2 P 2 формально содержат двойные связи фосфор-фосфор. Эти виды фосфора (I) редки, но стабильны при условии, что органические заместители достаточно велики, чтобы предотвратить образование цепей . Известно множество соединений со смешанной валентностью , например каркас P 7 (CH 3 ) 3 .