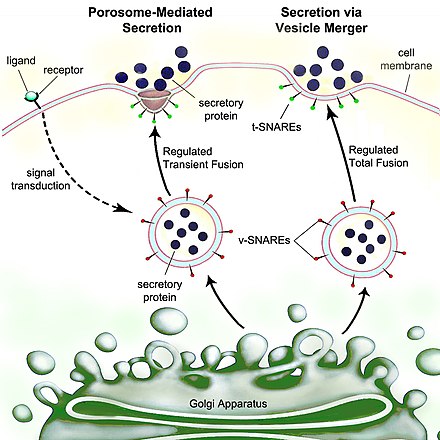
Секреция — это перемещение материала из одной точки в другую, например, химического вещества, секретируемого клеткой или железой . Напротив, экскреция — это удаление определенных веществ или продуктов жизнедеятельности из клетки или организма. Классический механизм клеточной секреции осуществляется через секреторные порталы плазматической мембраны, называемые поросомами . [1] Поросомы представляют собой постоянные липопротеиновые структуры чашеобразной формы , встроенные в клеточную мембрану, где секреторные пузырьки временно стыкуются и сливаются, высвобождая внутривезикулярное содержимое из клетки.
Секреция у видов бактерий означает транспорт или транслокацию эффекторных молекул. Например: белки , ферменты или токсины (такие как холерный токсин в патогенных бактериях, например, холерный вибрион ) изнутри ( цитоплазма или цитозоль ) бактериальной клетки к ее внешней поверхности. Секреция является очень важным механизмом функционирования и работы бактерий в их естественной окружающей среде для адаптации и выживания.

Эукариотические клетки , включая клетки человека , имеют высокоразвитый процесс секреции. Белки, предназначенные для внешнего воздействия, синтезируются рибосомами , прикрепленными к шероховатой эндоплазматической сети (ЭР). По мере синтеза эти белки перемещаются в просвет ЭР , где они гликозилируются и где молекулярные шапероны способствуют сворачиванию белка . Неправильно свернутые белки обычно идентифицируются здесь и ретротранслоцируются путем деградации, связанной с ER, в цитозоль , где они разрушаются протеасомой . Везикулы , содержащие правильно свернутые белки, затем попадают в аппарат Гольджи .
В аппарате Гольджи гликозилирование белков модифицируется и могут происходить дальнейшие посттрансляционные модификации , включая расщепление и функционализацию. Затем белки перемещаются в секреторные пузырьки, которые перемещаются по цитоскелету к краю клетки. В секреторных везикулах могут происходить дополнительные модификации (например, в секреторных везикулах инсулин отщепляется от проинсулина ).
В конце концов, происходит слияние пузырьков с клеточной мембраной в поросомах посредством процесса, называемого экзоцитозом , при котором их содержимое выбрасывается из окружающей среды клетки. [2]
Над этой последовательностью поддерживается строгий биохимический контроль за счет использования градиента pH : pH цитозоля составляет 7,4, pH ER составляет 7,0, а цис-гольджи имеет pH 6,5. Секреторные везикулы имеют pH от 5,0 до 6,0; некоторые секреторные везикулы превращаются в лизосомы , рН которых составляет 4,8.
Существует множество белков, таких как FGF1 (aFGF), FGF2 (bFGF), интерлейкин-1 (IL1) и т. д., которые не имеют сигнальной последовательности. Они не используют классический путь ER-Гольджи. Они секретируются различными неклассическими путями.
Описаны как минимум четыре неклассических (нетрадиционных) пути секреции белка. [3] К ним относятся:
Кроме того, белки могут высвобождаться из клеток при механическом или физиологическом повреждении [4] и через нелетальные, временные онкотические поры в плазматической мембране, индуцированные промыванием клеток бессывороточной средой или буферами. [5]
Многие типы клеток человека обладают способностью быть секреторными клетками. У них хорошо развита эндоплазматическая сеть и аппарат Гольджи , выполняющий эту функцию. К тканям , вырабатывающим секрет, относятся желудочно-кишечный тракт , выделяющий пищеварительные ферменты и желудочную кислоту , легкие , выделяющие поверхностно-активные вещества , и сальные железы , выделяющие кожное сало для смазывания кожи и волос. Мейбомиевы железы век выделяют мейбум для смазывания и защиты глаза.
Секреция не уникальна для эукариот — она также присутствует у бактерий и архей. Транспортеры типа АТФ-связывающей кассеты (ABC) являются общими для трех областей жизни. Некоторые секретируемые белки транслоцируются через цитоплазматическую мембрану с помощью транслокона SecYEG , одной из двух систем транслокации, которая требует присутствия N-концевого сигнального пептида на секретируемом белке. Другие транслоцируются через цитоплазматическую мембрану по пути транслокации двойного аргинина (Tat). Грамотрицательные бактерии имеют две мембраны, что топологически усложняет секрецию. У грамотрицательных бактерий существует по крайней мере шесть специализированных систем секреции. Многие секретируемые белки особенно важны в бактериальном патогенезе. [6]
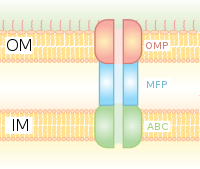
Секреция типа I представляет собой шаперон-зависимую систему секреции, использующую кластеры генов Hly и Tol. Процесс начинается с того, что лидерная последовательность секретируемого белка распознается HlyA и связывает HlyB на мембране. Эта сигнальная последовательность чрезвычайно специфична для транспортера ABC. Комплекс HlyAB стимулирует HlyD, который начинает раскручиваться и достигает внешней мембраны, где TolC распознает терминальную молекулу или сигнал на HlyD. HlyD рекрутирует TolC на внутреннюю мембрану, а HlyA выводится за пределы внешней мембраны через длинный туннельный белковый канал.
Система секреции I типа транспортирует различные молекулы: от ионов, лекарств до белков различного размера (20–900 кДа). Секретируемые молекулы различаются по размеру: от небольшого пептида колицина V Escherichia coli (10 кДа) до белка клеточной адгезии LapA Pseudomonas fluorescens массой 520 кДа. [7] Наиболее изученными являются токсины RTX и липазы. Секреция типа I также участвует в экспорте небелковых субстратов, таких как циклические β-глюканы и полисахариды.

Белки, секретируемые через систему типа II или главную терминальную ветвь общего секреторного пути, зависят от системы Sec или Tat для первоначального транспорта в периплазму . Оказавшись там, они проходят через внешнюю мембрану через мультимерный (12–14 субъединиц) комплекс порообразующих белков-секретинов. Помимо белка секретина, 10–15 других белков внутренней и внешней мембраны составляют полный аппарат секреции, функции многих из которых пока неизвестны. Грамотрицательные пили типа IV используют для своего биогенеза модифицированную версию системы типа II, и в некоторых случаях определенные белки являются общими для комплекса пилусов и системы типа II в пределах одного вида бактерий.
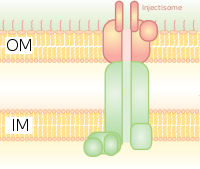
Он гомологичен базальному тельцу бактериальных жгутиков. Это похоже на молекулярный шприц, через который бактерия (например, некоторые виды сальмонелл , шигелл , иерсиний , вибрионов ) может вводить белки в эукариотические клетки. Низкая концентрация Ca 2+ в цитозоле открывает ворота, регулирующие ССТТ. Один из таких механизмов обнаружения низкой концентрации кальция был проиллюстрирован антигеном lcrV (Low Calcium Response), используемым Yersinia pestis , который используется для обнаружения низких концентраций кальция и вызывает прикрепление T3SS. Система Hrp в патогенах растений вводит в растения гарпины и эффекторные белки патогена посредством аналогичных механизмов. Эта система секреции была впервые обнаружена у Yersinia pestis и показала, что токсины могут быть инъецированы непосредственно из бактериальной цитоплазмы в цитоплазму клеток хозяина, а не просто секретироваться во внеклеточную среду. [8]
Он гомологичен механизму конъюгации бактерий — конъюгативным пилям . Он способен транспортировать как ДНК, так и белки. Он был обнаружен у Agrobacterium tumefaciens , которая использует эту систему для введения части Т-ДНК плазмиды Ti в растение-хозяин, что, в свою очередь, вызывает развитие пораженного участка в коронковый галл (опухоль). Helicobacter pylori использует систему секреции IV типа для доставки CagA в эпителиальные клетки желудка, что связано с канцерогенезом желудка. [9] Bordetella pertussis , возбудитель коклюша, секретирует коклюшный токсин частично через систему IV типа. Legionella pneumophila , возбудитель легионеллеза (болезни легионеров), использует систему секреции типа IVB, известную как система ICM/dot ( внутриклеточное размножение / дефект в генах , пересылающих органеллы ) , для перемещения многочисленных эффекторных белков . в своего эукариотического хозяина. [10] Прототипом системы секреции типа IVA является комплекс VirB Agrobacterium tumefaciens . [11]
Белки этого семейства являются компонентами системы секреции IV типа. Они опосредуют внутриклеточный перенос макромолекул посредством механизма , родственного механизму бактериальной конъюгации . [12] [13]
Система секреции типа IV (T4SS) представляет собой общий механизм, с помощью которого бактериальные клетки секретируют или поглощают макромолекулы. Их точный механизм остается неизвестным. ССТ4 кодируется грамотрицательными конъюгативными элементами бактерий . T4SS представляют собой комплексы, охватывающие клеточную оболочку, или, другими словами, 11–13 основных белков, образующих канал, по которому ДНК и белки могут перемещаться из цитоплазмы клетки-донора в цитоплазму клетки-реципиента. T4SS также секретирует белки факторов вирулентности непосредственно в клетки-хозяева, а также поглощает ДНК из среды во время естественной трансформации . [14]
Как показано на рисунке выше, TraC, в частности, состоит из трехспирального пучка и рыхлого шаровидного придатка. [13]
T4SS имеет два эффекторных белка: во-первых, ATS-1, который обозначает транслоцируемый Anaplasma субстрат 1, и, во-вторых, AnkA , который обозначает белок A, содержащий домен анкириновых повторов. Кроме того, связывающими белками T4SS являются VirD4, которые связываются с VirE2. [15]
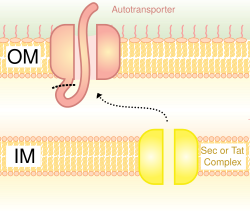
Секреция типа V , также называемая системой аутотранспортера, [16] предполагает использование системы Sec для пересечения внутренней мембраны. Белки, использующие этот путь, обладают способностью образовывать бета-цилиндр со своим С-концом, который встраивается во внешнюю мембрану, позволяя остальной части пептида (домену-пассажиру) достигать внешней части клетки. Часто аутотранспортеры расщепляются, оставляя домен бета-бочонка на внешней мембране и освобождая пассажирский домен. Некоторые исследователи полагают, что остатки автотранспортеров дали начало поринам , которые образуют аналогичные структуры бета-бочонка. [ нужна цитация ] Типичным примером автотранспортера, который использует эту систему секреции, являются тримерные автотранспортеры-адгезины . [17]
Системы секреции типа VI были первоначально идентифицированы в 2006 году группой Джона Мекаланоса из Гарвардской медицинской школы (Бостон, США) у двух бактериальных патогенов, Vibrio cholerae и Pseudomonas aeruginosa . [18] [19] Они были выявлены, когда мутации в генах Hcp и VrgG у холерного вибриона привели к снижению вирулентности и патогенности. С тех пор системы секреции типа VI были обнаружены в четверти всех геномов протеобактерий, включая патогены животных, растений, человека, а также почвенных, экологических или морских бактерий. [20] [21] В то время как большинство ранних исследований секреции типа VI были сосредоточены на ее роли в патогенезе высших организмов, более поздние исследования показали более широкую физиологическую роль в защите от простых эукариотических хищников и ее роль в межбактериальных взаимодействиях. [22] [23] Кластеры генов системы секреции типа VI содержат от 15 до более чем 20 генов, два из которых, Hcp и VgrG, как было показано, являются практически универсально секретируемыми субстратами системы. Структурный анализ этих и других белков в этой системе имеет поразительное сходство с хвостовым шипом фага Т4, и считается, что активность системы функционально напоминает фаговую инфекцию. [24]
Помимо использования перечисленных выше мультибелковых комплексов, грамотрицательные бактерии обладают еще одним способом высвобождения материала: образованием пузырьков наружной мембраны бактерий . [25] Части внешней мембраны отщипываются, образуя наноразмерные сферические структуры, состоящие из богатого липополисахаридами липидного бислоя, содержащего периплазматические материалы, и используются для перемещения мембранных везикул с целью манипулирования окружающей средой или проникновения на границу раздела хозяин-патоген . Было обнаружено, что везикулы ряда видов бактерий содержат факторы вирулентности, некоторые обладают иммуномодулирующим действием, а некоторые могут напрямую прикрепляться к клеткам-хозяевам и отравлять их. Было продемонстрировано, что высвобождение везикул является общей реакцией на стрессовые условия, процесс загрузки белков-грузов, по-видимому, является избирательным. [26]
У некоторых видов Staphylococcus и Streptococcus дополнительная секреторная система обеспечивает экспорт высокоповторяющихся адгезионных гликопротеинов.
[27]