
Гетерогенный катализ — это катализ , при котором фаза катализаторов отличается от фазы реагентов или продуктов . [1] Этот процесс отличается от гомогенного катализа , где реагенты, продукты и катализатор существуют в одной фазе. Фаза различает не только твердые , жидкие и газовые компоненты, но и несмешивающиеся смеси (например, нефть и вода ) или везде, где присутствует граница раздела.
Гетерогенный катализ обычно включает твердофазные катализаторы и газофазные реагенты. [2] В этом случае на поверхности катализатора происходит цикл молекулярной адсорбции, реакции и десорбции. Термодинамика, массоперенос и теплоперенос влияют на скорость (кинетику) реакции .
Гетерогенный катализ очень важен, поскольку он обеспечивает более быстрое, крупномасштабное производство и селективное образование продуктов. [3] Примерно 35% мирового ВВП зависит от катализа. [4] Производство 90% химикатов (по объему) осуществляется с помощью твердых катализаторов. [2] Химическая и энергетическая промышленность в значительной степени полагаются на гетерогенный катализ. Например, процесс Габера-Боша использует катализаторы на основе металлов при синтезе аммиака , важного компонента удобрений; В 2016 году было произведено 144 млн тонн аммиака. [5]
Адсорбция является важным этапом гетерогенного катализа. Адсорбция — это процесс, посредством которого молекула газовой фазы (или раствора) (адсорбат) связывается с поверхностными атомами твердого (или жидкого) вещества (адсорбент). Обратной стороной адсорбции является десорбция , отщепление адсорбата от адсорбента. В реакции, протекающей при гетерогенном катализе, катализатором является адсорбент, а реагентами – адсорбат.
Выделяют два типа адсорбции: физисорбция , слабосвязанная адсорбция, и хемосорбция , сильносвязанная адсорбция. Многие процессы гетерогенного катализа лежат между двумя крайностями. Модель Леннарда -Джонса обеспечивает базовую основу для прогнозирования молекулярных взаимодействий как функции разделения атомов. [6]
При физической адсорбции молекула притягивается к поверхностным атомам за счет сил Ван-дер-Ваальса . К ним относятся диполь-дипольные взаимодействия, индуцированные дипольные взаимодействия и дисперсионные силы Лондона. Отметим, что между адсорбатом и адсорбентом не образуется химических связей и их электронные состояния остаются относительно невозмущенными. Типичные энергии физисорбции составляют от 3 до 10 ккал/моль. [2] В гетерогенном катализе, когда молекула реагента физически адсорбируется на катализаторе, обычно говорят, что она находится в состоянии предшественника, промежуточном энергетическом состоянии перед хемосорбцией, более прочно связанной адсорбцией. [6] Из состояния-предшественника молекула может подвергаться хемосорбции, десорбции или миграции по поверхности. [7] Природа состояния-предшественника может влиять на кинетику реакции. [7]
Когда молекула приближается достаточно близко к поверхностным атомам, так что их электронные облака перекрываются, может произойти хемосорбция. При хемосорбции адсорбат и адсорбент разделяют электроны, что означает образование химических связей . Типичная энергия хемосорбции находится в диапазоне от 20 до 100 ккал/моль. [2] Два случая хемосорбции:

Большинство реакций на поверхности металлов происходят путем распространения цепи , при котором каталитические промежуточные продукты циклически производятся и расходуются. [8] Для A + B → C можно описать два основных механизма поверхностных реакций. [2]
Большинство гетерогенно катализируемых реакций описывается моделью Ленгмюра – Хиншелвуда. [9]
При гетерогенном катализе реагенты диффундируют из объемной жидкой фазы и адсорбируются на поверхности катализатора. Центр адсорбции не всегда является активным центром катализатора, поэтому молекулы реагента должны мигрировать по поверхности к активному центру. В активном центре молекулы реагентов будут реагировать с образованием молекул(ы) продукта, следуя по более энергетически легкому пути через каталитические промежуточные продукты (см. рисунок справа). Молекулы продукта затем десорбируются с поверхности и диффундируют. Сам катализатор остается неповрежденным и может свободно участвовать в дальнейших реакциях. Явления переноса, такие как тепло- и массоперенос, также играют роль в наблюдаемой скорости реакции.
Катализаторы не активны по отношению к реагентам по всей своей поверхности; только определенные места обладают каталитической активностью, называемые активными центрами . Площадь поверхности твердого катализатора оказывает сильное влияние на количество доступных активных центров. В промышленной практике твердые катализаторы часто бывают пористыми, чтобы максимизировать площадь поверхности, обычно достигая 50–400 м 2 /г. [2] Некоторые мезопористые силикаты , такие как MCM-41, имеют площадь поверхности более 1000 м 2 /г. [10] Пористые материалы экономически эффективны благодаря их высокому соотношению площади поверхности к массе и повышенной каталитической активности.
Во многих случаях твердый катализатор диспергируют на материале носителя для увеличения площади поверхности (распределения числа активных центров) и обеспечения стабильности. [2] Обычно носители катализатора представляют собой инертные материалы с высокой температурой плавления, но они также могут сами быть каталитическими. Большинство носителей катализатора являются пористыми (часто на основе углерода, кремнезема, цеолита или оксида алюминия) [4] и выбираются из-за высокого отношения площади поверхности к массе. Для данной реакции необходимо выбирать пористые подложки так, чтобы реагенты и продукты могли входить в материал и выходить из него.
Часто вещества намеренно добавляют в реакционное сырье или на катализатор, чтобы повлиять на каталитическую активность, селективность и/или стабильность. Эти соединения называются промоторами. Например, оксид алюминия (Al 2 O 3 ) добавляется во время синтеза аммиака для обеспечения большей стабильности за счет замедления процессов спекания на Fe-катализаторе. [2]
Принцип Сабатье можно считать одним из краеугольных камней современной теории катализа. [11] Принцип Сабатье гласит, что взаимодействие поверхность-адсорбаты должно быть оптимальным: не слишком слабым, чтобы быть инертным по отношению к реагентам, и не слишком сильным, чтобы отравить поверхность и избежать десорбции продуктов. [12] Утверждение о том, что взаимодействие поверхность-адсорбат должно быть оптимальным, является качественным. Обычно количество адсорбатов и переходных состояний, связанных с химической реакцией, велико, поэтому оптимум приходится искать в многомерном пространстве. Проектирование катализатора в таком многомерном пространстве не является вычислительно жизнеспособной задачей. Кроме того, такой процесс оптимизации будет далеко не интуитивным. Масштабные соотношения используются для уменьшения размерности пространства конструкции катализатора. [13] Такие отношения представляют собой корреляции между энергиями связи адсорбатов (или между энергиями связи адсорбатов и переходными состояниями, также известными как отношения BEP ) [14] , которые «достаточно похожи», например, масштабирование OH и OOH. [15] Применение масштабных соотношений к задачам проектирования катализаторов значительно снижает размерность пространства (иногда до 1 или 2). [16] Можно также использовать микрокинетическое моделирование, основанное на таких масштабных соотношениях, чтобы принять во внимание кинетику, связанную с адсорбцией, реакцией и десорбцией молекул при определенных условиях давления или температуры. [17] Такое моделирование затем приводит к хорошо известным графикам вулканов, на которых оптимум, качественно описываемый принципом Сабатье, называется «вершиной вулкана». Масштабные соотношения можно использовать не только для связи энергетики радикальных поверхностно-адсорбированных групп (например, O*,OH*) [13] , но и для связи энергетики молекул с замкнутой оболочкой между собой или с соответствующими радикальными адсорбатами. . [18] Недавней задачей исследователей в области каталитических наук является «разрушение» масштабных соотношений. [19] Корреляции, проявляющиеся в масштабных соотношениях, ограничивают пространство конструкции катализатора, не позволяя достичь «вершины вулкана». Нарушение масштабных соотношений может относиться либо к проектированию поверхностей или мотивов, которые не следуют масштабному соотношению, либо к мотивам, которые следуют другому масштабному соотношению (чем обычному соотношению для связанных адсорбатов) в правильном направлении: тому, которое может приблизить нас к вершина реактивного вулкана. [16] Помимо изучения каталитической реакционной способности, масштабные соотношения можно использовать для изучения и проверки материалов на селективность по отношению к определенному продукту. [20]Существуют особые комбинации энергий связи, которые отдают предпочтение определенным продуктам перед другими. Иногда набор энергий связи, которые могут изменить селективность в отношении конкретного продукта, «масштабируется» друг с другом, поэтому для улучшения селективности необходимо нарушить некоторые соотношения масштабирования; примером этого является масштабирование между энергиями окислительной активации метана и метанола, что приводит к отсутствию селективности при прямом превращении метана в метанол. [21]
Деактивация катализатора определяется как потеря каталитической активности и/или селективности с течением времени.
Вещества, снижающие скорость реакции, называются ядами . Яды хемосорбируются на поверхности катализатора и уменьшают количество доступных активных центров, с которыми могут связываться молекулы реагентов. [22] К распространенным ядам относятся элементы групп V, VI и VII (например, S, O, P, Cl), некоторые токсичные металлы (например, As, Pb) и адсорбирующие вещества с кратными связями (например, CO, ненасыщенные углеводороды). [6] [22] Например, сера нарушает производство метанола, отравляя катализатор Cu/ZnO. [23] Вещества, увеличивающие скорость реакции, называются промоторами . Например, присутствие щелочных металлов при синтезе аммиака увеличивает скорость диссоциации N 2 . [23]
Присутствие ядов и промоторов может изменить энергию активации стадии ограничения скорости и повлиять на селективность катализатора в отношении образования определенных продуктов. В зависимости от количества вещество может быть благоприятным или неблагоприятным для химического процесса. Например, при производстве этилена небольшое количество хемосорбированного хлора будет действовать как промотор, улучшая селективность Ag-катализатора по отношению к этилену по сравнению с CO 2 , тогда как слишком большое количество хлора будет действовать как яд. [6]
Другие механизмы дезактивации катализатора включают:
В промышленности дезактивация катализатора ежегодно обходится в миллиарды долларов из-за остановки процесса и замены катализатора. [22]
В промышленности необходимо учитывать множество проектных переменных, включая конструкцию реактора и катализатора в различных масштабах: от субнанометра до десятков метров. Обычные реакторы гетерогенного катализа включают реакторы периодического действия , непрерывного действия и реакторы с псевдоожиженным слоем , в то время как более поздние установки включают реакторы с неподвижным слоем, микроканальные и многофункциональные реакторы . [6] Другими переменными, которые следует учитывать, являются размеры реактора, площадь поверхности, тип катализатора, носитель катализатора, а также условия работы реактора, такие как температура, давление и концентрации реагентов.

Ниже перечислены некоторые крупномасштабные промышленные процессы с использованием гетерогенных катализаторов. [4]

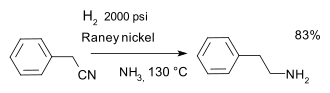
Хотя большинство гетерогенных катализаторов являются твердыми, существует несколько разновидностей, имеющих практическую ценность. В случае двух несмешивающихся растворов (жидкостей) один содержит катализатор, а другой — реагент. Эта установка лежит в основе двухфазного катализа, реализованного в промышленном производстве бутиральдегида гидроформилированием пропилена. [31]
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка ){{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка )