Гуманизированные антитела — это антитела нечеловеческих видов, чьи белковые последовательности были изменены для повышения их сходства с вариантами антител, вырабатываемыми естественным образом у людей. [1] [2] Процесс «гуманизации» обычно применяется к моноклональным антителам, разработанным для введения людям (например, антителам, разработанным в качестве противораковых препаратов). Гуманизация может быть необходима, когда процесс разработки специфического антитела включает генерацию в нечеловеческой иммунной системе (например, у мышей). Белковые последовательности антител, полученных таким образом, частично отличаются от гомологичных антител, встречающихся естественным образом у людей, и поэтому потенциально иммуногенны при введении пациентам-людям (см. также Человеческие антимышиные антитела ). Международные непатентованные названия гуманизированных антител заканчиваются на -зумаб , как в омализумабе (см. Номенклатура моноклональных антител ).
Гуманизированные антитела отличаются от химерных антител . У последних также есть свои белковые последовательности, более похожие на человеческие антитела, но они несут большую часть нечеловеческого белка.
Существуют и другие способы разработки моноклональных антител. Этот список охватывает многие из моноклональных антител, разработанных для использования на людях.
Процесс гуманизации использует тот факт, что производство моноклональных антител может быть достигнуто с использованием рекомбинантной ДНК для создания конструкций [3], способных к экспрессии в культуре клеток млекопитающих . То есть, сегменты генов, способные производить антитела, изолируются и клонируются в клетки, которые могут быть выращены в биореакторе, так что белки антител, полученные из ДНК клонированных генов, могут быть собраны в большом количестве . Этап, включающий рекомбинантную ДНК, обеспечивает точку вмешательства, которую можно легко использовать для изменения последовательности белка экспрессируемого антитела. Таким образом, все изменения в структуре антитела, достигаемые в процессе гуманизации, осуществляются с помощью методов на уровне ДНК. Не все методы получения антител, предназначенных для терапии человека, требуют этапа гуманизации (например, фагового дисплея ), но по сути все они зависят от методов, которые аналогичным образом позволяют «вставлять» или «выгружать» части молекулы антитела.
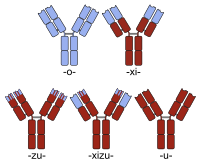
Гуманизация обычно рассматривается как нечто отличное от создания химеры антитела мышь-человек . Таким образом, хотя создание химеры антитела обычно предпринимается для получения более человеческого антитела (путем замены константной области мышиного антитела на человеческую), простые химеры этого типа обычно не называются гуманизированными. Скорее, белковая последовательность гуманизированного антитела по существу идентична таковой человеческого варианта, несмотря на нечеловеческое происхождение некоторых сегментов его определяющей комплементарность области (CDR), ответственных за способность антитела связываться с его целевым антигеном.
Названия химерных антител содержат корень -xi- . Примерами химерных антител, одобренных для терапии у людей, являются абциксимаб (ReoPro), базиликсимаб (Simulect), цетаксимаб (Erbitux), инфликсимаб (Remicade) и ритуксимаб (MabThera). Также есть несколько примеров химер, которые в настоящее время проходят клинические испытания (например, бавитуксимаб , см. сортируемый список для дополнительных примеров).
Процесс гуманизации может также включать создание химеры мышь-человек в качестве начального шага. В этом случае вариабельная область мыши сшивается с константной областью человека. Затем химера может быть далее гуманизирована путем выборочного изменения последовательности аминокислот в вариабельной области молекулы.
Процесс изменения должен быть «избирательным», чтобы сохранить специфичность, для которой антитело было изначально разработано. То есть, поскольку части CDR вариабельной области необходимы для способности антитела связываться с его предполагаемой целью, аминокислоты в этих частях не могут быть изменены без риска подорвать цель разработки. Помимо сегментов CDR, части вариабельных областей, которые отличаются от тех, что у людей, могут быть скорректированы путем замены соответствующих отдельных аминокислот. Это достигается на уровне ДНК посредством мутагенеза .
Наименование гуманизированных химер включает основу для обоих обозначений ( -xi- + -zu- ). Отеликсизумаб является примером гуманизированной химеры, которая в настоящее время проходит клинические испытания для лечения ревматоидного артрита и сахарного диабета . [4]
Можно получить гуманизированное антитело без создания химерного промежуточного продукта. «Прямое» создание гуманизированного антитела может быть достигнуто путем вставки соответствующих сегментов кодирования CDR (так называемых «доноров», отвечающих за желаемые свойства связывания) в «каркас» человеческого антитела (так называемый «акцептор»). Как обсуждалось выше, это достигается с помощью методов рекомбинантной ДНК с использованием соответствующего вектора [3] и экспрессии в клетках млекопитающих. То есть, после того, как антитело разработано с желаемыми свойствами у мыши (или другого нечеловеческого организма), ДНК, кодирующая это антитело, может быть выделена, клонирована в вектор и секвенирована (или ДНК может быть секвенирована напрямую с использованием методов отдельных клеток). Затем может быть определена последовательность ДНК, соответствующая CDR антитела. Как только точная последовательность желаемых CDR известна, может быть разработана стратегия для вставки этих последовательностей соответствующим образом в конструкцию, содержащую ДНК для варианта человеческого антитела. [5] [6] [7] [8] [9] Стратегия может также использовать синтез линейных фрагментов ДНК на основе чтения последовательностей CDR. Процесс требует программного обеспечения для компьютерного моделирования, чтобы определить, какие аминокислоты антитела могут быть изменены с мышиной последовательности на человеческую последовательность без изменений, нарушающих конформацию сайта связывания. В Соединенных Штатах это программное обеспечение было разработано, запатентовано и продемонстрировано Protein Design Labs, Inc. в Маунтин-Вью, Калифорния, в 1980-х и 1990-х годах. [10]
Алемтузумаб является ранним примером антитела, гуманизация которого не включала химерный промежуточный продукт. В этом случае моноклональное антитело, названное «Campath-1», было разработано для связывания CD52 с использованием мышиной системы. Гипервариабельные петли Campath-1 (которые содержат его CDR и, таким образом, придают ему способность связывать CD52) были затем извлечены и вставлены в каркас человеческого антитела. [1] Алемтузумаб одобрен для лечения В-клеточного хронического лимфоцитарного лейкоза [11] и в настоящее время проходит клинические испытания для множества других состояний, включая рассеянный склероз . [12]
Существуют технологии, которые полностью исключают использование мышей или других нечеловеческих млекопитающих в процессе обнаружения антител для человеческой терапии. Примерами таких систем являются различные методы «дисплея» (в первую очередь фаговый дисплей ), а также методы, которые используют повышенные уровни В-клеток, возникающие во время иммунного ответа человека.
Они используют селективные принципы производства специфических антител, но используют микроорганизмы (как в фаговом дисплее ) или даже бесклеточные экстракты (как в рибосомном дисплее ). Эти системы основаны на создании «библиотек» генов антител , которые могут быть полностью получены из человеческой РНК, выделенной из периферической крови . Непосредственными продуктами этих систем являются фрагменты антител, обычно Fab или scFv .
Это означает, что, хотя фрагменты антител, созданные с использованием методов отображения, имеют полностью человеческую последовательность, они не являются полными антителами. Поэтому для включения и выражения полученных аффинностей в полное антитело используются процессы, по сути идентичные гуманизации.
Адалимумаб (Хумира) — пример антитела, одобренного для терапии человека, который был создан с помощью фагового дисплея. [13] [14]
Можно использовать иммунную реакцию человека при открытии моноклональных антител. Проще говоря, иммунная реакция человека работает так же, как у мыши или другого млекопитающего, не являющегося человеком. Поэтому люди, испытывающие вызов своей иммунной системе, такой как инфекционное заболевание, рак или вакцинация, являются потенциальным источником моноклональных антител, направленных на этот вызов. Этот подход кажется особенно подходящим для разработки противовирусной терапии, которая использует принципы пассивного иммунитета . Варианты этого подхода были продемонстрированы в принципе [15] , и некоторые из них находят свой путь в коммерческую разработку. [16]