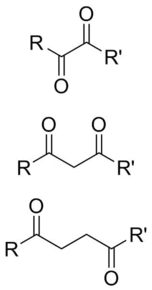
В органической химии дикарбонилом называют молекулу , содержащую две карбонильные ( С=О ) группы . Хотя этот термин может относиться к любому органическому соединению , содержащему две карбонильные группы, более конкретно он используется для описания молекул, в которых оба карбонила находятся достаточно близко, чтобы их реакционная способность изменилась, например, 1,2-, 1,3- и 1,4-дикарбонилы. Их свойства часто отличаются от свойств монокарбонилов, поэтому их обычно считают собственными функциональными группами. Эти соединения могут иметь симметричные или несимметричные заместители на каждом карбониле, а также могут быть функционально симметричными (диальдегиды , дикетоны , диэфиры и т . д. ) или несимметричными (кетоэфиры, кетокислоты и т. д. ).
Единственным 1,2-диальдегидом является глиоксаль ( CHO) 2 . Как и многие алкилдиальдегиды, глиоксаль встречается почти исключительно в виде его гидрата и его олигомеров. Эти производные часто ведут себя так же, как альдегиды, поскольку гидратация обратима. Глиоксаль легко конденсируется с аминами . В результате таких реакций он является предшественником многих гетероциклов , например имидазолов .

Основным дикетоном является диацетил , также известный как 2,3-бутандион, CH 3 C(O)C(O)CH 3 . 1,2-Дикетоны часто образуются в результате окисления (дегидрирования) диолов : [ 1]
2,3-Бутандион, 2,3-пентандион и 2,3-гександион содержатся в небольших количествах в различных продуктах питания. Их используют в качестве ароматических компонентов в безалкогольных напитках и хлебобулочных изделиях. [1] Бензил ( PhCO) 2 представляет собой соответствующее производное дифенила.
Отличительной особенностью 1,2-дикетонов является длинная связь CC, соединяющая карбонильные группы. Это расстояние связи составляет около 1,54 Å по сравнению с 1,45 Å для соответствующей связи в 1,3-бутадиене . Эффект объясняется отталкиванием частичных положительных зарядов карбонильных атомов углерода. [2]
1,2-Дикетоны конденсируются со многими бифункциональными нуклеофилами, такими как мочевина и тиомочевина , с образованием гетероциклов. Конденсация с ароматическими аминами дает дикетимин ( (RC=NAr) 2 ).
В случае 1,2-циклогександиона и 1,2-циклопентандиона енол примерно на 1–3 ккал/моль более стабилен , чем дикето-форма. [3]
орто-хинон , C 4 H 4 (CO) 2 , является родителем большого семейства 1,2-дикетонов.

Хорошо известным соединением этого класса является метилглиоксаль CH 3 C( O )CHO , также известный как пирувальдегид. Эти соединения известны также как 2-оксоальдегиды [4] или α-кетоальдегиды.
Щавелевая кислота и ее эфиры определяют это семейство соединений. Двухкислотную кислоту производят в промышленных масштабах путем окисления отходов сахара. Он встречается в природе (как конъюгированное основание), особенно у растений вида Oxalis . Конденсация диэфиров с диаминами дает циклические диамиды.

α-Кетокислоты и -эфиры хорошо известны. Пировиноградная кислота ( CH 3 C(O)CO 2 H ) является исходной α-кетокислотой. Его сопряженное основание пируват ( CH 3 C(O)CO−2), является компонентом цикла лимонной кислоты и продуктом метаболизма глюкозы ( гликолиза ). Соответствующей альдегидной кислотой является глиоксалевая кислота ( HC(O)CO 2 H ).
Исходным 1,3-диальдегидом является малоновой диальдегид ( CH 2 (CHO) 2 ), β-дикарбонил. Как и большинство диальдегидов, он редко встречается как таковой. Вместо этого с ним обращаются почти исключительно как с его гидратом, метилацеталем и его олигомерами. Эти производные часто ведут себя как родительские. Известно множество 2-замещенных производных. Их часто получают алкилированием енолята малонового диальдегида.
1,3-Дикетоны также называют β-дикетонами. Важным членом является ацетилацетон CH 3 C (O)CH 2 C(O)CH 3 . Димедон представляет собой циклический 1,3-дикетон. 1,3-Индандион представляет собой циклический 1,3-дикетон, конденсированный с бензольным кольцом. Ацетилацетон получают в промышленности термической перегруппировкой изопропенилацетата. [1] Другим циклическим 1,3-дикетоном является 2,2,4,4-тетраметилциклобутандион , который является предшественником полезного диола .
1,3-Дикетоны часто таутомеризуются с образованием енола . Обычно они существуют преимущественно в енольной форме. Процент енола в ацетилацетоне , трифторацетилацетоне и гексафторацетилацетоне составляет 85, 97 и 100% соответственно (в чистом виде, 33 °C). [5] Циклические 1,3-дикетоны, такие как 1,3-циклогександион и димедон , также существуют в значительной степени в енольной форме.
Как и другие дикетоны, 1,3-дикетоны являются универсальными предшественниками гетероциклов. Основание-конъюгат, полученное из 1,3-кетонов, может служить лигандом для образования координационных комплексов ацетилацетоната металла . В реакции ДеМайо 1,3-дикетоны реагируют с алкенами в фотохимической перициклической реакции с образованием (замещенных) 1,5-дикетонов.
Классически 1,3-дикетоны получают конденсацией Кляйзена кетона со сложным эфиром.
Малоновая кислота и ее эфиры являются исходными представителями этого класса дикарбонилов. Также распространены 2-замещенные производные формулы RCH(CO 2 R) 2 , которые возникают в результате C-алкилирования сопряженного основания (енолята) NaCH(CO 2 R) 2 .
β-кетоэфиры легко возникают в результате конденсации пары сложных эфиров. Хорошо известным примером является этилацетоацетат (хотя его получают путем этанолиза кетена ).
Сукцинальдегид (CH 2 CHO) 2 — простейший и родительский 1,4-диальдегид. Ароматическое производное — фталальдегид .

Дикетоны с двумя метиленовыми группами, разделяющими карбонильные группы, также называемые γ-дикетонами, обычно сосуществуют со своими енольными таутомерами . Наиболее выдающимся представителем является ацетонилацетон . 1,4-Дикетоны являются полезными предшественниками гетероциклов посредством синтеза Паала-Кнорра , который дает пирролы :
Эта реактивность лежит в основе нейротоксичности γ -дикетонов. [6] 1,4-Дикетоны также являются предшественниками фуранов и тиофенов . Конденсация 1,4-дикетонов (и родственных субстратов) с гидразинами дает дигидропиридазины, которые можно превратить в пиридазины .
парахинон , C 4 H 4 (CO) 2 , является родителем большого семейства 1,4-дикетонов.
Янтарная кислота и ее эфиры являются родительскими членами этого семейства 1,4-дикарбонилов. Янтарная кислота известна как компонент цикла лимонной кислоты . Образует ангидрид циклической кислоты, янтарный ангидрид . К ненасыщенным членам относятся малеиновая и фумаровая кислоты и их сложные эфиры.
Глутаральдегид (CH 2 ) 3 (CHO) 2 является простейшим и исходным 1,5-диальдегидом. Он легко увлажняет. Ароматический аналог — изофталевый альдегид . [7]
Эти дикетоны имеют три метиленовые группы, разделяющие карбонильные группы.
Глутаровая кислота (CH 2 ) 3 (CO 2 H) 2 является исходной 1,5-дикислотой.

Малые альдегиды имеют тенденцию к гидратации. Для диальдегидов преобладает гидратация. Глиоксаль образует ряд циклических гидратов. Сукцинальдегид легко гидратируется с образованием 2,5-дигидрокситетрагидрофурана. Ароматический фталальдегид также образует гидратированный.

Подобные равновесия гидратации и циклизации применимы к малеиновому диальдегиду, [8] [9] глутаральдегиду и адипальдегиду .
Ряд дикарбонильных соединений биоактивны. Известно, что диацетил вызывает облитерирующий бронхиолит у лиц, подвергающихся его воздействию на производстве. [10] Диальдегиды, например глутаральдегид и малоновый альдегид, являются фиксаторами или стерилизаторами.