Жировая ткань (также известная как жировые отложения или просто жир ) представляет собой рыхлую соединительную ткань , состоящую в основном из адипоцитов . [1] [2] Он также содержит стромально-сосудистую фракцию ( СВФ ) клеток, включая преадипоциты , фибробласты , сосудистые эндотелиальные клетки и различные иммунные клетки, такие как макрофаги жировой ткани . Его основная роль — хранить энергию в виде липидов , хотя он также смягчает и изолирует тело.
Ранее считавшаяся гормонально инертной, в последние годы жировая ткань признана основным эндокринным органом [3] , поскольку она вырабатывает такие гормоны , как лептин , эстроген , резистин и цитокины (особенно TNFα ). [2] При ожирении жировая ткань участвует в хроническом высвобождении провоспалительных маркеров, известных как адипокины , которые ответственны за развитие метаболического синдрома — совокупности заболеваний, включая диабет 2 типа , сердечно-сосудистые заболевания и атеросклероз . [2] [4]
Жировая ткань происходит из преадипоцитов, и ее образование, по-видимому, частично контролируется жировым геном . Два типа жировой ткани — это белая жировая ткань (БЖТ), которая сохраняет энергию, и бурая жировая ткань (БЖТ), которая генерирует тепло тела. Жировая ткань, точнее бурая жировая ткань, была впервые обнаружена швейцарским натуралистом Конрадом Гесснером в 1551 году. [5]
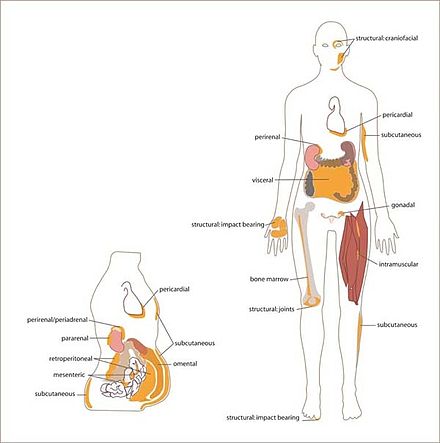
У человека жировая ткань расположена: под кожей ( подкожный жир ), вокруг внутренних органов ( висцеральный жир ), в костном мозге ( желтый костный мозг ), межмышечной ( мышечная система ) и в молочной железе ( ткань молочной железы ). Жировая ткань находится в определенных местах, которые называются жировыми депо . Помимо адипоцитов, которые составляют самый высокий процент клеток в жировой ткани, присутствуют и другие типы клеток, которые в совокупности называются стромально-васкулярной фракцией (СВФ) клеток. СВФ включает преадипоциты , фибробласты , макрофаги жировой ткани и эндотелиальные клетки .
Жировая ткань содержит множество мелких кровеносных сосудов . В покровной системе , к которой относится и кожа, он накапливается на самом глубоком уровне, в подкожном слое, обеспечивая изоляцию от жары и холода. Вокруг органов он обеспечивает защитную прокладку. Однако его основная функция — быть резервом липидов, которые могут окисляться для удовлетворения энергетических потребностей организма и защиты его от избытка глюкозы путем хранения триглицеридов, вырабатываемых печенью из сахаров, хотя некоторые данные свидетельствуют о том, что большая часть синтеза липидов из углеводов происходит в самой жировой ткани. [6] Жировые депо в разных частях тела имеют разные биохимические профили. В нормальных условиях он обеспечивает обратную связь с мозгом о голоде и диете.

У мышей есть восемь основных жировых депо, четыре из которых находятся в брюшной полости . [1] Парные депо гонад прикрепляются к матке и яичникам у женщин, а также к придаткам яичек и семенникам у мужчин; парные забрюшинные депо располагаются вдоль дорсальной стенки живота , окружая почку, и в случае массивности распространяются в таз. Брыжеечное депо образует клееподобную паутину, которая поддерживает кишечник и сальниковое депо (начинающееся возле желудка и селезенки ) и - когда оно массивное - распространяется на вентральную часть живота. И брыжеечные, и сальниковые депо включают большое количество лимфоидной ткани в виде лимфатических узлов и молочных пятен соответственно.
Двумя поверхностными депо являются парные паховые депо, которые находятся впереди верхнего сегмента задних конечностей (под кожей), и подлопаточные депо, парные медиальные смеси бурой жировой ткани, прилегающие к областям белой жировой ткани, которые обнаруживаются под кожей между тыльными гребнями лопаток. Слой бурой жировой ткани в этом депо часто покрыт «глазурью» белой жировой ткани; иногда эти два типа жира (бурый и белый) трудно различить. Паховые депо окружают паховую группу лимфатических узлов. Второстепенные депо включают перикард , который окружает сердце, и парные подколенные депо, между основными мышцами позади коленей, каждый из которых содержит один большой лимфатический узел . [7] Из всех депо у мышей гонадные депо являются самыми большими и наиболее легко рассекаемыми, [8] они составляют около 30% расслаиваемого жира. [9]
У человека с ожирением избыток жировой ткани, свисающий вниз от живота, называется панникулюсом . Панникулюс осложняет хирургическое вмешательство у людей с морбидным ожирением. Он может оставаться в буквальном смысле «кожным фартуком», если человек с тяжелым ожирением теряет большое количество жира (частый результат операции по шунтированию желудка ). Ожирение лечится с помощью физических упражнений, диеты и поведенческой терапии. Реконструктивная хирургия является одним из аспектов лечения. [10]

Висцеральный жир или абдоминальный жир [11] (также известный как органный жир или внутрибрюшный жир) расположен внутри брюшной полости , упакован между органами (желудком, печенью, кишечником, почками и т. д.). Висцеральный жир отличается от подкожного жира под кожей и внутримышечного жира, рассеянного в скелетных мышцах . Жир в нижней части тела, как на бедрах и ягодицах, находится подкожно и не представляет собой равномерно расположенную ткань, тогда как жир в области живота в основном висцеральный и полужидкий. [12] Висцеральный жир состоит из нескольких жировых отложений, в том числе мезентериальных , придаточных отложений белой жировой ткани (EWAT) и околопочечных отложений. Висцеральный жир часто выражают по его площади в см 2 (ВЖК, площадь висцерального жира). [13]
Избыток висцерального жира известен как абдоминальное ожирение , или «животный жир», при котором живот чрезмерно выпячивается. Новые разработки, такие как индекс объема тела (BVI), специально разработаны для измерения объема брюшной полости и количества брюшного жира. Избыток висцерального жира также связан с диабетом 2 типа , [14] резистентностью к инсулину , [15] воспалительными заболеваниями , [16] и другими заболеваниями, связанными с ожирением. [17] Аналогично, было показано, что накопление жира на шее (или шейной жировой ткани) связано со смертностью. [18] Несколько исследований показали, что висцеральный жир можно предсказать на основе простых антропометрических показателей, [19] и он предсказывает смертность более точно, чем индекс массы тела или окружность талии. [20]
У мужчин чаще жир накапливается в области живота из-за различий в половых гормонах . Эстроген (женский половой гормон) вызывает отложение жира в ягодицах, бедрах и бедрах у женщин. [21] [22] Когда женщины достигают менопаузы и уровень эстрогена, вырабатываемого яичниками, снижается, жир мигрирует с ягодиц, бедер и бедер на талию; [23] позже жир откладывается в области живота. [12]
Висцеральный жир может быть вызван избытком кортизола. [24] По крайней мере 10 МЕТ -часов в неделю аэробных упражнений приводят к уменьшению висцерального жира у людей без метаболических нарушений. [25] Тренировки с отягощениями и ограничение калорий также уменьшают количество висцерального жира, хотя их эффект может не быть кумулятивным. [26] И физические упражнения, и гипокалорийная диета вызывают потерю висцерального жира, но упражнения оказывают большее влияние на висцеральный жир, чем на общий жир. [27] Высокоинтенсивные упражнения — один из способов эффективного уменьшения общего количества жира в брюшной полости. [28] [29] Диета с ограничением энергии в сочетании с физическими упражнениями приведет к снижению общего количества жира в организме и соотношения висцеральной жировой ткани к подкожной жировой ткани, что предполагает предпочтительную мобилизацию висцерального жира по сравнению с подкожным жиром. [30]
Эпикардиальная жировая ткань (ЭЖТ) представляет собой особую форму висцерального жира, отложившегося вокруг сердца и являющегося метаболически активным органом, генерирующим различные биоактивные молекулы, которые могут существенно влиять на сердечную функцию. [31] [32] [33] Заметные различия компонентов наблюдались при сравнении ЭЖТ с подкожным жиром , что позволяет предположить специфическое влияние накопленных жирных кислот на функцию и метаболизм адипоцитов. [34]
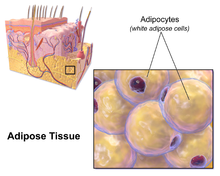
Большая часть оставшегося невисцерального жира находится чуть ниже кожи в области, называемой гиподермой . [35] Этот подкожный жир не связан со многими классическими патологиями, связанными с ожирением, такими как болезни сердца , рак и инсульт , и некоторые данные даже предполагают, что он может иметь защитную функцию. [36] Типично женский (или гинекоидный) тип распределения жира в организме вокруг бедер, бедер и ягодиц представляет собой подкожный жир и, следовательно, представляет меньший риск для здоровья по сравнению с висцеральным жиром. [37] [38]
Как и все другие жировые органы, подкожно-жировая клетчатка является активной частью эндокринной системы, секретирующей гормоны лептин и резистин . [35]
Взаимосвязь между подкожным жировым слоем и общим количеством жира в организме человека часто моделируется с помощью уравнений регрессии. Самое популярное из этих уравнений было составлено Дарнином и Уормерсли, которые тщательно протестировали многие типы кожных складок и в результате создали две формулы для расчета плотности тела как мужчин, так и женщин. Эти уравнения представляют обратную корреляцию между кожными складками и плотностью тела: по мере увеличения суммы кожных складок плотность тела уменьшается. [39]
Такие факторы, как пол, возраст, численность населения или другие переменные, могут сделать уравнения недействительными и непригодными для использования, и по состоянию на 2012 год [обновлять]уравнения Дарнина и Уормерсли остаются лишь оценками истинного уровня ожирения человека. Новые формулы все еще создаются. [39]
Костный жир, также известный как костномозговая жировая ткань (ЖТ), представляет собой плохо изученное жировое депо, которое находится в кости и перемежается кроветворными клетками, а также костными элементами. Адипоциты в этом депо происходят из мезенхимальных стволовых клеток (МСК) , которые могут давать начало жировым клеткам, костным клеткам, а также другим типам клеток. Тот факт, что МАТ увеличивается в условиях ограничения калорий/анорексии, является особенностью, отличающей это депо от других жировых депо. [40] [41] [42] Физические упражнения регулируют MAT, уменьшая количество MAT и размер адипоцитов костного мозга. [43] [44] [45] Регуляция содержания жира в костном мозге с помощью упражнений позволяет предположить, что он имеет некоторое физиологическое сходство с другими отложениями белой жировой ткани. Более того, увеличение MAT при ожирении также предполагает сходство с отложениями белого жира. [43]
Эктопический жир — это накопление триглицеридов в тканях, отличных от жировой ткани, которые, как предполагается, содержат лишь небольшое количество жира, таких как печень , скелетные мышцы , сердце и поджелудочная железа . [1] Это может влиять на клеточные функции и, следовательно, на функции органов и связано с резистентностью к инсулину при диабете 2 типа. [46] Он хранится в относительно больших количествах вокруг органов брюшной полости , но его не следует путать с висцеральным жиром.
Конкретная причина накопления внематочного жира неизвестна. Причиной, вероятно, является сочетание генетических, экологических и поведенческих факторов, которые связаны с избыточным потреблением энергии и снижением физической активности. Существенная потеря веса может уменьшить запасы эктопического жира во всех органах, что связано с улучшением функции этих органов. [46]
В последнем случае неинвазивные меры по снижению веса, такие как диета или физические упражнения, могут уменьшить количество эктопического жира (особенно в сердце и печени) у детей и взрослых с избыточным весом или ожирением. [47] [48]
Свободные жирные кислоты (СЖК) высвобождаются из липопротеинов под действием липопротеинлипазы (ЛПЛ) и попадают в адипоциты, где снова собираются в триглицериды путем этерификации их на глицерине . [2] Жировая ткань человека содержит около 87% липидов . [49]
Существует постоянный поток СЖК, поступающих и покидающих жировую ткань. [2] Чистое направление этого потока контролируется инсулином и лептином: если уровень инсулина повышен, то возникает чистый приток СЖК внутрь, и только при низком уровне инсулина СЖК могут покинуть жировую ткань. Секреция инсулина стимулируется высоким уровнем сахара в крови, возникающим в результате потребления углеводов. [50]
У людей липолиз (гидролиз триглицеридов до свободных жирных кислот) контролируется посредством сбалансированного контроля липолитических B-адренергических рецепторов и антилиполиза, опосредованного a2A-адренергическими рецепторами.
Жировые клетки играют важную физиологическую роль в поддержании уровня триглицеридов и свободных жирных кислот, а также в определении резистентности к инсулину . [2] Абдоминальный жир имеет другой метаболический профиль — он более склонен вызывать резистентность к инсулину. Это в значительной степени объясняет, почему центральное ожирение является маркером нарушения толерантности к глюкозе и независимым фактором риска сердечно-сосудистых заболеваний (даже при отсутствии сахарного диабета и гипертонии ). [51] Исследования самок обезьян в Университете Уэйк Форест (2009) обнаружили, что люди с более высоким стрессом имеют более высокий уровень висцерального жира в организме. Это предполагает возможную причинно-следственную связь между ними, при которой стресс способствует накоплению висцерального жира, что, в свою очередь, вызывает гормональные и метаболические изменения, которые способствуют болезням сердца и другим проблемам со здоровьем. [52]
Последние достижения в области биотехнологии позволили получать взрослые стволовые клетки из жировой ткани, что позволяет стимулировать возобновление роста тканей с использованием собственных клеток пациента. Кроме того, как сообщается, стволовые клетки, полученные из жировой ткани, как человека, так и животных, можно эффективно перепрограммировать в индуцированные плюрипотентные стволовые клетки без необходимости использования фидерных клеток . [53] Использование собственных клеток пациента снижает вероятность отторжения тканей и позволяет избежать этических проблем, связанных с использованием эмбриональных стволовых клеток человека . [54] Все больше данных также свидетельствует о том, что различные жировые отложения (т.е. абдоминальные, сальниковые, перикардиальные) дают стволовые клетки, полученные из жировой ткани, с разными характеристиками. [54] [55] Эти депо-зависимые особенности включают скорость пролиферации , иммунофенотип , потенциал дифференцировки , экспрессию генов , а также чувствительность к гипоксическим условиям культивирования. [56] Уровни кислорода, по-видимому, играют важную роль в метаболизме и в целом на функции стволовых клеток, полученных из жировой ткани. [57]
Жировая ткань является основным периферическим источником ароматазы как у мужчин, так и у женщин, способствуя выработке эстрадиола . [58]
Гормоны, полученные из жировой ткани , включают:
Жировая ткань также секретирует тип цитокинов (межклеточные сигнальные белки), называемых адипокинами (жировые цитокины), которые играют роль в осложнениях, связанных с ожирением. Периваскулярная жировая ткань высвобождает адипокины, такие как адипонектин, которые влияют на сократительную функцию сосудов, которые они окружают. [1] [59]

Бурый жир или бурая жировая ткань (БЖТ) представляет собой специализированную форму жировой ткани, важную для адаптивного термогенеза у людей и других млекопитающих. BAT может генерировать тепло, «разъединяя» дыхательную цепь окислительного фосфорилирования в митохондриях посредством тканеспецифической экспрессии разобщающего белка 1 (UCP1). [60] BAT в основном локализуется вокруг шеи и крупных кровеносных сосудов грудной клетки , где может эффективно осуществлять теплообмен. BAT активно активируется при воздействии холода за счет высвобождения катехоламинов из симпатических нервов , что приводит к активации UCP1. Почти половина нервов, присутствующих в жировой ткани, представляют собой сенсорные нейроны, связанные с ганглиями дорсальных корешков . [61]
Активация BAT также может произойти в ответ на перекармливание. [62] Активность UCP1 стимулируется длинноцепочечными жирными кислотами, которые образуются после активации β-адренергических рецепторов . [60] Предполагается, что UCP1 действует как симпортер протонов жирных кислот , хотя точный механизм еще не выяснен. [63] Напротив, UCP1 ингибируется АТФ , АДФ и ГТФ . [64]
Попытки смоделировать этот процесс фармакологически пока не увенчались успехом. Методы управления дифференциацией «бурого жира» могут стать механизмом терапии для снижения веса в будущем, стимулируя рост тканей с помощью этого специализированного метаболизма, не вызывая его в других органах. Обзор возможного терапевтического применения бурого жира для лечения ожирения у людей был опубликован Самуэльсоном и Видалем-Пуигом в 2020 году. [65]
До недавнего времени считалось, что бурая жировая ткань у людей в основном встречается только у младенцев, но новые данные опровергли это мнение. Метаболически активная ткань с температурными реакциями, сходными с бурой жировой тканью, впервые была обнаружена на шее и туловище некоторых взрослых людей в 2007 году [66] , а наличие бурой жировой ткани у взрослых людей было позже подтверждено гистологически в тех же анатомических областях. [67] [68] [69]
Потемнение WAT, также называемое «beiging», происходит, когда адипоциты в депо WAT приобретают черты BAT. Бежевые адипоциты приобретают многокамерный вид (содержат несколько липидных капель) и повышают экспрессию разобщающего белка 1 (UCP1). [70] При этом эти адипоциты, обычно запасающие энергию, становятся адипоцитами, высвобождающими энергию.
Способность бурого и бежевого жира сжигать калории тщательно изучается, поскольку исследовательские усилия сосредоточены на методах лечения ожирения и диабета. Препарат 2,4-динитрофенол , который также действует как химический разобщитель, подобно UCP1, использовался для снижения веса в 1930-х годах. Однако его быстро прекратили, когда чрезмерная дозировка привела к неблагоприятным побочным эффектам, включая гипертермию и смерть. [70] Агонисты β3, такие как CL316,243, также были разработаны и протестированы на людях. Однако использование таких препаратов оказалось в значительной степени безуспешным из-за ряда проблем, включая различную видовую специфичность рецепторов и плохую биодоступность при пероральном приеме . [71]
Холод является основным регулятором процессов BAT и вызывает потемнение WAT. Потемнение в ответ на хроническое воздействие холода хорошо документировано и является обратимым процессом. Исследование на мышах показало, что потемнение, вызванное холодом, можно полностью обратить вспять за 21 день, при этом измеримое снижение UCP1 наблюдается в течение 24 часов. [72] Исследование Rosenwald et al. выявили, что когда животные повторно подвергаются воздействию холодной среды, те же самые адипоциты приобретают бежевый фенотип, что позволяет предположить, что бежевые адипоциты сохраняются. [73]
Регуляторы транскрипции, а также растущее число других факторов регулируют индукцию образования бежевого жира. Четыре регулятора транскрипции играют центральную роль в потемнении WAT и служат мишенями для многих молекул, которые, как известно, влияют на этот процесс. [74] К ним относятся гамма-рецептор, активирующий пролифератор пероксисом (PPARγ) , PRDM16, [75] коактиватор гамма-рецептора, активирующий пролифератор пероксисомы 1 альфа (PGC-1α) , и ранний B-клеточный фактор-2 (EBF2). [76] [77] [78]
Список молекул, влияющих на потемнение, вырос прямо пропорционально популярности этой темы и постоянно расширяется по мере приобретения новых знаний. Среди этих молекул — иризин и фактор роста фибробластов 21 ( FGF21 ), которые хорошо изучены и считаются важными регуляторами потемнения. Иризин секретируется мышцами в ответ на физическую нагрузку и, как было показано, усиливает потемнение кожи, воздействуя на бежевые преадипоциты. [79] FGF21, гормон, секретируемый в основном печенью, вызвал большой интерес после того, как был идентифицирован как мощный стимулятор поглощения глюкозы и регулятор потемнения благодаря своему влиянию на PGC-1α. [70] Он увеличивается в BAT во время воздействия холода и, как полагают, способствует устойчивости к ожирению, вызванному диетой. [80] FGF21 также может секретироваться в ответ на физические упражнения и диету с низким содержанием белка, хотя последняя не была тщательно исследована. [81] [82] Данные этих исследований показывают, что факторы окружающей среды, такие как диета и физические упражнения, могут быть важными факторами потемнения. У мышей было обнаружено, что бейджинг может происходить за счет продукции метионин-энкефалиновых пептидов врожденными лимфоидными клетками 2 типа в ответ на интерлейкин 33 . [83]
Из-за сложной природы жировой ткани и растущего списка молекул, регулирующих потемнение, существует большой потенциал для использования инструментов биоинформатики для улучшения исследований в этой области. Исследования по подрумяниванию WAT получили большую пользу от достижений в этих методах, поскольку бежевый жир быстро набирает популярность в качестве терапевтической мишени для лечения ожирения и диабета.
ДНК-микроматрица — это биоинформатический инструмент, используемый для одновременной количественной оценки уровней экспрессии различных генов и широко используемый при изучении жировой ткани. В одном из таких исследований использовался микроматричный анализ в сочетании с программным обеспечением Ingenuity IPA для изучения изменений в экспрессии генов WAT и BAT, когда мыши подвергались воздействию температур 28 и 6 °C. [84] Затем были идентифицированы и использованы для анализа путей дифференциальной экспрессии наиболее значительно повышающих и понижающих активность генов. Было обнаружено, что многие пути, активизирующиеся в WAT после воздействия холода, также высоко выражены в BAT, такие как окислительное фосфорилирование , метаболизм жирных кислот и метаболизм пирувата. [84] Это говорит о том, что некоторые адипоциты перешли на бежевый фенотип при 6 °C. Мессенбёк и др. также использовали микроматричный анализ, чтобы продемонстрировать, что дефицит инсулина ингибирует дифференцировку бежевых адипоцитов, но не нарушает их способность к потемнению. [85] Эти два исследования демонстрируют потенциал использования микрочипов в изучении потемнения WAT.
Секвенирование РНК ( RNA-Seq ) — мощный вычислительный инструмент, позволяющий количественно оценить экспрессию РНК для всех генов в образце. Включение RNA-Seq в исследования потемнения имеет большую ценность, поскольку оно обеспечивает лучшую специфичность, чувствительность и более полный обзор экспрессии генов, чем другие методы. RNA-Seq использовался как в исследованиях на людях, так и на мышах в попытке охарактеризовать бежевые адипоциты в соответствии с профилями экспрессии их генов и идентифицировать потенциальные терапевтические молекулы, которые могут индуцировать бежевый фенотип. В одном из таких исследований использовалась RNA-Seq для сравнения профилей экспрессии генов WAT у мышей дикого типа (WT) и мышей со сверхэкспрессией раннего B-клеточного фактора-2 (EBF2). WAT от трансгенных животных демонстрировал программу генов бурого жира и снижал экспрессию специфичных для WAT генов по сравнению с мышами WT. [86] Таким образом, EBF2 был идентифицирован как потенциальная терапевтическая молекула, вызывающая появление бежи.
Иммунопреципитация хроматина с секвенированием (ChIP-seq) — это метод, используемый для идентификации сайтов связывания белков на ДНК и оценки модификаций гистонов . Этот инструмент позволил изучить эпигенетическую регуляцию потемнения и помогает выяснить механизмы, с помощью которых взаимодействия белок-ДНК стимулируют дифференцировку бежевых адипоцитов. Исследования, наблюдающие за ландшафтами хроматина бежевых адипоцитов, показали, что адипогенез этих клеток является результатом формирования клеточно-специфичных ландшафтов хроматина, которые регулируют программу транскрипции и, в конечном итоге, контролируют дифференцировку. Используя ChIP-seq в сочетании с другими инструментами, недавние исследования выявили более 30 транскрипционных и эпигенетических факторов, которые влияют на развитие бежевых адипоцитов. [86]
Гипотеза бережливого гена (также называемая гипотезой голода) утверждает, что в некоторых популяциях организм будет более эффективно удерживать жир во времена изобилия, тем самым обеспечивая большую устойчивость к голоданию во времена нехватки продовольствия. Эта гипотеза, первоначально выдвинутая в контексте метаболизма глюкозы и резистентности к инсулину, была дискредитирована физическими антропологами, физиологами и самим первоначальным сторонником идеи в этом контексте, хотя, по мнению ее разработчика, она остается «столь же жизнеспособной, как и тогда, когда [оно было] впервые выдвинуто» в других контекстах. [87] [88]
В 1995 году Джеффри Фридман в своей резиденции в Рокфеллеровском университете вместе с Рудольфом Лейбелем , Дугласом Коулманом и др. обнаружили белок лептин , которого не хватало мышам с генетическим ожирением. [89] [90] [91] Лептин вырабатывается в белой жировой ткани и передает сигналы гипоталамусу . Когда уровень лептина падает, организм интерпретирует это как потерю энергии, и голод усиливается. Мыши, которым не хватает этого белка, едят до тех пор, пока их размер не увеличится в четыре раза.
Однако лептин играет разную роль в ожирении, вызванном диетой, у грызунов и людей. Поскольку адипоциты вырабатывают лептин, уровень лептина повышается у людей с ожирением. Однако голод остается, а когда уровень лептина падает из-за потери веса, голод усиливается. Падение уровня лептина лучше рассматривать как сигнал голодания, чем повышение уровня лептина как сигнал насыщения . [92] Однако повышенный уровень лептина при ожирении известен как резистентность к лептину . Изменения, которые происходят в гипоталамусе и приводят к резистентности к лептину при ожирении, в настоящее время находятся в центре внимания исследований ожирения. [93]
Генные дефекты в гене лептина ( ob ) при ожирении у человека встречаются редко. [94] По состоянию на июль 2010 года [обновлять]во всем мире было идентифицировано только 14 человек из пяти семей, несущих мутировавший ген ob (один из которых был первой когда-либо выявленной причиной генетического ожирения у людей) — две семьи пакистанского происхождения, живущие в Великобритании. , одна семья, живущая в Турции, одна в Египте и одна в Австрии [95] [96] [97] [98] [99] — и были обнаружены две другие семьи, несущие мутировавший ob- рецептор. [100] [101] У других людей был выявлен генетический частичный дефицит лептина, и у этих людей уровень лептина на нижней границе нормального диапазона может предсказать ожирение. [102]
Было также выявлено, что несколько мутаций генов, включающих меланокортины (используемые в передаче сигналов мозга, связанных с аппетитом) и их рецепторы , вызывают ожирение у большей части населения, чем мутации лептина. [103]
Жировая ткань имеет плотность ~0,9 г/мл. [104] Таким образом, человеку с большим количеством жировой ткани будет легче плавать, чем человеку того же веса с большим количеством мышечной ткани , поскольку плотность мышечной ткани составляет 1,06 г/мл. [105]
Измеритель жира в организме — это инструмент, используемый для измерения соотношения жира и веса в организме человека. В разных счетчиках используются разные методы определения соотношения. Они склонны недооценивать процентное содержание жира в организме.
В отличие от клинических инструментов, таких как DXA и подводное взвешивание , один относительно недорогой тип измерителя жира в организме использует принцип биоэлектрического импедансного анализа (BIA) для определения процентного содержания жира в организме человека. Для этого прибор пропускает небольшой, безвредный электрический ток через тело и измеряет сопротивление , а затем использует информацию о весе, росте, возрасте и поле человека для расчета приблизительного значения процентного содержания жира в организме человека. При расчете измеряется общий объем воды в организме (сухая ткань и мышцы содержат более высокий процент воды, чем жир) и на основе этой информации оценивается процент жира. Результат может колебаться на несколько процентных пунктов в зависимости от того, что было съедено и сколько воды выпито перед анализом. Этот метод быстрый и доступный, но неточный. Альтернативными методами являются: методы кожных складок с использованием штангенциркуля , подводное взвешивание , плетизмография с вытеснением воздуха всего тела (ADP) и DXA .
В жировой (жировой) ткани мышей с дефицитом CCR2 наблюдается повышенное количество эозинофилов , большая активация альтернативных макрофагов и склонность к экспрессии цитокинов 2 типа . Более того, этот эффект был преувеличен, когда мыши страдали ожирением из-за диеты с высоким содержанием жиров. [106]
Висцеральный жир представляет большую угрозу для здоровья, чем подкожный жир.
Эстроген вызывает накопление жира в области таза, бедер, ягодиц и бедер (область таза).