Зеленые серобактерии представляют собой тип Chlorobiota [4] облигатно анаэробных фотоавтотрофных бактерий , которые метаболизируют серу. [5]
Зеленые серные бактерии неподвижны (за исключением Chloroherpeton thalassium , который может скользить) и способны к аноксигенному фотосинтезу . [5] [6] Они живут в анаэробной водной среде. [7] В отличие от растений, зеленые серобактерии в качестве доноров электронов используют преимущественно сульфид-ионы. [8] Они являются автотрофами , которые используют обратный цикл трикарбоновых кислот для фиксации углерода . [9] Они также являются миксотрофами и восстанавливают азот. [10] [11]
Зеленые серобактерии представляют собой грамотрицательные палочковидные или шаровидные бактерии. Некоторые виды зеленых серобактерий имеют газовые вакуоли, обеспечивающие движение. Они являются фотолитоавтотрофами и используют энергию света и восстановленные соединения серы в качестве источника электронов. [12] Доноры электронов включают H 2 , H 2 S, S. Основным фотосинтетическим пигментом у этих бактерий являются бактериохлорофиллы c или d у зеленых видов и e у коричневых видов, которые расположены в хлоросомах и плазматических мембранах. [7] Хлоросомы обладают уникальной особенностью, которая позволяет им улавливать свет в условиях низкой освещенности. [13]
Большинство зеленых серобактерий мезофильны , предпочитают умеренные температуры и живут в водной среде. Они требуют анаэробных условий и пониженного содержания серы; они обычно находятся в верхних миллиметрах отложений. Они способны к фотосинтезу в условиях низкой освещенности. [7]
Было обнаружено, что в Черном море , чрезвычайно бескислородной среде, на глубине около 100 м обитает большая популяция зеленых серных бактерий. Из-за нехватки света в этом районе моря большинство бактерий были фотосинтетически неактивны. Фотосинтетическая активность, обнаруженная в сульфидном хемоклине, позволяет предположить, что бактериям требуется очень мало энергии для поддержания клеток. [14]
Вид зеленых серобактерий был обнаружен живущим рядом с черным курильщиком у побережья Мексики на глубине 2500 м в Тихом океане . На этой глубине бактерия, получившая обозначение GSB1, живет за счет тусклого свечения теплового источника, поскольку солнечный свет не может проникнуть на эту глубину. [15]
Зеленые серные бактерии также были обнаружены живущими на колониях коралловых рифов на Тайване. Они составляют большую часть «зеленого слоя» этих колоний. Вероятно, они играют роль в коралловой системе, и между бактериями и кораллом-хозяином могут существовать симбиотические отношения. [16] Коралл может обеспечить анаэробную среду и источник углерода для бактерий. Бактерии могут обеспечивать питательные вещества и очищать кораллы от токсинов, окисляя сульфид. [17]
В серных источниках был обнаружен один тип зеленых серобактерий, Chlorobaculum tepidum . Эти организмы термофильны , в отличие от большинства других зеленых серобактерий. [7]
Зеленые серобактерии относятся к семейству Chlorobiaceae. Есть четыре рода; Хлорогерпетон , Простекохлорис , Хлоробий и Хлоробакулум . Характеристики, используемые для различия этих родов, включают некоторые метаболические свойства, пигменты, морфологию клеток и спектры поглощения. Однако различить эти свойства сложно, поэтому таксономическое деление иногда неясно. [24]
Обычно хлоробии имеют палочковидную или вибровидную форму, а некоторые виды содержат газовые пузырьки. Они могут развиваться как одиночные или совокупные клетки. Они могут быть зелеными или темно-коричневыми. Зеленые штаммы используют фотосинтетические пигменты Bchl c или d с хлоробактеновыми каротиноидами, а коричневые штаммы используют фотосинтетический пигмент Bchl e с изорениратиновыми каротиноидами. Для роста требуется небольшое количество соли. [24]
Простекохлоры состоят из виброидных, яйцевидных или палочковидных клеток. Они начинаются с одиночных клеток, образующих неветвящиеся придатки, называемые неветвящимися протезами. Они также могут образовывать газовые пузырьки. Присутствующие фотосинтетические пигменты включают Bchl c, d или e. Кроме того, соль необходима для роста. [24]
Хлоробакулум развивается в виде одиночных клеток и обычно имеет виброидную или палочковидную форму. Некоторые из них могут образовывать газовые пузырьки. Фотосинтетические пигменты этого рода — Bchl c, d или e . Некоторым видам для роста требуется NaCl (хлорид натрия). Представители этого рода раньше входили в состав рода Chlorobium, но образовали отдельную линию. [24]
Род Chloroherpeton уникален, поскольку представители этого рода подвижны. Они представляют собой сгибающиеся длинные стержни и могут передвигаться, скользя. Они зеленого цвета и содержат фотосинтетический пигмент Bchl c , а также γ-каротин . Соль необходима для роста. [24]
Зеленые серобактерии используют для фотосинтеза реакционный центр типа I. Реакционные центры типа I являются бактериальным гомологом фотосистемы I (PSI) у растений и цианобактерий . Реакционные центры GSB содержат бактериохлорофилл а и известны как реакционные центры P840 из-за длины волны возбуждения 840 нм, которая обеспечивает поток электронов. У зеленых серобактерий реакционный центр связан с большим комплексом антенн, называемым хлоросомой , который захватывает и направляет световую энергию в реакционный центр. Хлоросомы имеют пик поглощения в дальней красной области спектра между 720 и 750 нм, поскольку они содержат бактериохлорофиллы c, d и e. [25] Белковый комплекс, называемый комплексом Фенны-Мэтьюза-Олсона (FMO), физически расположен между хлоросомами и RC P840. Комплекс ФМО помогает эффективно передавать поглощенную антенной энергию в реакционный центр.
Реакционные центры PSI и типа I способны восстанавливать ферредоксин (Fd), сильный восстановитель, который можно использовать для фиксации CO.
2и уменьшить НАД + . Как только реакционный центр (RC) отдал электрон Fd, он становится окислителем (P840 + ) с восстановительным потенциалом около +300 мВ. Хотя этого недостаточно, чтобы отобрать электроны у воды и синтезировать O.
2( Э
0= +820 мВ), он может принимать электроны из других источников, таких как H
2S , тиосульфат или Fe2+
ионы. [26] Этот транспорт электронов от доноров, таких как H
2S к акцептору Fd называется линейным потоком электронов или линейным транспортом электронов. Окисление сульфид-ионов приводит к образованию серы в качестве побочного продукта, который накапливается в виде глобул на внеклеточной стороне мембраны. Эти шарики серы дали название зеленым серным бактериям. Когда сульфид истощается, шарики серы расходуются и далее окисляются до сульфата. Однако путь окисления серы недостаточно изучен. [8]
Вместо передачи электронов на Fd кластеры Fe-S в реакционном центре P840 могут передавать электроны менахинону ( MQ: MQH
2), который возвращает электроны в P840 + через цепь переноса электронов (ETC). На обратном пути в РЦ электроны от MQH2 проходят через комплекс цитохрома bc 1 (аналогичный комплексу III митохондрий), который перекачивает H+
ионы через мембрану. Электрохимический потенциал протонов через мембрану используется для синтеза АТФ с помощью АТФ-синтазы F o F 1 . Этот циклический транспорт электронов отвечает за преобразование энергии света в клеточную энергию в форме АТФ. [25]
Зеленые серные бактерии окисляют неорганические соединения серы, чтобы использовать их в качестве доноров электронов для анаэробного фотосинтеза, в частности, для фиксации углекислого газа. В качестве донора электронов они обычно предпочитают использовать сульфид, а не другие соединения серы, однако они могут использовать тиосульфат или H 2 . [27] Промежуточным продуктом обычно является сера, которая откладывается вне клетки, [28] а конечным продуктом является сульфат. Сера, откладывающаяся внеклеточно, имеет форму серных глобул, которые впоследствии могут быть полностью окислены. [27]
Механизмы окисления серы у зеленых серобактерий изучены недостаточно. Некоторые ферменты, которые, как полагают, участвуют в окислении сульфидов, включают флавоцитохром с, сульфид: хинон оксидоредуктазу и SO.
Икссистема. Флавоцитохром может катализировать перенос электронов на цитохромы из сульфида, и эти цитохромы могут затем перемещать электроны в реакционный центр фотосинтеза. Однако не все зеленые серобактерии производят этот фермент, что свидетельствует о том, что он не необходим для окисления сульфида. Сульфид:хиноноксидоредуктаза (SQR) также способствует транспорту электронов, но, как было обнаружено, она снижает скорость окисления сульфидов у зеленых серных бактерий, что позволяет предположить, что существует другой, более эффективный механизм. [27] Однако большинство зеленых серных бактерий содержат гомолог гена SQR. [29] Окисление тиосульфата до сульфата может катализироваться ферментами SO .
Икссистема. [27]
Считается, что ферменты и гены, связанные с метаболизмом серы, были получены путем горизонтального переноса генов в ходе эволюции зеленых серобактерий. [29]
Зеленые серные бактерии являются фотоавтотрофами : они не только получают энергию от света, но и могут расти, используя углекислый газ в качестве единственного источника углерода. Они фиксируют углекислый газ, используя обратный цикл трикарбоновых кислот (rTCA) [9] , где энергия расходуется на восстановление углекислого газа, а не на окисление, как это видно в прямом цикле TCA , [9] для синтеза пирувата и ацетата . Эти молекулы используются в качестве сырья для синтеза всех строительных блоков, необходимых клетке для создания макромолекул . Цикл rTCA очень энергоэффективен, позволяя бактериям расти в условиях низкой освещенности. [30] Однако он содержит несколько чувствительных к кислороду ферментов, что ограничивает его эффективность в аэробных условиях. [30]
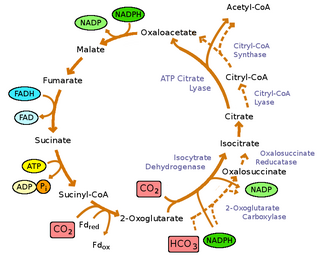
Реакции обращения окислительного цикла трикарбоновых кислот катализируются четырьмя ферментами: [9]
Однако окислительный цикл ТСА (ОТЦА) все еще присутствует у зеленых серобактерий. OTCA может ассимилировать ацетат, однако OTCA, по-видимому, является неполным у зеленых серных бактерий из-за расположения и подавления гена во время фототрофного роста. [9]
Зеленые серные бактерии часто называют облигатными фотоавтотрофами, поскольку они не могут расти в отсутствие света, даже если им обеспечены органические вещества. [9] [26] Однако они проявляют форму миксотрофии , при которой они могут потреблять простые органические соединения в присутствии света и CO 2 . [9] В присутствии CO 2 или HCO 3 - некоторые зеленые серобактерии могут использовать ацетат или пируват. [9]
Миксотрофию зеленых серобактерий лучше всего моделирует представительная зеленая серная бактерия Chlorobaculum tepidum . [31] Миксотрофия возникает во время биосинтеза аминокислот/утилизации углерода и энергетического метаболизма. [32] Бактерия использует электроны, образующиеся в результате окисления серы, и энергию, которую она захватывает из света, для запуска rTCA. C. tepidum также демонстрирует использование пирувата и ацетата в качестве источника органического углерода. [32]
Примером миксотрофии C. tepidum , сочетающей в себе автотрофию и гетеротрофию , является синтез ацетил-КоА. C. tepidum может автотрофно генерировать ацетил-КоА посредством цикла rTCA или гетеротрофно генерировать его за счет поглощения ацетата. Аналогичная миксотрофная активность возникает, когда пируват используется для биосинтеза аминокислот, но миксотрофный рост с использованием ацетата дает более высокие скорости роста. [31] [32]
В энергетическом метаболизме C. tepidum полагается на световые реакции для производства энергии (НАДФН и НАДН), поскольку пути, обычно отвечающие за производство энергии (окислительный пентозофосфатный путь и нормальный цикл ТСА), функционируют лишь частично. [32] Фотоны, поглощаемые светом, используются для производства НАДФН и НАДН, кофакторов энергетического метаболизма. C. tepidum также генерирует энергию в форме АТФ, используя движущую силу протонов, образующуюся в результате окисления сульфида. [31] Производство энергии как за счет окисления сульфидов, так и за счет поглощения фотонов бактериохлорофиллами . [32]
Большинство зеленых серобактерий являются диазотрофами : они способны восстанавливать азот до аммиака, который затем используется для синтеза аминокислот. [33] Фиксация азота среди зеленых серобактерий обычно типична для аноксигенных фототрофов и требует присутствия света. Зеленые серные бактерии проявляют активность системы секреции типа 1 и ферредоксин-НАДФ+ оксидоредуктазы, производя восстановленное железо - признак, который развился для поддержки фиксации азота. [34] Подобно пурпурным серным бактериям, они могут регулировать активность нитрогеназы посттрансляционно в ответ на концентрацию аммиака. Наличие у них генов nif , даже несмотря на то, что они эволюционно различны, может свидетельствовать о том, что их способности к фиксации азота возникли в результате двух разных событий или от общего очень далекого предка. [33]
Примеры зеленых серобактерий, способных к фиксации азота, включают род Chlorobium и Pelodictyon , за исключением P. phaeoclathratiforme . Prosthecochromis aestuarii и Chloroherpeton thalassium также попадают в эту категорию. [33] Их фиксация N 2 широко распространена и играет важную роль в общей доступности азота для экосистем. Зеленые серные бактерии, живущие в коралловых рифах, такие как Prosthecochromis , играют решающую роль в производстве доступного азота в и без того ограниченной среде. [16]