
Карбокатион — это ион с положительно заряженным атомом углерода . Среди простейших примеров — метений CH +
3, метан CH+
5, ацилий-ионы RCO + и винил C
2ЧАС+
3катионы. [2]
До начала 1970-х годов карбокатионы назывались ионами карбония . [3] В современном определении, данном ИЮПАК, карбокатион — это любой четный электрон-катион со значительным частичным положительным зарядом на атоме углерода. Они далее классифицируются на две основные категории в соответствии с координационным числом заряженного углерода: три в ионах карбония и пять в ионах карбония . Эта номенклатура была предложена GA Olah . [4] Ионы карбония, как первоначально было определено Olah, характеризуются трехцентровой двухэлектронной делокализованной схемой связи и по существу являются синонимами так называемых « неклассических карбокатионов », которые представляют собой карбокатионы, содержащие мостиковые C–C или C–H σ-связи. Однако другие более узко определили термин «ион карбония» как формально протонированные или алкилированные алканы ( CR+
5, где R — H или алкил), за исключением неклассических карбокатионов, таких как 2-норборнил-катион . [5]
Согласно ИЮПАК , карбокатион — это любой катион, содержащий четное число электронов, в котором значительная часть положительного заряда находится на атоме углерода. [6] До наблюдения пятикоординированных карбокатионов Олахом и его коллегами, карбокатион и ион карбония использовались взаимозаменяемо. Олах предложил переопределение иона карбония как карбокатиона, характеризующегося любым типом трехцентровой двухэлектронной связи, в то время как ион карбения был недавно придуман для обозначения карбокатиона, содержащего только двухцентровые двухэлектронные связи с трехкоординированным положительным углеродом. Впоследствии другие использовали термин ион карбония более узко для обозначения видов, которые получены (по крайней мере формально) из электрофильной атаки H + или R + на алкан, по аналогии с другими основными ониевыми видами группы, в то время как карбокатион, который содержит любой тип трехцентровой связи, называется неклассическим карбокатионом . В этом использовании 2-норборнил катион не является ионом карбония, поскольку формально он получен протонированием алкена (норборнена), а не алкана, хотя это неклассический карбокатион из-за его мостиковой структуры. ИЮПАК признает три расходящихся определения иона карбония и призывает к осторожности при использовании этого термина. В оставшейся части этой статьи термин ион карбония будет использоваться в этом последнем ограниченном смысле, в то время как неклассический карбокатион будет использоваться для обозначения любого карбокатиона с σ-связями C–C и/или C–H, делокализованными мостиковой связью.

Ионы карбония можно рассматривать как протонированные или алкилированные алканы. Они характеризуются делокализованными связями 3c-2e. По этой причине их часто называют неклассическими ионами. Хорошо изученным примером, хотя и не имеющим практической ценности, является катион 2-норборнила . Подобно ионам карбения, ионы карбония часто используются в качестве промежуточных продуктов при модернизации углеводородов на нефтеперерабатывающих заводах.
По крайней мере, в формальном смысле, ионы карбения получаются из протонирования (присоединения H + ) или алкилирования (присоединения R + ) карбена или алкена . Таким образом, по крайней мере в одном из их резонансных изображений они обладают атомом углерода, несущим формальный положительный заряд, который окружен секстетом электронов (шесть валентных электронов ) вместо обычного октета, необходимого для заполнения валентной оболочки углерода ( правило октета ). Поэтому ионы карбения (и карбокатионы в целом) часто являются реактивными, стремясь заполнить октет валентных электронов, а также восстановить нейтральный заряд . В соответствии с VSEPR и правилом Бента , если геометрически не ограничено пирамидальной формой (например, катион 1-адамантил), 3-координированный углерод в ионах карбения обычно является тригональным плоским, с чистой p-символикой пустой орбитали в качестве его самой низкой незанятой молекулярной орбитали (LUMO) и связями CH/CC, образованными из орбиталей C(sp 2 ). Прототипическим примером является метильный катион CH+3.
История карбокатионов восходит к 1891 году, когда Г. Мерлинг [8] сообщил, что он добавил бром к тропилидену ( циклогептатриену ), а затем нагрел продукт, чтобы получить кристаллический, растворимый в воде материал, C
7ЧАС
7Br . Он не предложил структуру для него; однако, Деринг и Нокс [9] убедительно показали, что это был тропилий (циклогептатриенилий) бромид. Этот ион предсказывается как ароматический по правилу Хюккеля .
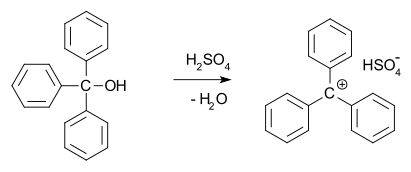
В 1902 году Норрис и Керман независимо друг от друга открыли, что бесцветный трифенилметанол дает темно-желтые растворы в концентрированной серной кислоте . Трифенилметилхлорид также образовывал оранжевые комплексы при обработке хлоридами алюминия и олова. В 1902 году Адольф фон Байер распознал солеподобный характер образующихся соединений. Он назвал связь между цветом и образованием соли галохромией , ярким примером которой является малахитовый зеленый . Тритилкарбокатион (показан ниже) действительно является стабильной карбокатионной системой, например, в форме тритилгексафторфосфата . [10]
Карбокатионы являются реакционноспособными промежуточными продуктами во многих органических реакциях. Эта идея, впервые предложенная Юлиусом Штиглицем в 1899 году [11], была далее развита Гансом Меервейном в его исследовании 1922 года [12] [13] перегруппировки Вагнера-Меервейна . Было также обнаружено, что карбокатионы участвуют в реакции S N 1 , реакции E1 и в реакциях перегруппировки, таких как сдвиг Уитмора 1,2 . Химическое сообщество неохотно принимало понятие карбокатиона, и в течение долгого времени Журнал Американского химического общества отклонял статьи, в которых они упоминались.
Спектр ЯМР карбокатиона был впервые получен Дерингом и др. [14] в 1958 году . Это был ион гептаметилбензола , полученный обработкой гексаметилбензола метилхлоридом и хлоридом алюминия . Стабильный катион 7-норборнадиенил был получен Стори и др. в 1960 году [15] путем реакции норборнадиенилхлорида с тетрафторборатом серебра в диоксиде серы при -80 °C. Спектр ЯМР установил, что он неклассически мостиковый (первый стабильный неклассический наблюдаемый ион).
В 1962 году Олах непосредственно наблюдал трет -бутиловый карбокатион с помощью ядерного магнитного резонанса как стабильный вид при растворении трет -бутилфторида в магической кислоте . Спектр ЯМР норборнилового катиона был опубликован Шлейером и др. [16]. Было показано, что он быстро подвергается скремблированию протонов. [17]