Карбоангидразы (или карбонатдегидратазы ) ( EC 4.2.1.1) образуют семейство ферментов , которые катализируют взаимопревращение между углекислым газом и водой и диссоциированными ионами угольной кислоты (т. е. бикарбонатом и ионами водорода ). [1] Активный центр большинства карбоангидраз содержит ион цинка . Поэтому их классифицируют как металлоферменты . Фермент поддерживает кислотно-щелочной баланс и помогает транспортировать углекислый газ. [2]
Карбоангидраза помогает поддерживать кислотно-щелочной гомеостаз , регулировать pH и баланс жидкости. В зависимости от его расположения роль фермента немного меняется. Например, карбоангидраза вырабатывает кислоту в слизистой оболочке желудка. В почках контроль ионов бикарбоната влияет на содержание воды в клетке. Контроль ионов бикарбоната также влияет на содержание воды в глазах. Ингибиторы карбоангидразы используются для лечения глаукомы, чрезмерного накопления воды в глазах. Блокирование этого фермента изменяет баланс жидкости в глазах, уменьшая накопление жидкости, тем самым снимая давление. [2] [3]
Карбоангидраза имеет решающее значение для функции гемоглобина через эффект Бора , который катализирует гидратацию углекислого газа с образованием угольной кислоты и быстрой диссоциацией на воду. [4] По сути, увеличение углекислого газа приводит к снижению pH крови, что снижает связывание кислорода с гемоглобином . [5] Обратное верно, когда снижение концентрации углекислого газа повышает pH крови, что увеличивает скорость связывания кислорода с гемоглобином. Связь эффекта Бора с карбоангидразой проста: карбоангидраза ускоряет реакцию углекислого газа, реагирующего с водой, с образованием ионов водорода (протонов) и ионов бикарбоната.
Для описания равновесия в реакции карбоангидразы используется принцип Ле Шателье . Большинство тканей более кислые, чем легочная ткань, поскольку углекислый газ вырабатывается клеточным дыханием в этих тканях, где он реагирует с водой, образуя протоны и бикарбонат. Поскольку концентрация углекислого газа выше, равновесие смещается вправо, в сторону бикарбоната. Противоположная ситуация наблюдается в легких, где выделяется углекислый газ, что снижает его концентрацию, поэтому равновесие смещается влево, благоприятствуя выработке углекислого газа. [6]
Карбоангидраза была первоначально выделена и охарактеризована из эритроцитов в 1933 году, с одновременными отчетами Мелдрума и Раутона (в Кембриджском университете в Соединенном Королевстве) и Стэди и О'Брайена (в Пенсильванском университете в Соединенных Штатах), [7] [8] оба искали «каталитический фактор... необходимый для быстрого транзита HCO3- [ бикарбонат-аниона] из эритроцита в... легочные капилляры ». [9]
Карбоангидраза играет важную роль в регуляции pH крови, что ускоряет реакцию CO 2 + H 2 O HCO 3 - + H + для обеспечения быстрого поддержания равновесия. На равновесную реакцию влияет соотношение бикарбоната и H + к углекислому газу. [10] HCO 3 - представляет собой сопряженное основание, которое нейтрализует кислоты, а H + представляет собой сопряженную кислоту, которая нейтрализует основания с помощью кислотно-щелочного гомеостаза . HCO 3 - и H + идеально подходят для буферизации pH в крови и тканях, поскольку pKa близок к физиологическому pH = 7,2–7,6. Поскольку HCO 3 - и H + регулируются в почках, а углекислый газ плазмы регулируется в легких, оба действия в почках и легких важны для поддержания стабильности pH крови. Поэтому карбоангидраза помогает с секрецией H + в просвет почечных канальцев почек и реабсорбцией HCO 3 - в почках. Кроме того, он помогает транспортировать углекислый газ из легочной ткани в альвеолы легочных капилляров, откуда углекислый газ будет выводиться во время выдоха. [10]
Карбоангидраза — очень древний фермент, обнаруженный в обоих доменах прокариот, который существует в шести различных классах среди большинства живых организмов. [11] Эти семейства не похожи по последовательности или структуре, поскольку они эволюционировали независимо друг от друга, но все они развили одну и ту же структуру активного центра Zn 2+ , демонстрируя прекрасный пример конвергентной эволюции. [ необходима цитата ]
Фермент — это вещество, которое действует как катализатор в живых организмах, помогая ускорить химические реакции. [12] Карбоангидраза — один из важных ферментов, который содержится в эритроцитах, слизистой оболочке желудка, клетках поджелудочной железы и даже почечных канальцах. Он был открыт в 1932 году и был разделен на три основных класса. [13] Первый класс — альфа-карбоангидраза, которая содержится в млекопитающих, второй класс — бета-карбоангидраза, которая содержится в бактериях и растениях, и, наконец, третий класс — гамма-карбоангидраза, которая содержится в метаногенных бактериях в горячих источниках. [14] Все три класса карбоангидразы имеют один и тот же активный центр с металлическим центром Zn; однако они структурно не похожи друг на друга. Основная роль карбоангидразы у людей — катализировать превращение углекислого газа в угольную кислоту и обратно. Однако она также может помогать с транспортировкой CO2 в крови, что, в свою очередь, помогает дыханию. Он даже может участвовать в образовании соляной кислоты в желудке. [Необходима ссылка] Поэтому роль карбоангидразы зависит от того, где она находится в организме.
В CA II млекопитающих активный центр состоит из следующих элементов: атом металла Zn +2, представляющий собой жесткую кислоту Льюиса, координированный с остатками His -94, -96 и -119 на расстоянии 109˚ друг от друга, и гидроксид-ион (pKa = 6,8; 120° в конфигурации T d ) , гидрофобный карман, прилегающий к связанному с цинком гидроксиду, состоящий из Val-143 у его основания и Val-121, Trp-209 и Leu-198 у его шейки, остаток переноса протонов (PSR) His-64 H + перемещает H + в активный центр и из него посредством конформационного переключения, и сеть водородных связей, состоящая из гидроксильной группы Thr-199 и карбоксильной группы Glu-106, которая стабилизирует связанный с цинком гидроксид, способствуя ориентации молекул воды на активной стороне в определенной геометрической конфигурации. CA II имеет частоту оборота 10 6 с −1 , что составляет В 107 раз быстрее, чем некатализированная реакция.

Реакция, которая показывает катализ карбоангидразы в наших тканях, это
Катализацию карбоангидразы в легких можно увидеть на рисунке
Причина противоположных направлений реакций в тканях и легких заключается в разных уровнях pH, которые в них обнаружены. Без катализатора карбоангидразы реакция идет очень медленно, однако с катализатором реакция идет в 10 7 раз быстрее.
Реакция, катализируемая карбоангидразой,
Угольная кислота имеет pKa около 6,36 (точное значение зависит от среды), поэтому при pH 7 небольшой процент бикарбоната протонируется.
Карбоангидраза является одним из самых быстрых ферментов, и ее скорость обычно ограничена скоростью диффузии ее субстратов . Типичные каталитические скорости различных форм этого фермента варьируются от 10 4 до 10 6 реакций в секунду. [15]
Некатализируемая обратная реакция относительно медленная (кинетика в диапазоне 15 секунд). Вот почему газированный напиток не дегазируется мгновенно при открытии контейнера; однако он быстро дегазируется во рту при контакте с карбоангидразой, содержащейся в слюне. [16]
Ангидраза определяется как фермент, катализирующий удаление молекулы воды из соединения, и именно эта «обратная» реакция дала название карбоангидразе, поскольку она удаляет молекулу воды из угольной кислоты.
В легких карбоангидраза преобразует бикарбонат в углекислый газ, пригодный для выдоха.
.jpg/440px-Active_site_of_CAII_(cropped).jpg)
Углекислый газ транспортируется в крови в трех формах:
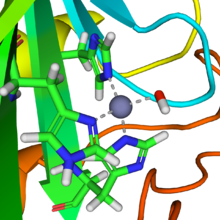

Простетическая группа цинка в ферменте координируется в трех положениях боковыми цепями гистидина . Четвертое координационное положение занимает вода . Четвертый гистидин находится близко к водному лиганду, что облегчает образование центра Zn-OH, который связывает CO2 с образованием бикарбоната цинка. [18] Конструкция является примером общего кислотно-основного катализа (см. статью « Кислотный катализ »). Активный центр также имеет карман, подходящий для диоксида углерода, что приближает его к гидроксидной группе. Проведенные кинетические исследования определяют следующий механизм для фермента: на этапе 1 и 2 нуклеофил O− на гидроксидном ионе, координированном с Zn2 +, осуществляет нуклеофильную атаку на частично электрофильный углерод на молекуле CO2 . Здесь Zn 2+ действует как кислота Льюиса, которая снижает pK a координированного лиганда OH 2 с ~7-8 до 6,8 в качестве T d , что приводит к депротонированию воды до гидроксид-иона, а свободный протон нейтрализуется окружающим буфером. На этапе 3) происходит перенос протона (H + ) от OH −1 к некоординированному O − в CO 3 −2, координированному с атомом Zn +2 в активном центре. Затем высвобождается ион бикарбоната, и каталитический центр регенерируется посредством связывания другой молекулы воды в обмен на ион бикарбоната. На этапе 4) координированный лиганд воды депротонируется при содействии Zn +2 , чтобы генерировать другой гидроксид-ион, чтобы начать цикл заново. [19] [20]

Признано по крайней мере пять различных семейств CA: α, β, γ, δ и ζ. Эти семейства не имеют значительного сходства аминокислотных последовательностей и в большинстве случаев считаются примером конвергентной эволюции . α-CA обнаружены у людей.
Эукариотные организмы, включая позвоночных , водоросли , растения и грибы , а также некоторые бактерии, содержат это семейство КА.
Ферменты КА, обнаруженные у млекопитающих, делятся на четыре обширные подгруппы, [ необходима ссылка ], которые, в свою очередь, состоят из нескольких гомологичных классов генов:
Существуют три дополнительные «акаталитические» изоформы человеческой карбоангидразы ( CA-VIII , CA-X и CA-XI ) ( CA8 , CA10 , CA11 ), функции которых остаются неясными. [21]

Большинство прокариотических и растительных хлоропластных КА принадлежат к семейству бета. Для этого семейства были идентифицированы два образца подписи :
Гамма-класс КА происходит от метаногенов — архей, вырабатывающих метан и растущих в горячих источниках.
Класс дельта-КА был описан у диатомовых водорослей . Однако недавно [27] различие этого класса КА было поставлено под сомнение.
Класс дзета-КА встречается исключительно в бактериях, в нескольких хемолитотрофах и морских цианобактериях , которые содержат cso- карбоксисомы . [28] Недавние трехмерные анализы [27] показывают, что ζ-КА имеет некоторое структурное сходство с β-КА, особенно вблизи участка иона металла. Таким образом, эти две формы могут быть отдаленно связаны, хотя базовая аминокислотная последовательность с тех пор значительно разошлась.
Семейство эта-КА было недавно обнаружено в организмах рода Plasmodium . Это группа ферментов, которые ранее считались принадлежащими к альфа-семейству КА, однако было показано, что η-КА обладают уникальными особенностями, такими как их схема координации ионов металлов. [29]
Класс йота является самым последним описанным классом КА. Он был обнаружен в морской диатомовой водоросли Thalassiosira pseudonana и широко распространен среди морского фитопланктона. [30] У диатомовых водорослей ι-КА необходима для механизмов концентрации CO 2 и, в отличие от других классов КА, может использовать марганец вместо цинка в качестве металлического кофактора. [30] Гомологи ι-КА также были подтверждены у грамотрицательных бактерий, где они могут присутствовать в виде белкового гомодимера. [31]
В природе встречаются несколько форм карбоангидразы. В наиболее изученной форме α-карбоангидразы, присутствующей в животных, ион цинка координируется имидазольными кольцами 3 остатков гистидина , His94, His96 и His119. [32]
Основная функция фермента у животных — взаимопревращение углекислого газа и бикарбоната для поддержания кислотно-щелочного баланса в крови и других тканях, а также помощь в транспортировке углекислого газа из тканей.
У млекопитающих существует не менее 14 различных изоформ. Растения содержат другую форму, называемую β-карбоангидраза , которая с эволюционной точки зрения является отдельным ферментом, но участвует в той же реакции и также использует ион цинка в своем активном центре. У растений карбоангидраза помогает повысить концентрацию CO2 в хлоропласте , чтобы увеличить скорость карбоксилирования фермента RuBisCO . Это реакция, которая интегрирует CO2 в органические углеродные сахара во время фотосинтеза и может использовать только форму углерода CO2, а не угольную кислоту или бикарбонат. [ необходима цитата ]
Было обнаружено, что морские диатомовые водоросли экспрессируют новую форму ζ-карбоангидразы. Было обнаружено, что T. weissflogii , вид фитопланктона, распространенный во многих морских экосистемах, содержит карбоангидразу с ионом кадмия вместо цинка. [33] Ранее считалось, что кадмий является токсичным металлом, не имеющим никакой биологической функции. Однако этот вид фитопланктона, по-видимому, приспособился к низкому уровню цинка в океане, используя кадмий, когда цинка недостаточно. [34] Хотя концентрация кадмия в морской воде также низкая (около 1x10−16 моль ) , есть экологическое преимущество в возможности использовать любой металл в зависимости от того, какой из них более доступен в данный момент. Таким образом, этот тип карбоангидразы является камбиалистическим, то есть он может заменять металл в своем активном центре другими металлами (а именно, цинком и кадмием). [35]
Механизм действия кадмиевой карбоангидразы (CDCA) по сути такой же, как и у других карбоангидраз, в процессе превращения углекислого газа и воды в бикарбонат и протон. [36] Кроме того, как и другие карбоангидразы, CDCA заставляет реакцию протекать почти так же быстро, как и скорость диффузии ее субстратов, и ее можно ингибировать производными сульфонамида и сульфамата . [36]
В отличие от большинства других карбоангидраз, ион металла активного центра не связан тремя остатками гистидина и гидроксид-ионом. Вместо этого он связан двумя остатками цистеина , одним остатком гистидина и гидроксид-ионом, что характерно для β-CA. [36] [37] В связи с тем, что кадмий является мягкой кислотой , он будет более прочно связан с мягкими основными лигандами. [35] Атомы серы на остатках цистеина являются мягкими основаниями, таким образом, связывая кадмий более прочно, чем азот на остатках гистидина. CDCA также имеет трехмерную складчатую структуру, которая не похожа ни на одну другую карбоангидразу, и ее аминокислотная последовательность отличается от других карбоангидраз. [36] Это мономер с тремя доменами, каждый из которых идентичен по аминокислотной последовательности и каждый из которых содержит активный центр с ионом металла. [37]
Еще одно ключевое отличие CDCA от других карбоангидраз заключается в том, что CDCA имеет механизм переключения своего иона кадмия на ион цинка в случае, если цинк становится более доступным для фитопланктона, чем кадмий. Активный центр CDCA по сути «закрыт» цепочкой из девяти аминокислот с остатками глицина в положениях 1 и 9. Обычно эти ворота остаются закрытыми, а ион кадмия удерживается внутри. Однако из-за гибкости и положения остатков глицина эти ворота могут быть открыты для удаления иона кадмия. Затем на его место можно поместить ион цинка, и ворота закроются за ним. [36] Как пограничная кислота , цинк не будет связываться с лигандами цистеина так же прочно, как кадмий, но фермент все равно будет активным и достаточно эффективным. Металл в активном центре может переключаться между цинком и кадмием в зависимости от того, какой из них более распространен в данный момент. Вероятно, именно способность CDCA использовать кадмий или цинк дает T. weissflogii преимущество в выживании. [34]
Кадмий по-прежнему считается смертельным для фитопланктона в больших количествах. Исследования показали, что T. weissflogii имеет начальную токсическую реакцию на кадмий при его воздействии. Токсичность металла снижается за счет транскрипции и трансляции фитохелатина , которые являются белками, способными связывать и транспортировать кадмий. После связывания фитохелатином кадмий больше не является токсичным, и его можно безопасно транспортировать к ферменту CDCA. [33] Также было показано, что поглощение кадмия через фитохелатин приводит к значительному увеличению экспрессии CDCA. [33]
Другие виды фитопланктона из разных источников воды были проверены на наличие CDCA. Было обнаружено, что многие из них содержат белки, гомологичные CDCA, обнаруженному в T. weissflogii . [33] Сюда входят виды из залива Грейт-Бей, Нью-Джерси , а также из Тихого океана вблизи экватора . У всех протестированных видов CDCA-подобные белки показали высокий уровень экспрессии даже при высоких концентрациях цинка и в отсутствие кадмия. [33] Сходство между этими белками и CDCA, экспрессируемым T. weissflogii, варьировалось, но они всегда были похожи по крайней мере на 67%. [33]
Карбоангидраза в принципе может оказаться релевантной для улавливания углерода . Некоторые карбоангидразы могут выдерживать температуры до 107 °C и экстремальную щелочность (pH > 10). [38] Пилотный запуск с более стабильной CA на дымовом потоке, который состоял из 12–13% молярного состава CO₂, имел скорость улавливания 63,6% в течение 60-часового периода без заметных эффектов в производительности фермента. CA была помещена в раствор N-метилдиэтаноламина (MDEA), где она служила для увеличения разницы концентраций (движущей силы) CO2 между дымовым потоком электростанции и жидкой фазой в жидкостно-газовом контакторе. [38]