.jpg/440px-GFAJ-1_(grown_on_arsenic).jpg)
GFAJ- 1 — штамм палочковидных бактерий семейства Halomonadaceae . Это экстремофил , который был выделен из гиперсоленого и щелочного озера Моно в восточной Калифорнии геобиологом Фелисой Вулф-Саймон , научным сотрудником НАСА, проживающей в Геологической службе США . В публикации журнала Science за 2010 год [1] авторы заявили, что микроб, когда ему не хватает фосфора , способен замещать мышьяком небольшой процент своего фосфора для поддержания своего роста. [2] [3] Сразу после публикации другие микробиологи и биохимики выразили сомнение по поводу этого утверждения, которое подверглось резкой критике в научном сообществе. Последующие независимые исследования, опубликованные в 2012 году, не обнаружили обнаруживаемого арсената в ДНК GFAJ-1, опровергли это утверждение и продемонстрировали, что GFAJ-1 представляет собой просто устойчивый к арсенату и фосфат-зависимый организм. [4] [5] [6] [7]

Бактерия GFAJ-1 была обнаружена геомикробиологом Фелисой Вулф-Саймон , научным сотрудником НАСА по астробиологии , проживающей в Геологической службе США в Менло-Парке, Калифорния . [8] GFAJ означает «Дайте Фелизе работу». [9] Организм был изолирован и культивирован начиная с 2009 года из образцов, которые она и ее коллеги собрали из отложений на дне озера Моно , Калифорния, США. [10] Озеро Моно является гиперсоленым (около 90 граммов на литр) и сильно щелочным ( рН) . 9.8). [11] Он также имеет одну из самых высоких природных концентраций мышьяка в мире (200 мкМ ) . [1] Открытие получило широкую огласку 2 декабря 2010 года. [2]
Молекулярный анализ, основанный на последовательностях 16S рРНК , показывает, что GFAJ-1 тесно связан с другими умеренно галофильными («солелюбивыми») бактериями семейства Halomonadaceae . Хотя авторы составили кладограмму , на которой штамм гнездится среди представителей Halomonas , включая H.alaliphila и H.venusta , [12] они не отнесли штамм явно к этому роду. [1] [10] Известно, что многие бактерии способны переносить высокие уровни мышьяка и склонны поглощать его в свои клетки. [1] [13] Однако GFAJ-1 было неоднозначно предложено пойти еще дальше; при нехватке фосфора было предложено вместо этого включить мышьяк в его метаболиты и макромолекулы и продолжить рост. [10]
Последовательность генома бактерии GFAJ-1 теперь размещена в GenBank . [14]

В статье журнала Science GFAJ-1 упоминается как штамм Halomonadaceae, а не как новый вид . [1] Международный кодекс номенклатуры бактерий , свод правил, регулирующих таксономию бактерий, а также некоторые статьи в Международном журнале систематической и эволюционной микробиологии содержат руководящие принципы и минимальные стандарты для описания новых видов, например минимальные стандарты. описать представителя семейства Halomonadaceae . [15] Организмы описываются как новые виды, если они соответствуют определенным физиологическим и генетическим условиям, таким как, как правило, менее 97% идентичности последовательности 16S рРНК с другими известными видами [16] и метаболические различия, позволяющие их различать. Помимо индикаторов, позволяющих отличить новый вид от других видов, необходимы другие анализы, такие как состав жирных кислот , используемый респираторный хинон, диапазоны толерантности и хранение штамма как минимум в двух микробиологических репозиториях. Новые предложенные названия выделены курсивом, после чего следует sp. ноябрь (и gen. nov. , если это новый род согласно описаниям этой клады ). [17] [18]
В случае штамма GFAJ-1 эти критерии не выполняются, и этот штамм не заявлен как новый вид. [1] Когда штамм не отнесен к виду (например, из-за недостаточности данных или выбора), его часто обозначают названием рода, за которым следует «sp». (т. е. неопределенные виды этого рода) и название штамма. В случае GFAJ-1 авторы решили ссылаться на штамм только по его обозначению. Штаммы, тесно связанные с GFAJ-1, включают Halomonas sp. GTW и Halomonas sp. G27, ни один из которых не был описан как действительный вид. [19] [20] Если бы авторы формально отнесли штамм GFAJ-1 к роду Halomonas , [10] название было бы дано как Halomonas sp. ГФАЖ-1.
База данных геномной таксономии относит GFAJ-1 к собственному экспериментальному виду, Halomonas sp002966495 . Это означает, что филогенетически штамм относится к Halomonas , а его полногеномное сходство по сравнению с другими определенными видами рода достаточно низкое. Ни штамм GTW, ни штамм G27 не имеют генома, доступного в базе данных для его классификации. [21]
Для культивирования бактерий в режиме возрастающего воздействия арсената использовали бесфосфорную питательную среду (которая фактически содержала 3,1 ± 0,3 мкМ остаточного фосфата от примесей в реагентах ) ; первоначальный уровень 0,1 мМ в конечном итоге был повышен до 40 мМ. Альтернативные среды, использованные для сравнительных экспериментов, содержали либо высокие уровни фосфата (1,5 мМ) без арсената, либо не добавляли ни фосфат, ни арсенат. Было замечено, что GFAJ-1 мог расти за счет многократного удвоения числа клеток при культивировании в фосфатной или арсенатной среде, но не мог расти при помещении в среду аналогичного состава, к которой не добавлялись ни фосфат, ни арсенат. [1] Содержание фосфора в бактериях, получавших мышьяк и испытывающих недостаток фосфора (по измерениям с помощью ICP-MS), составляло всего 0,019 (± 0,001) % по сухому весу, что составляет одну тридцатую от этого показателя при выращивании в богатой фосфатами среде. Это содержание фосфора также составляло лишь около одной десятой от среднего содержания мышьяка в клетках (0,19 ± 0,25% по сухому весу). [1] Содержание мышьяка в клетках, измеренное методом ИСП-МС, варьируется в широких пределах и может быть ниже содержания фосфора в одних экспериментах и до четырнадцати раз выше в других. [22] Другие данные того же исследования, полученные с помощью nano- SIMS, предполагают ~75-кратное превышение фосфата (P) над мышьяком (As), когда оно выражается в соотношениях P:C и As:C, даже в клетках, выращенных с арсенатом и мышьяком. без добавления фосфатов. [12] При культивировании в растворе арсената GFAJ-1 рос только на 60% быстрее, чем в растворе фосфата. [2] Бактерии, страдающие от фосфатного голодания, имели внутриклеточный объем в 1,5 раза превышающий нормальный; больший объем, по-видимому, был связан с появлением крупных « вакуолеподобных областей». [1]
.jpg/440px-GFAJ-1_(grown_on_phosphorus).jpg)
Когда исследователь Джозеф Толле добавил в раствор арсенат , меченный изотопами , чтобы отслеживать его распределение , они обнаружили, что мышьяк присутствует в клеточных фракциях, содержащих белки , липиды и метаболиты бактерий , такие как АТФ , а также в их ДНК и РНК . [2] Нуклеиновые кислоты из клеток стационарной фазы, лишенных фосфора, концентрировали посредством пяти экстракций (одну фенолом , три фенол-хлороформом и одну экстракционным растворителем хлороформом ) с последующим осаждением этанолом . Хотя прямых доказательств включения мышьяка в биомолекулы до сих пор нет, измерения радиоактивности показали, что примерно одна десятая часть (11,0 ± 0,1%) мышьяка, поглощенного этими бактериями, оказалась во фракции, содержащей нуклеиновые кислоты (ДНК и РНК). и все другие соосажденные соединения, не экстрагированные предыдущими обработками. [1] Сравнительный контрольный эксперимент с меченым изотопом фосфатом не проводился. После распространения штамма в середине 2011 года другие лаборатории начали независимо проверять достоверность открытия. Розмари Редфилд из Университета Британской Колумбии , проследив проблемы с условиями роста, исследовала требования к росту GFAJ-1 и обнаружила, что штамм лучше растет на твердой агаровой среде, чем в жидкой культуре. Редфилд объяснил это низким уровнем калия и предположил, что уровни калия в базовой среде ML60 могут быть слишком низкими для поддержания роста. [23] Редфилд после обнаружения и решения дополнительных проблем (ионная сила, pH и использование стеклянных трубок вместо полипропилена) обнаружил, что арсенат незначительно стимулирует рост, но не влияет на конечную плотность культур, в отличие от того, что утверждалось. [24] Последующие исследования с использованием масс-спектрометрии, проведенные той же группой, не обнаружили никаких доказательств включения арсената в ДНК GFAJ-1. [25]
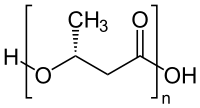
Обычно ожидается, что сложные эфиры арсената , такие как те, которые присутствуют в ДНК , на несколько порядков менее устойчивы к гидролизу , чем соответствующие сложные эфиры фосфатов . [26] dAMA, структурный мышьяковый аналог строительного блока ДНК dAMP , имеет период полураспада 40 минут в воде при нейтральном pH. [27] По оценкам, период полураспада в воде арсенодиэфирных связей, которые связывают нуклеотиды вместе, составляет всего 0,06 секунды — по сравнению с 30 миллионами лет для фосфодиэфирных связей в ДНК. [28] Авторы предполагают, что бактерии могут в некоторой степени стабилизировать эфиры арсената, используя поли-β-гидроксибутират (который, как было обнаружено, повышен в «вакуольных областях» родственных видов рода Halomonas [29] ) или другие средства для снижения эффективной концентрации воды. [1] [10] Полигидроксибутираты используются многими бактериями для хранения энергии и углерода в условиях, когда рост ограничен элементами, отличными от углерода, и обычно выглядят как большие восковые гранулы, очень напоминающие «вакуольные области», наблюдаемые у GFAJ-1. клетки. [30] Авторы не представляют механизма, с помощью которого нерастворимый полигидроксибутират может снизить эффективную концентрацию воды в цитоплазме в достаточной степени для стабилизации эфиров арсената. Хотя все галофилы должны каким-то образом снижать активность воды в своей цитоплазме, чтобы избежать высыхания, [31] цитоплазма всегда остается водной средой.
Объявление НАСА о пресс-конференции, «которая повлияет на поиск доказательств внеземной жизни», подверглось критике как сенсационное и вводящее в заблуждение; в редакционной статье New Scientist прокомментировано: «Хотя открытие инопланетной жизни, если оно когда-либо произойдет, было бы одной из величайших историй, которые только можно себе представить, до этого было несколько световых лет». [32] [33]
Кроме того, многие эксперты, оценивавшие статью, пришли к выводу, что опубликованные исследования не предоставляют достаточных доказательств в поддержку утверждений авторов. [34] В онлайн-статье на Slate научный писатель Карл Циммер обсудил скептицизм нескольких учёных: «Я обратился к дюжине экспертов… Они почти единогласно считают, что учёным НАСА не удалось доказать свою правоту». [35] [36] Химик Стивен А. Беннер выразил сомнение в том, что арсенат заменил фосфат в ДНК этого организма. Он предположил, что следовые примеси в питательной среде, которую Вулф-Саймон использовала в своих лабораторных культурах, достаточны для обеспечения фосфора, необходимого для ДНК клеток. Он считает, что более вероятно, что мышьяк накапливается в других частях клеток. [2] [10] Микробиолог из Университета Британской Колумбии Розмари Редфилд заявила, что в статье «не представлено никаких убедительных доказательств того, что мышьяк был включен в ДНК или любую другую биологическую молекулу», и предполагает, что в экспериментах отсутствовали этапы промывки и контроля. необходимо правильно обосновать свои выводы. [37] [38] Гарвардский микробиолог Алекс Брэдли сказал, что мышьяк-содержащая ДНК будет настолько нестабильной в воде, что не сможет выдержать процедуру анализа. [35] [39]
8 декабря 2010 года журнал Science опубликовал ответ Вулф-Саймон, в котором она заявила, что критика исследования ожидаема. В ответ 16 декабря 2010 г. была опубликована страница « Часто задаваемые вопросы » для лучшего понимания работы. [40] Команда планирует разместить штамм GFAJ-1 в коллекциях культур ATCC и DSMZ , чтобы обеспечить широкое распространение. [41] В конце мая 2011 г. штамм был доступен по запросу непосредственно из лаборатории авторов. [42] Наука предоставила статью в свободный доступ. [43] Статья была опубликована в печати через шесть месяцев после принятия в выпуске журнала Science от 3 июня 2011 года . Публикация сопровождалась восемью техническими комментариями, посвященными различным проблемам, касающимся экспериментальной процедуры и выводов статьи, [44] [45] [46] [47] [48] [49] [50] [51] [52], а также реакция авторов на эти опасения. [42] [53] Главный редактор Брюс Альбертс отметил, что некоторые проблемы остаются и что их решение, вероятно, будет длительным процессом. [54] Обзор Rosen et al. , [55] в мартовском выпуске журнала BioEssays за 2011 год обсуждаются технические проблемы научной статьи , даются альтернативные объяснения и освещаются известные биохимические процессы других устойчивых к мышьяку и мышьяк-утилизирующих микробов.
27 мая 2011 года Вулф-Саймон и ее команда ответили на критику в последующей публикации журнала Science . [42] Затем, в январе 2012 года, группа исследователей под руководством Рози Редфилд из Университета Британской Колумбии проанализировала ДНК GFAJ-1 с помощью жидкостной хроматографии-масс-спектрометрии и не смогла обнаружить никакого мышьяка, что Редфилд называет «четким опровержением» выводы оригинальной статьи. [56] После публикации анализа Вулф-Саймон заявила, что она и ее коллеги «ожидают опубликовать новую информацию в ближайшие несколько месяцев», [57] но по состоянию на 2024 год не представляли никаких новых публикаций с 2011 года.
Простое объяснение роста GFAJ-1 в среде, содержащей арсенат вместо фосфата, было предоставлено группой исследователей из Университета Майами во Флориде. После мечения рибосом лабораторного штамма Escherichia coli радиоактивными изотопами (с образованием радиоактивного индикатора ) они наблюдали за ростом бактерий в среде, содержащей арсенат, но не фосфат. Они обнаружили, что арсенат вызывает массовую деградацию рибосом, обеспечивая тем самым достаточное количество фосфата для медленного роста толерантных к арсенату бактерий. Аналогичным образом, предполагают они, клетки GFAJ-1 растут за счет переработки фосфата из деградированных рибосом, а не за счет замены его арсенатом. [58]
После публикации статей, оспаривающих выводы оригинальной статьи Science , впервые описывающей GFAJ-1, веб-сайт Retraction Watch заявил, что оригинальную статью следует отозвать из-за искажения важных данных. [59] [60] По состоянию на январь 2024 года [обновлять]статья не была отозвана. [1]