

Клеточная мембрана ( также известная как плазматическая мембрана или цитоплазматическая мембрана и исторически называемая плазмалеммой ) представляет собой биологическую мембрану , которая отделяет и защищает внутреннюю часть клетки от внешней среды (внеклеточного пространства). [1] [2] Клеточная мембрана состоит из липидного бислоя , состоящего из двух слоев фосфолипидов с вкраплениями холестерина (липидного компонента), поддерживающего соответствующую текучесть мембраны при различных температурах. Мембрана также содержит мембранные белки , в том числе интегральные белки , которые охватывают мембрану и служат мембранными переносчиками , а также периферические белки , которые свободно прикрепляются к внешней (периферической) стороне клеточной мембраны, действуя как ферменты , облегчающие взаимодействие с окружающей средой клетки. [3] Гликолипиды , встроенные во внешний липидный слой, служат той же цели. Клеточная мембрана контролирует движение веществ в клетку и из нее, будучи избирательно проницаемой для ионов и органических молекул. [4] Кроме того, клеточные мембраны участвуют в различных клеточных процессах, таких как клеточная адгезия , ионная проводимость и передача сигналов в клетках , и служат поверхностью прикрепления для нескольких внеклеточных структур, включая клеточную стенку и углеводный слой, называемый гликокаликсом . а также внутриклеточная сеть белковых волокон, называемая цитоскелетом . В области синтетической биологии клеточные мембраны можно собирать искусственно . [5] [6] [7] [8]
В то время как открытие Робертом Гуком клеток в 1665 году привело к предложению клеточной теории , Гук ввел в заблуждение теорию клеточных мембран , согласно которой все клетки содержат твердую клеточную стенку, поскольку в то время можно было наблюдать только растительные клетки. [9] Микроскописты изучали клеточную стенку более 150 лет, пока не были достигнуты успехи в микроскопии. В начале 19 века клетки были признаны отдельными объектами, несвязанными и связанными отдельными клеточными стенками, после того как было обнаружено, что растительные клетки могут быть разделены. Эта теория распространилась на клетки животных, чтобы предложить универсальный механизм защиты и развития клеток. Ко второй половине XIX века микроскопия еще не была достаточно развита, чтобы различать клеточные мембраны и клеточные стенки. Однако некоторые микроскописты в то время правильно определили, что, хотя они и невидимы, можно сделать вывод, что клеточные мембраны существуют в клетках животных из-за внутриклеточного движения компонентов внутрь, а не наружу, и что мембраны не являются эквивалентом стенки растительной клетки . Был также сделан вывод, что клеточные мембраны не являются жизненно важными компонентами для всех клеток. Многие опровергали существование клеточной мембраны еще ближе к концу 19 века. В 1890 году в обновленной версии клеточной теории говорилось, что клеточные мембраны существуют, но являются лишь вторичными структурами. Лишь в более поздних исследованиях осмоса и проницаемости клеточные мембраны получили большее признание. [9] В 1895 году Эрнест Овертон предположил, что клеточные мембраны состоят из липидов. [10]
Гипотеза липидного бислоя, предложенная в 1925 году Гортером и Гренделем [11], породила предположения в описании двухслойной структуры клеточной мембраны, основанные на кристаллографических исследованиях и наблюдениях за мыльными пузырями. Пытаясь принять или отвергнуть эту гипотезу, исследователи измерили толщину мембраны. Эти исследователи извлекли липид из эритроцитов человека и измерили площадь поверхности, которую липид покроет при распределении по поверхности воды. Поскольку в зрелых эритроцитах млекопитающих отсутствуют как ядра, так и цитоплазматические органеллы, плазматическая мембрана является единственной липидсодержащей структурой в клетке. Следовательно, можно предположить, что все липиды, экстрагированные из клеток, находятся в плазматических мембранах клеток. Отношение площади поверхности воды, покрытой экстрагированным липидом, к площади поверхности, рассчитанной для эритроцитов, из которых был получен липид, составляло 2:1 (приблизительно), и они пришли к выводу, что плазматическая мембрана содержит липидный бислой. [9] [12]
В 1925 году Фрике установил, что толщина мембран эритроцитов и дрожжевых клеток составляет от 3,3 до 4 нм, что соответствует толщине липидного монослоя. Выбор диэлектрической проницаемости, использованной в этих исследованиях, был поставлен под сомнение, но будущие испытания не смогли опровергнуть результаты первоначального эксперимента. Независимо от этого был изобретен лепптоскоп для измерения очень тонких мембран путем сравнения интенсивности света, отраженного от образца, с интенсивностью эталона мембраны известной толщины. Прибор мог определять толщины, которые зависели от измерений pH и присутствия мембранных белков в диапазоне от 8,6 до 23,2 нм, при этом более низкие измерения подтверждают гипотезу липидного бислоя. Позже, в 1930-х годах, модель мембранной структуры, по общему мнению, превратилась в маломолекулярную модель Дэвсона и Даниэлли (1935). Эта модель была основана на исследованиях поверхностного натяжения между маслами и яйцами иглокожих . Поскольку значения поверхностного натяжения оказались намного ниже, чем можно было бы ожидать для границы раздела масло-вода, было предположено, что какое-то вещество отвечает за снижение межфазного натяжения на поверхности клеток. Было высказано предположение, что липидный бислой находится между двумя тонкими белковыми слоями. Пауцимолекулярная модель сразу же стала популярной и доминировала в исследованиях клеточных мембран в течение следующих 30 лет, пока не стала конкурировать с жидкостно-мозаичной моделью Сингера и Николсона ( 1972). [13] [9]
Несмотря на многочисленные модели клеточной мембраны, предложенные до появления модели жидкостной мозаики , она остается основным архетипом клеточной мембраны еще долгое время после ее создания в 1970-х годах. [9] Хотя модель жидкостной мозаики была модернизирована с учетом современных открытий, ее основы остались неизменными: мембрана представляет собой липидный бислой, состоящий из гидрофильных внешних головок и гидрофобной внутренней части, где белки могут взаимодействовать с гидрофильными головками посредством полярных взаимодействий, но белки которые полностью или частично охватывают бислой, содержат гидрофобные аминокислоты, которые взаимодействуют с внутренней частью неполярного липида. Модель жидкостной мозаики не только обеспечила точное представление о механике мембран, но и способствовала изучению гидрофобных сил, которые позже превратились в существенное описательное ограничение для описания биологических макромолекул . [9]
На протяжении многих столетий ученые не соглашались со значением структуры, которую они считали клеточной мембраной. На протяжении почти двух столетий мембраны рассматривались, но по большей части игнорировались, как важная структура с клеточной функцией. Лишь в 20 веке значение клеточной мембраны было признано. Наконец, два учёных Гортер и Грендель (1925) сделали открытие, что мембрана «основана на липидах». Исходя из этого, они выдвинули идею о том, что эта структура должна иметь форму, имитирующую слои. После дальнейшего изучения путем сравнения суммы клеточных поверхностей и поверхностей липидов было обнаружено соотношение 2:1; таким образом, обеспечивая первую основу известной сегодня двухслойной структуры. Это открытие положило начало множеству новых исследований, возникших во всем мире в различных областях научных исследований, подтвердив, что структура и функции клеточной мембраны широко признаны. [9]
Эту структуру разные авторы называли по-разному: эктопласт ( de Vries , 1885), [14] Plasmahaut (плазменная кожа, Pfeffer , 1877, 1891), [15] Hautschicht (кожный слой, Pfeffer, 1886; используется с иное значение по Хофмейстеру , 1867), плазматическая мембрана (Пфеффер, 1900), [16] плазматическая мембрана, цитоплазматическая мембрана, клеточная оболочка и клеточная мембрана. [17] [18] Некоторые авторы, которые не верили, что на поверхности клетки существует функциональная проницаемая граница, предпочитали использовать термин «плазмалемма» (придуманный Мастом, 1924) для внешней области клетки. [19] [20] [21]
Клеточные мембраны содержат множество биологических молекул , особенно липидов и белков. Состав не установлен, но постоянно меняется в зависимости от текучести и изменений окружающей среды, даже колеблясь на разных стадиях развития клеток. В частности, изменяется количество холестерина в мембране первичных нейронов человека, и это изменение в составе влияет на текучесть на всех стадиях развития. [22]
Материал внедряется в мембрану или удаляется из нее с помощью различных механизмов:

Клеточная мембрана состоит из трех классов амфипатических липидов: фосфолипидов , гликолипидов и стеринов . Количество каждого зависит от типа клетки, но в большинстве случаев фосфолипиды являются наиболее распространенными, часто на их долю приходится более 50% всех липидов в плазматических мембранах. [23] [24] Гликолипиды составляют лишь незначительное количество, около 2%, а стерины составляют остальную часть. При исследованиях эритроцитов 30% плазматической мембраны составляют липиды. Однако для большинства эукариотических клеток состав плазматических мембран примерно наполовину состоит из липидов и наполовину из белков по массе.
Жирные цепи фосфолипидов и гликолипидов обычно содержат четное количество атомов углерода, обычно от 16 до 20. Наиболее распространены жирные кислоты с 16 и 18 атомами углерода. Жирные кислоты могут быть насыщенными или ненасыщенными, с конфигурацией двойных связей почти всегда «цис». Длина и степень ненасыщенности цепей жирных кислот оказывают глубокое влияние на текучесть мембраны, поскольку ненасыщенные липиды создают излом, препятствуя плотной упаковке жирных кислот, тем самым снижая температуру плавления (повышая текучесть) мембраны. [23] [24] Способность некоторых организмов регулировать текучесть своих клеточных мембран путем изменения липидного состава называется гомеовязкой адаптацией .
Вся мембрана удерживается вместе за счет нековалентного взаимодействия гидрофобных хвостов, однако структура достаточно текучая и не закреплена жестко на месте. В физиологических условиях молекулы фосфолипидов в клеточной мембране находятся в жидкокристаллическом состоянии . Это означает, что молекулы липидов могут свободно диффундировать и проявлять быструю латеральную диффузию вдоль слоя, в котором они присутствуют. [23] Однако обмен молекул фосфолипидов между внутриклеточными и внеклеточными листками бислоя представляет собой очень медленный процесс. Липидные рафты и кавеолы являются примерами микродоменов, обогащенных холестерином , в клеточной мембране. [24] Кроме того, часть липида, находящаяся в непосредственном контакте с интегральными мембранными белками, которая прочно связана с поверхностью белка, называется кольцевой липидной оболочкой ; он ведет себя как часть белкового комплекса.
Холестерин обычно обнаруживается в различной степени диспергированным по клеточным мембранам, в неравномерных пространствах между гидрофобными хвостами мембранных липидов, где он придает мембране эффект жесткости и укрепления. [4] Кроме того, количество холестерина в биологических мембранах варьируется в зависимости от организма, типа клеток и даже в отдельных клетках. Холестерин, основной компонент плазматических мембран, регулирует текучесть всей мембраны, а это означает, что холестерин контролирует количество движения различных компонентов клеточной мембраны в зависимости от его концентрации. [4] При высоких температурах холестерин ингибирует движение цепей фосфолипидов жирных кислот, вызывая снижение проницаемости для малых молекул и снижение текучести мембран. Противоположное верно в отношении роли холестерина при более низких температурах. Производство холестерина и, следовательно, его концентрация регулируются (увеличиваются) в ответ на низкую температуру. При низких температурах холестерин препятствует взаимодействию цепей жирных кислот. Действуя как антифриз, холестерин поддерживает текучесть мембраны. Холестерина больше у животных, живущих в холодную погоду, чем у животных, живущих в теплую погоду. В растениях, в которых отсутствует холестерин, родственные соединения, называемые стеролами, выполняют ту же функцию, что и холестерин. [4]
Липидные везикулы или липосомы представляют собой примерно сферические карманы, окруженные липидным бислоем. [25] Эти структуры используются в лабораториях для изучения воздействия химических веществ на клетки путем доставки этих химических веществ непосредственно в клетку, а также для получения более глубокого понимания проницаемости клеточных мембран. Липидные везикулы и липосомы образуются путем сначала суспендирования липида в водном растворе, а затем перемешивания смеси посредством обработки ультразвуком , в результате чего образуется везикула. Измерение скорости оттока из внутренней части везикулы в окружающий раствор позволяет исследователю лучше понять проницаемость мембраны. Везикулы могут быть образованы молекулами и ионами внутри везикул путем формирования везикул с желаемой молекулой или ионом, присутствующими в растворе. Белки также можно внедрить в мембрану путем солюбилизации нужных белков в присутствии детергентов и присоединения их к фосфолипидам, из которых формируется липосома. Они предоставляют исследователям инструмент для изучения различных функций мембранных белков.
Плазматические мембраны также содержат углеводы , преимущественно гликопротеины , но с некоторым количеством гликолипидов ( цереброзиды и ганглиозиды ). Углеводы играют важную роль в межклеточном распознавании у эукариот; они расположены на поверхности клетки, где распознают клетки-хозяева и делятся информацией; вирусы, которые связываются с клетками с помощью этих рецепторов, вызывают инфекцию [26] . По большей части на мембранах внутри клетки гликозилирование не происходит; скорее всего гликозилирование происходит на внеклеточной поверхности плазматической мембраны. Гликокаликс является важной особенностью всех клеток, особенно эпителия с микроворсинками . Недавние данные свидетельствуют о том, что гликокаликс участвует в клеточной адгезии, возвращении лимфоцитов [26] и многих других. Предпоследний сахар представляет собой галактозу , а концевой сахар — сиаловую кислоту , поскольку сахарный остов модифицируется в аппарате Гольджи . Сиаловая кислота несет отрицательный заряд, обеспечивая внешний барьер для заряженных частиц.
Клеточная мембрана содержит большое количество белков, обычно около 50% объема мембраны [27]. Эти белки важны для клетки, поскольку они отвечают за различную биологическую активность. Примерно треть генов дрожжей кодируют именно их, а у многоклеточных организмов это число еще выше . [25] Мембранные белки состоят из трех основных типов: интегральные белки, периферические белки и белки, закрепленные на липидах. [4]
Как показано в соседней таблице, интегральные белки представляют собой амфипатические трансмембранные белки. Примеры интегральных белков включают ионные каналы, протонные насосы и рецепторы, связанные с g-белком. Ионные каналы позволяют неорганическим ионам, таким как натрий, калий, кальций или хлор, диффундировать по электрохимическому градиенту через липидный бислой через гидрофильные поры через мембрану. Электрическое поведение клеток (т.е. нервных клеток) контролируется ионными каналами. [4] Протонные насосы — это белковые насосы, встроенные в липидный бислой, которые позволяют протонам проходить через мембрану путем переноса с одной боковой цепи аминокислоты на другую. Такие процессы, как транспорт электронов и производство АТФ, используют протонные насосы. [4] Рецептор, связанный с G-белком, представляет собой одну полипептидную цепь, которая семь раз пересекает липидный бислой, реагируя на сигнальные молекулы (т.е. гормоны и нейротрансмиттеры). Рецепторы, связанные с G-белком, используются в таких процессах, как передача сигналов от клетки к клетке, регуляция выработки цАМФ и регуляция ионных каналов. [4]
Клеточная мембрана, подвергающаяся воздействию внешней среды, является важным местом межклеточной коммуникации. Таким образом, на поверхности мембраны присутствует большое разнообразие белковых рецепторов и идентификационных белков, таких как антигены . Функции мембранных белков могут также включать межклеточный контакт, распознавание поверхности, контакт с цитоскелетом, передачу сигналов, ферментативную активность или транспорт веществ через мембрану.
Большинство мембранных белков должны каким-то образом встраиваться в мембрану. [28] Чтобы это произошло, N-концевая «сигнальная последовательность» аминокислот направляет белки в эндоплазматический ретикулум , который вставляет белки в липидный бислой. После внедрения белки транспортируются к конечному пункту назначения в везикулах, где везикула сливается с целевой мембраной.


Клеточная мембрана окружает цитоплазму живых клеток, физически отделяя внутриклеточные компоненты от внеклеточной среды. Клеточная мембрана также играет роль в закреплении цитоскелета, придавая клетке форму, а также в прикреплении к внеклеточному матриксу и другим клеткам, удерживая их вместе для формирования тканей . Грибы , бактерии , большинство архей и растения также имеют клеточную стенку , которая обеспечивает механическую поддержку клетки и предотвращает прохождение более крупных молекул .
Клеточная мембрана избирательно проницаема и способна регулировать то, что входит в клетку и выходит из нее, тем самым облегчая транспорт материалов, необходимых для выживания. Перемещение веществ через мембрану может осуществляться либо пассивным транспортом , происходящим без затрат клеточной энергии, либо активным транспортом , требующим от клетки затрат энергии на его транспортировку. Мембрана также поддерживает потенциал клетки . Таким образом, клеточная мембрана работает как селективный фильтр, который позволяет только определенным вещам проникать внутрь клетки или выходить за ее пределы. Клетка использует ряд транспортных механизмов, в которых участвуют биологические мембраны:
1. Пассивный осмос и диффузия . Некоторые вещества (малые молекулы, ионы), такие как углекислый газ (CO 2 ) и кислород (O 2 ), могут перемещаться через плазматическую мембрану путем диффузии, которая представляет собой процесс пассивного транспорта. Поскольку мембрана действует как барьер для определенных молекул и ионов, они могут встречаться в разных концентрациях по обе стороны мембраны. Диффузия происходит, когда небольшие молекулы и ионы свободно перемещаются от высокой концентрации к низкой концентрации, чтобы уравновесить мембрану. Это считается пассивным процессом транспорта, поскольку он не требует энергии и приводится в движение градиентом концентрации, создаваемым каждой стороной мембраны. [29] Такой градиент концентрации на полупроницаемой мембране создает осмотический поток воды. Осмос в биологических системах включает в себя движение растворителя через полупроницаемую мембрану аналогично пассивной диффузии, поскольку растворитель все еще движется по градиенту концентрации и не требует энергии. Хотя вода является наиболее распространенным растворителем в клетке, ею могут быть и другие жидкости, а также сверхкритические жидкости и газы. [30]
2. Трансмембранные белковые каналы и переносчики . Трансмембранные белки проходят через липидный бислой мембран; они функционируют по обе стороны мембраны, транспортируя через нее молекулы. [31] Питательные вещества, такие как сахара или аминокислоты, должны поступать в клетку, а некоторые продукты метаболизма должны покидать клетку. Такие молекулы могут пассивно диффундировать через белковые каналы, такие как аквапорины , при облегченной диффузии , или перекачиваться через мембрану трансмембранными переносчиками . Белки белковых каналов, также называемые пермеазами , обычно весьма специфичны и распознают и транспортируют только ограниченное количество химических веществ, часто ограниченное одним веществом. Другим примером трансмембранного белка является рецептор клеточной поверхности, который позволяет сигнальным молекулам клетки связываться между клетками. [31]
3. Эндоцитоз : Эндоцитоз — это процесс, при котором клетки поглощают молекулы, поглощая их. Плазматическая мембрана создает небольшую деформацию внутрь, называемую инвагинацией, при которой захватывается транспортируемое вещество. Эта инвагинация вызвана белками, находящимися снаружи клеточной мембраны, действующими как рецепторы и группирующимися в углубления, которые в конечном итоге способствуют накоплению большего количества белков и липидов на цитозольной стороне мембраны. [32] Затем деформация отрывается от мембраны внутри клетки, образуя везикулу, содержащую захваченное вещество. Эндоцитоз — это путь интернализации твердых частиц («поедание клеток» или фагоцитоз ), малых молекул и ионов («питание клеток» или пиноцитоз ) и макромолекул. Эндоцитоз требует энергии и, таким образом, является формой активного транспорта.
4. Экзоцитоз . Точно так же, как материал может быть введен в клетку путем инвагинации и образования пузырька, мембрана пузырька может сливаться с плазматической мембраной, выдавливая ее содержимое в окружающую среду. Это процесс экзоцитоза. Экзоцитоз происходит в различных клетках для удаления непереваренных остатков веществ, поступивших в результате эндоцитоза, для секреции таких веществ, как гормоны и ферменты, и для полной транспортировки веществ через клеточный барьер. В процессе экзоцитоза непереваренная пищевая вакуоль, содержащая отходы, или секреторный везикула, отпочковавшаяся из аппарата Гольджи , сначала перемещается цитоскелетом из внутренней части клетки на поверхность. Мембрана пузырька соприкасается с плазматической мембраной. Молекулы липидов двух бислоев перестраиваются, и две мембраны, таким образом, сливаются. В сросшейся мембране образуется проход и везикулы выбрасывают свое содержимое за пределы клетки.
Прокариоты делятся на две разные группы: археи и бактерии , причем бактерии делятся на грамположительные и грамотрицательные . Грамотрицательные бактерии имеют как плазматическую мембрану, так и внешнюю мембрану, разделенную периплазмой , однако другие прокариоты имеют только плазматическую мембрану. Эти две мембраны различаются во многих аспектах. Наружная мембрана грамотрицательных бактерий отличается от других прокариот тем, что фосфолипиды образуют внешнюю часть бислоя, а липопротеины и фосфолипиды образуют внутреннюю часть. [33] Внешняя мембрана обычно имеет пористую структуру из-за присутствия в ней мембранных белков, таких как грамотрицательные порины, которые являются порообразующими белками. Внутренняя плазматическая мембрана также обычно симметрична, тогда как внешняя мембрана асимметрична из-за таких белков, как вышеупомянутые. Кроме того, на текучесть прокариотических мембран может влиять множество факторов. Одним из основных факторов, которые могут повлиять на текучесть, является состав жирных кислот. Например, когда бактерии Staphylococcus aureus выращивались при температуре 37 ◦ C в течение 24 часов, мембрана находилась в более жидком состоянии, а не в гелеобразном. Это подтверждает концепцию о том, что при более высоких температурах мембрана более текучая, чем при более низких температурах. Когда мембрана становится более жидкой и нуждается в большей стабилизации, она образует более длинные цепи жирных кислот или цепи насыщенных жирных кислот, чтобы помочь стабилизировать мембрану. [34] Бактерии также окружены клеточной стенкой , состоящей из пептидогликана (аминокислот и сахаров). Некоторые эукариотические клетки также имеют клеточные стенки, но ни одна из них не состоит из пептидогликана. Наружная мембрана грамотрицательных бактерий богата липополисахаридами , представляющими собой сочетание поли- или олигосахаридов и углеводно-липидных участков, которые стимулируют естественный иммунитет клетки. [35] Внешняя мембрана может выделяться в периплазматические выступы в условиях стресса или при необходимости вирулентности при встрече с клеткой-мишенью-хозяином, и, таким образом, такие пузырьки могут работать как органеллы вирулентности. [36] Бактериальные клетки служат многочисленными примерами разнообразных способов, которыми мембраны прокариотических клеток адаптируются к структурам, соответствующим нише организма. Например, белки на поверхности некоторых бактериальных клеток способствуют их скольжению. [37] Многие грамотрицательные бактерии имеют клеточные мембраны, которые содержат системы экспорта белка, управляемые АТФ.[37]
Согласно жидкостно-мозаичной модели С. Дж. Сингера и Г. Л. Николсона (1972), пришедшей на смену более ранней модели Дэвсона и Даниэлли , биологические мембраны можно рассматривать как двумерную жидкость, в которой молекулы липидов и белков диффундируют более или менее легко. [38] Хотя липидные бислои, составляющие основу мембран, действительно сами по себе образуют двумерные жидкости, плазматическая мембрана также содержит большое количество белков, которые обеспечивают большую структуру. Примерами таких структур являются белково-белковые комплексы, пикеты и заборы, образованные актиновым цитоскелетом , и потенциально липидные рафты .

Липидные бислои образуются в процессе самосборки . Клеточная мембрана состоит в основном из тонкого слоя амфипатических фосфолипидов , которые самопроизвольно располагаются таким образом, что гидрофобные «хвостовые» области изолированы от окружающей воды, в то время как гидрофильные «головные» области взаимодействуют с внутриклеточными (цитозольными) и внеклеточными поверхностями образовавшегося бислоя. . Это образует непрерывный сферический липидный бислой . Гидрофобные взаимодействия (также известные как гидрофобный эффект ) являются основными движущими силами образования липидных бислоев. Увеличение взаимодействий между гидрофобными молекулами (вызывающее кластеризацию гидрофобных областей) позволяет молекулам воды более свободно связываться друг с другом, увеличивая энтропию системы. Это сложное взаимодействие может включать нековалентные взаимодействия, такие как ван-дер-ваальсовые , электростатические и водородные связи.
Липидные бислои обычно непроницаемы для ионов и полярных молекул. Расположение гидрофильных головок и гидрофобных хвостов липидного бислоя предотвращает диффузию полярных растворенных веществ (например, аминокислот, нуклеиновых кислот, углеводов, белков и ионов) через мембрану, но обычно обеспечивает пассивную диффузию гидрофобных молекул. Это дает клетке возможность контролировать движение этих веществ через трансмембранные белковые комплексы, такие как поры, каналы и ворота.Флиппазы и скрамблазы концентрируют на внутренней мембране фосфатидилсерин , несущий отрицательный заряд. Вместе с NANA это создает дополнительный барьер для прохождения заряженных фрагментов через мембрану.
Мембраны выполняют разнообразные функции в эукариотических и прокариотических клетках. Одной из важных функций является регулирование движения материалов в клетки и из них. Двухслойная структура фосфолипидов (модель жидкостной мозаики) со специфическими мембранными белками обеспечивает избирательную проницаемость мембраны, а также механизмы пассивного и активного транспорта. Кроме того, мембраны прокариот, а также митохондрий и хлоропластов эукариот облегчают синтез АТФ посредством хемиосмоса. [8]
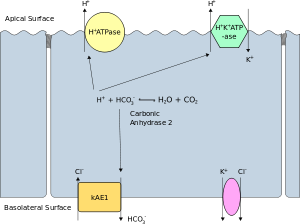
Апикальная мембрана или просветная мембрана поляризованной клетки представляет собой поверхность плазматической мембраны, обращенную внутрь просвета . Это особенно очевидно в эпителиальных и эндотелиальных клетках , но также характерно и для других поляризованных клеток, таких как нейроны . Базолатеральная мембрана или базолатеральная клеточная мембрана поляризованной клетки — это поверхность плазматической мембраны, образующая ее базальную и латеральную поверхности. [39] Он обращен наружу, в сторону интерстиция и в сторону от просвета. Базолатеральная мембрана — это сложное словосочетание, обозначающее термины «базальная (базовая) мембрана» и «латеральная (боковая) мембрана», которые, особенно в эпителиальных клетках, идентичны по составу и активности. Белки (такие как ионные каналы и насосы ) могут свободно перемещаться от базальной к латеральной поверхности клетки или наоборот в соответствии с моделью жидкостной мозаики . Плотные соединения соединяют эпителиальные клетки вблизи их апикальной поверхности, чтобы предотвратить миграцию белков из базолатеральной мембраны в апикальную мембрану. Таким образом, базальная и латеральная поверхности остаются примерно эквивалентными [ необходимы пояснения ] друг другу, но отличаются от апикальной поверхности.

Клеточная мембрана может образовывать различные типы «надмембранных» структур, таких как кавеолы , постсинаптическая плотность , подосомы , инвадоподии , фокальная адгезия и различные типы клеточных соединений . Эти структуры обычно отвечают за клеточную адгезию , коммуникацию, эндоцитоз и экзоцитоз . Их можно визуализировать с помощью электронной или флуоресцентной микроскопии . Они состоят из специфических белков, таких как интегрины и кадгерины .
Цитоскелет находится под клеточной мембраной в цитоплазме и обеспечивает основу для закрепления мембранных белков, а также формирует органеллы , выходящие из клетки. Действительно, элементы цитоскелета широко и тесно взаимодействуют с клеточной мембраной. [40] Закрепление белков ограничивает их определенную поверхность клетки — например, апикальную поверхность эпителиальных клеток, выстилающих кишечник позвоночных , — и ограничивает степень их диффузии внутри бислоя. Цитоскелет способен формировать органеллы, подобные придаткам, такие как реснички , которые представляют собой расширения на основе микротрубочек , покрытые клеточной мембраной, и филоподии , которые представляют собой расширения на основе актина . Эти расширения покрыты мембраной и выступают над поверхностью клетки, чтобы воспринимать внешнюю среду и/или вступать в контакт с субстратом или другими клетками. Апикальные поверхности эпителиальных клеток плотны и покрыты пальцеобразными выступами на основе актина, известными как микроворсинки , которые увеличивают площадь поверхности клеток и тем самым увеличивают скорость поглощения питательных веществ. Локализованное разделение цитоскелета и клеточной мембраны приводит к образованию пузыря .
Содержимое клетки внутри клеточной мембраны состоит из многочисленных мембраносвязанных органелл , которые способствуют общей функции клетки. Происхождение, структура и функция каждой органеллы приводят к большим различиям в составе клеток из-за индивидуальной уникальности, связанной с каждой органеллой.
Клеточная мембрана имеет разный липидный и белковый состав в разных типах клеток и поэтому может иметь особые названия для определенных типов клеток.
Проницаемость мембраны – это скорость пассивной диффузии молекул через мембрану. Эти молекулы известны как проникающие молекулы. Проницаемость зависит главным образом от электрического заряда и полярности молекулы и в меньшей степени от молярной массы молекулы. Из-за гидрофобной природы клеточной мембраны небольшие электрически нейтральные молекулы проходят через мембрану легче, чем заряженные большие. Неспособность заряженных молекул проходить через клеточную мембрану приводит к рН-распределению веществ по жидкостям организма.
{{cite journal}}: CS1 maint: местоположение ( ссылка )