
В клеточной биологии веретенообразный аппарат представляет собой цитоскелетную структуру эукариотических клеток , которая образуется во время клеточного деления для разделения сестринских хроматид между дочерними клетками . Его называют митотическим веретеном во время митоза — процесса, в результате которого образуются генетически идентичные дочерние клетки, или мейотическим веретеном во время мейоза — процесса, в результате которого образуются гаметы с половиной числа хромосом родительской клетки.
Помимо хромосом, веретенообразный аппарат состоит из сотен белков . [1] [2] Микротрубочки составляют наиболее распространенные компоненты механизма.
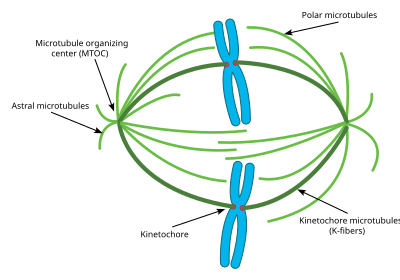
Прикрепление микротрубочек к хромосомам опосредуется кинетохорами , которые активно контролируют формирование веретена и предотвращают преждевременное наступление анафазы . Полимеризация и деполимеризация микротрубочек динамически управляют конгрессом хромосом. Деполимеризация микротрубочек вызывает напряжение кинетохор; [3] биполярное прикрепление сестринских кинетохор к микротрубочкам, исходящим от противоположных полюсов клеток, образует пары, противодействующие силам натяжения, выравнивая хромосомы по экватору клетки и подготавливая их для разделения на дочерние клетки. Как только каждая хромосома становится биориентированной, начинается анафаза и когезин , соединяющий сестринские хроматиды , разрывается, обеспечивая переход сестринских хроматид к противоположным полюсам.
Аппарат клеточного веретена включает микротрубочки веретена , связанные с ним белки, в том числе молекулярные моторы кинезина и динеина , конденсированные хромосомы и любые центросомы или астры , которые могут присутствовать на полюсах веретена в зависимости от типа клеток. [4] Веретенообразный аппарат имеет в поперечном сечении неопределенно эллипсоидную форму и сужается на концах. В широкой средней части, известной как средняя зона веретена, антипараллельные микротрубочки связаны кинезинами . На заостренных концах, известных как полюса веретена, микротрубочки зарождаются центросомами в большинстве животных клеток. В ацентросомальных или анастральных веретенах отсутствуют центросомы или астры на полюсах веретена соответственно, и они возникают, например, во время женского мейоза у большинства животных. [5] В этом случае градиент Ran GTP является основным регулятором организации и сборки веретена микротрубочек. У грибов веретена образуются между телами полюсов веретена, встроенными в ядерную оболочку , которая не разрушается во время митоза.
Динамическое удлинение и укорочение микротрубочек веретена посредством процесса, известного как динамическая нестабильность , в значительной степени определяет форму митотического веретена и способствует правильному выравниванию хромосом в средней зоне веретена. Белки, ассоциированные с микротрубочками (MAP), связываются с микротрубочками в средней зоне и полюсах веретена, регулируя их динамику. γ-тубулин представляет собой специализированный вариант тубулина , который собирается в кольцевой комплекс, называемый γ-TuRC , который запускает полимеризацию гетеродимеров α/β тубулина в микротрубочки. Привлечение γ-TuRC в перицентросомальную область стабилизирует минус-концы микротрубочек и закрепляет их вблизи центра организации микротрубочек . Связанный с микротрубочками белок Augmin действует совместно с γ-TURC, образуя ядра новых микротрубочек из существующих микротрубочек. [6]
Растущие концы микротрубочек защищены от катастрофы действием белков, отслеживающих плюс-концы микротрубочек (+TIPs), которые способствуют их ассоциации с кинетохорами в средней зоне. Было показано, что CLIP170 локализуется вблизи плюс-концов микротрубочек в клетках HeLa [7] и накапливается в кинетохорах во время прометафазы . [8] Хотя то, как CLIP170 распознает плюс-концы, остается неясным, было показано, что его гомологи защищают от катастрофы и способствуют спасению, [9] [10] предполагая роль CLIP170 в стабилизации плюс-концов и, возможно, опосредовании их прямого прикрепления к кинетохоры. [11] Также было показано , что CLIP-ассоциированные белки, такие как CLASP1 у людей, локализуются на плюс-концах и внешнем кинетохоре, а также модулируют динамику микротрубочек кинетохора (Maiato 2003). Гомологи CLASP у Drosophila , Xenopus и дрожжей необходимы для правильной сборки веретена; у млекопитающих CLASP1 и CLASP2 способствуют правильной сборке веретена и динамике микротрубочек в анафазе. [12] Полимеризация плюс-конца может быть дополнительно замедлена белком EB1, который напрямую связывает растущие концы микротрубочек и координирует связывание других +TIP. [13] [14]
Действию этих белков, стабилизирующих микротрубочки, противостоит ряд факторов, деполимеризующих микротрубочки, которые позволяют динамическое ремоделирование митотического веретена, чтобы способствовать конгрессу хромосом и достижению биполярности . Суперсемейство кинезина -13 MAP содержит класс моторных белков, направленных на плюс-концы, с ассоциированной активностью деполимеризации микротрубочек, включая хорошо изученные MCAK млекопитающих и Xenopus XKCM1 . MCAK локализуется на растущих кончиках микротрубочек в кинетохорах, где может вызвать катастрофу в прямой конкуренции со стабилизирующей активностью +TIP. [15] Эти белки используют энергию гидролиза АТФ , чтобы вызвать дестабилизирующие конформационные изменения в структуре протофиламентов, которые вызывают высвобождение кинезина и деполимеризацию микротрубочек. [16] Потеря их активности приводит к многочисленным митотическим дефектам. [15] Дополнительные белки, дестабилизирующие микротрубочки, включают Op18/ статмин и катанин , которые играют роль в ремоделировании митотического веретена, а также способствуют сегрегации хромосом во время анафазы. [17]
Активность этих MAP тщательно регулируется для поддержания правильной динамики микротрубочек во время сборки веретена, при этом многие из этих белков служат субстратами Aurora и Polo-подобных киназ . [17] [18]
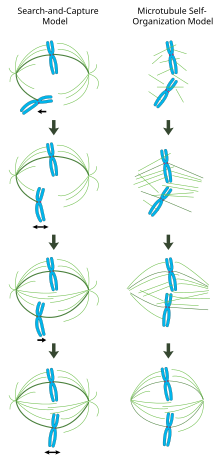
В правильно сформированном митотическом веретене биориентированные хромосомы выровнены вдоль экватора клетки, причем микротрубочки веретена ориентированы примерно перпендикулярно хромосомам, их плюс-концы встроены в кинетохоры, а их минус-концы закреплены на полюсах клетки. Точная ориентация этого комплекса необходима для обеспечения точного разделения хромосом и определения плоскости деления клеток. Однако остается неясным, как организовано веретено. В этой области преобладают две модели, которые являются синергическими и не исключают друг друга. В модели поиска и захвата веретено преимущественно организовано путем разделения к полюсам центросомальных центров организации микротрубочек (MTOCs). Микротрубочки веретена исходят из центросом и «ищут» кинетохоры; когда они связываются с кинетохорами, они стабилизируются и оказывают на хромосомы напряжение. В альтернативной модели самосборки микротрубочки подвергаются ацентросомальному зарождению среди конденсированных хромосом. Ограниченные клеточными размерами, латеральными ассоциациями с антипараллельными микротрубочками посредством моторных белков и прикреплением концов к кинетохорам, микротрубочки естественным образом принимают веретенообразную структуру с хромосомами, выровненными вдоль экватора клетки.
В этой модели микротрубочки зарождаются в центрах организации микротрубочек и подвергаются быстрому росту и катастрофе для «поиска» цитоплазмы кинетохор. Как только они связываются с кинетохорой, они стабилизируются, и их динамика снижается. Вновь моноориентированная хромосома колеблется в пространстве вблизи полюса, к которому она прикреплена, пока микротрубочка с противоположного полюса не свяжет сестринскую кинетохору. Это второе прикрепление дополнительно стабилизирует прикрепление кинетохор к митотическому веретену. Постепенно биориентированная хромосома тянется к центру клетки до тех пор, пока натяжение микротрубочек не сбалансируется по обе стороны центромеры ; затем сросшаяся хромосома колеблется в метафазной пластинке до тех пор, пока наступление анафазы не приведет к потере сцепления сестринских хроматид.
В этой модели центры организации микротрубочек локализованы на полюсах клетки, их разделение обусловлено полимеризацией микротрубочек и "скольжением" антипараллельных микротрубочек веретена относительно друг друга в средней зоне веретена, опосредованное биполярными кинезинами, направленными на плюс-концы. [19] [20] Такие силы скольжения могут объяснять не только разделение полюсов веретена на ранних стадиях митоза, но и удлинение веретена во время поздней анафазы.
В отличие от механизма поиска и захвата, при котором центросомы в значительной степени определяют организацию митотического веретена, эта модель предполагает, что микротрубочки зарождаются ацентросомально вблизи хромосом и спонтанно собираются в антипараллельные пучки и принимают веретеноподобную структуру. [21] Классические эксперименты Хилда и Карсенти показывают, что функциональные митотические веретена и ядра формируются вокруг покрытых ДНК шариков, инкубированных в экстрактах яиц Xenopus , и что биполярные массивы микротрубочек образуются в отсутствие центросом и кинетохор. [22] Действительно, также было показано, что лазерная абляция центросом в клетках позвоночных не ингибирует ни сборку веретена, ни сегрегацию хромосом. [23] Согласно этой схеме, форма и размер митотического веретена являются функцией биофизических свойств сшивающих моторных белков. [24]
Фактор обмена гуаниновых нуклеотидов для малой ГТФазы Ran (регулятор конденсации хромосом 1 или RCC1 ) прикрепляется к нуклеосомам через коровые гистоны H2A и H2B. [25] Таким образом, градиент GTP-связанного Ran генерируется вокруг митотического хроматина. Стеклянные шарики, покрытые RCC1, индуцируют зарождение микротрубочек и образование биполярного веретена в экстрактах яиц Xenopus , показывая, что одного градиента Ran GTP достаточно для сборки веретена. [26] Градиент запускает высвобождение факторов сборки веретена (SAF) от ингибирующих взаимодействий через транспортные белки импортин β/α. Несвязанные SAF затем способствуют зарождению и стабилизации микротрубочек вокруг митотического хроматина, а биполярность веретена организуется моторными белками микротрубочек. [27]
Сборка веретена в значительной степени регулируется событиями фосфорилирования, катализируемыми митотическими киназами. Циклинзависимые киназные комплексы (CDK) активируются митотическими циклинами, трансляция которых увеличивается во время митоза. CDK1 (также называемый CDC2) считается основной митотической киназой в клетках млекопитающих и активируется циклином B1. Киназы Авроры необходимы для правильной сборки и разделения веретена. [28] Аврора А связывается с центросомами и, как полагают, регулирует вход в митоз. Аврора B является членом хромосомного пассажирского комплекса и обеспечивает прикрепление хромосом к микротрубочкам и слипание сестринских хроматид. Поло-подобная киназа, также известная как PLK, особенно PLK1, играет важную роль в поддержании веретена, регулируя динамику микротрубочек. [29]
К концу репликации ДНК сестринские хроматиды соединяются в аморфную массу запутанной ДНК и белка. Митотический вход запускает резкую реорганизацию дублированного генома, в результате чего сестринские хроматиды распутываются и отделяются друг от друга. Хромосомы также укорачиваются в длину, в 10 000 раз в животных клетках [30] в процессе, называемом конденсацией. Конденсация начинается в профазе, и хромосомы максимально уплотняются в палочковидные структуры к моменту их выравнивания в середине веретена в метафазе. Это придает митотическим хромосомам классическую форму «X», наблюдаемую в кариотипах , где каждая конденсированная сестринская хроматида связана по длине белками когезина и соединена, часто около центра, в центромере . [30] [31] [32]
Хотя эти динамические перестройки жизненно важны для обеспечения точного и точного разделения генома, наше понимание структуры митотических хромосом остается в значительной степени неполным. Однако было идентифицировано несколько конкретных молекулярных игроков: топоизомераза II использует гидролиз АТФ, чтобы катализировать распад запутанностей ДНК, способствуя разрешению сестринских хроматид. [33] Конденсины представляют собой комплексы из 5 субъединиц, которые также используют АТФ-гидролиз для содействия конденсации хромосом. [34] Эксперименты с экстрактами яиц Xenopus также показали, что линкер гистон H1 является важным регулятором уплотнения митотических хромосом. [35]
Завершение формирования веретена является решающей точкой перехода в клеточном цикле, называемой контрольной точкой сборки веретена . Если к моменту этой контрольной точки хромосомы не прикрепятся должным образом к митотическому веретену, наступление анафазы будет отложено. [36] Неисправность этой контрольной точки сборки веретена может привести к анеуплоидии и может быть вовлечена в старение и образование рака. [37]

Ориентация клеточного деления имеет большое значение для тканевой архитектуры, клеточных судеб и морфогенеза. Клетки имеют тенденцию делиться вдоль своей длинной оси в соответствии с так называемым правилом Гертвига . Ось деления клеток определяется ориентацией веретенообразного аппарата. Клетки делятся по линии, соединяющей две центросомы веретенообразного аппарата. После формирования веретенообразный аппарат подвергается вращению внутри клетки. Астральные микротрубочки, исходящие из центросом, достигают клеточной мембраны, где они тянутся к определенным корковым сигналам. In vitro распределение корковых сигналов определяется адгезионным паттерном. [38] Сигналы полярности in vivo определяются локализацией трехклеточных соединений, локализованных в вершинах клеток. [39] Пространственное распределение корковых сигналов приводит к формированию силового поля, которое определяет окончательную ориентацию веретенообразного аппарата и последующую ориентацию клеточного деления.
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка )