Нейрофиброматоз II типа (также известный как синдром MISME – множественные наследственные шванномы, менингиомы и эпендимомы) – это генетическое заболевание, которое может передаваться по наследству или возникать спонтанно и вызывает доброкачественные опухоли головного, спинного мозга и периферических нервов. Типы опухолей, часто ассоциированные с NF2, включают вестибулярные шванномы, менингиомы и эпендимомы. Основным проявлением состояния является развитие двусторонних доброкачественных опухолей головного мозга в нервной оболочке VIII черепного нерва , который представляет собой «слухово-вестибулярный нерв», передающий сенсорную информацию от внутреннего уха к мозгу . Кроме того, возникают другие доброкачественные опухоли головного и спинного мозга. Симптомы зависят от наличия, локализации и роста опухоли(ок), в которую могут поражаться несколько черепных нервов. [2] Многие люди с этим заболеванием также испытывают проблемы со зрением. Нейрофиброматоз типа II (NF2 или NF II) вызван мутациями гена «Мерлин» , [ 3] который, по-видимому, влияет на форму и движение клеток . Основные методы лечения включают нейрохирургическое удаление опухолей и хирургическое лечение поражений глаз. Исторически основное заболевание не подвергалось никакому лечению из-за функции клеток, вызванной генетической мутацией.
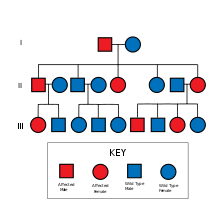
НФ2 — наследственное заболевание с аутосомно-доминантным типом передачи. [4]
Существует две формы NF2: [5]
Симптомы могут возникнуть в любом возрасте, обычно в подростковом и раннем взрослом возрасте, редко наблюдаются у детей, а тяжесть зависит от местоположения опухолей. Симптомы включают, помимо прочего :
Поскольку потеря слуха у людей с NF2 почти всегда происходит после приобретения навыков вербальной речи, люди с NF2 не всегда хорошо интегрируются в культуру глухих и с большей вероятностью прибегают к слуховым вспомогательным технологиям . [ нужна цитата ] Одним из таких устройств является кохлеарный имплант , который иногда может восстановить высокий уровень слуховой функции, даже когда естественный слух полностью потерян. Однако степень разрушения улиткового нерва, вызванная типичной шванномой NF2, часто исключает использование такого имплантата. В этих случаях слуховой имплант ствола мозга (ABI) может восстановить некоторый уровень слуха, дополненный чтением по губам . [ нужна цитата ]
NF2 вызывается инактивирующими мутациями в гене NF2, расположенном в 22q12.2 хромосомы 22. Типы мутаций различаются и включают изменения, связанные с усечением белка (делеции/вставки сдвига рамки считывания и нонсенс-мутации), мутации сайта сплайсинга, миссенс-мутации и другие. Делеции в NH2-концевом домене белков мерлина также связаны с ранним возникновением опухоли и плохим прогнозом у людей с NF2. [6] Мутации усечения белка коррелируют с более тяжелым фенотипом. [7] Известен широкий клинический спектр, но у всех людей с этим заболеванием, которые были проверены, была обнаружена некоторая мутация одного и того же гена на хромосоме 22 . Согласно статистике, предполагается, что половина случаев передается по наследству, а половина является результатом новых мутаций de novo . [ нужна цитата ]
Потеря слуха, вызванная NF2, является постепенной и возникает в результате наличия двусторонних кохлеовестибулярных шванном, также известных как акустические невриномы, которые повреждают улитковый нерв, вызывая потерю слуха. [ нужна цитация ] Потеря слуха также может быть результатом доброкачественных опухолей, которые растут на вестибулярных и слуховых нервах, ведущих во внутреннее ухо. [ нужна цитата ]
NF2 вызван дефектом гена, который в норме дает начало продукту под названием Мерлин или Шванномин , расположенному в полосе q11-13.1 хромосомы 22. Мерлин был впервые обнаружен как структурный белок, выполняющий функцию регулятора актинового цитоскелета. Позже была описана роль Мерлина в подавлении опухолей. Мерлин регулирует множественные пролиферативные сигнальные каскады, такие как передача сигналов рецепторной тирозинкиназы , передача сигналов p21-активируемой киназы , передача сигналов Ras , каскад MEK - ERK , каскад MST-YAP . [8] В нормальной клетке концентрация активного (дефосфорилированного) мерлина контролируется такими процессами, как клеточная адгезия (что указывает на необходимость ограничения клеточного деления). Было показано, что Мерлин ингибирует Rac1 , который имеет решающее значение для подвижности клеток и инвазии опухоли. [9] Также было описано взаимодействие мерлина с циклином D. [10] Известно, что дефицит Мерлина может привести к неопосредованному прогрессированию клеточного цикла из-за отсутствия контактно-опосредованного подавления опухоли, главным образом из-за разрушения межклеточного соединения, достаточного для возникновения опухолей, характерных для нейрофиброматоза II типа. . Недавние исследования показали, что помимо своих цитоскелетных и цитоплазматических функций Мерлин также перемещается в ядро и подавляет пролиферацию путем ингибирования убиквитинлигазы E3 CRL4 (DCAF1). [11] Наконец, самые последние исследования показали, что Мерлин также играет важную роль в регуляции энергетического метаболизма. [12] [13] Предполагается, что мутации NF2 приводят либо к неспособности синтезировать Мерлин, либо к выработке дефектного пептида, которому не хватает нормального опухолесупрессирующего эффекта. Шванномин-пептид состоит из 595 аминокислот . Сравнение шванномина с другими белками показывает сходство с белками, которые соединяют цитоскелет с клеточной мембраной . Считается, что мутации в гене Schwannomin изменяют движение и форму пораженных клеток с потерей контактного торможения. Эпендимомы — это опухоли, возникающие из эпендимы , эпителиоподобной ткани центральной нервной системы . [14] У людей с NF2 и эпендимомами функция подавления опухолей Мерлина может быть нарушена. Мутации потери функции, происходящие в хромосоме 22q , где кодируются белки Мерлина, могут способствовать онкогенезу.или создание новых опухолевых клеток. [6] Делеции в NH2-концевом домене белков мерлина также связаны с ранним возникновением опухоли и плохим прогнозом у больных людей. [6]



Так называемая акустическая неврома NF2 на самом деле является шванномой вестибулярного нерва, или вестибулярной шванномой. До сих пор часто используется неправильное название акустической невромы. Вестибулярные шванномы медленно растут у внутреннего входа внутреннего слухового прохода (meatus Acouscus Internus). Они происходят из нервных оболочек верхней части вестибулярного нерва в области между центральным и периферическим миелином (зона Оберштайнера-Редлиха) в области слухового поруса, на расстоянии 1 см от ствола мозга. [ нужна цитата ]
Многие люди с NF2 были включены в исследования, целью которых было сравнение типа и прогрессирования заболевания с точным определением связанной с ним мутации. Цель таких сравнений генотипа и фенотипа — определить, вызывают ли конкретные мутации соответствующие комбинации симптомов. Это было бы чрезвычайно ценно для прогнозирования прогрессирования заболевания и планирования терапии, начиная с молодого возраста. Результаты таких исследований следующие: [ нужна ссылка ]
Эти результаты позволяют предположить, что другие факторы (окружающая среда, другие мутации), вероятно, будут определять клинический исход.

NF2 является генетически передаваемым заболеванием. Диагноз чаще всего ставится в раннем взрослом возрасте (20–30 лет); однако его можно диагностировать раньше. NF2 можно диагностировать по наличию двусторонней вестибулярной шванномы или акустической невромы, которая вызывает потерю слуха, которая может начаться односторонне. [15] Если пациент не соответствует этому критерию диагноза, у него должен быть семейный анамнез НФ2, а также односторонняя вестибулярная шваннома и другие сопутствующие опухоли (менингиома черепа, шваннома черепного нерва, менингиома спинного мозга, эпендимома спинного мозга, поражение периферических нервов). опухоль, шваннома позвоночника, опухоль подкожной клетчатки, кожная бляшка). При этом более половины всех пациентов с диагнозом NF2 не имеют семейного анамнеза этого заболевания. [15] Хотя он еще не включен в клиническую классификацию, периферическая невропатия или повреждение периферических нервов, которое часто вызывает слабость, онемение и боль в руках и ногах, также может привести к диагнозу NF2. У детей NF2 может проявляться сходными симптомами, но обычно вызывает «нарушения зрения (катаракта, гамартомы), опухоли кожи, мононейропатию (парез лица, опущенная стопа), симптоматические опухоли спинного мозга или невестибулярные внутричерепные опухоли». [15]
Двусторонние вестибулярные шванномы являются диагностическими признаками NF2. [16]
Фернер и др. [17] приводят три набора диагностических критериев НФ2:
Другой набор диагностических критериев следующий :
Критерии со временем менялись. [18] Последний пересмотр критериев NF2 был сделан MJ Smith в 2017 году. Он включал рассмотрение мутации LZTR1 (шванноматоз) вместо NF2 и исключение двусторонних вестибулярных шванном, возникающих после 70 лет. [19]
Существует несколько различных хирургических методик удаления невриномы слухового нерва. [20] Выбор подхода определяется размером опухоли, слухом и общим клиническим состоянием человека.
Более крупные опухоли можно лечить транслабиринтным или ретросигмовидным доступом, в зависимости от опыта хирургической бригады. При больших опухолях вероятность сохранения слуха при любом подходе невелика. Когда слух уже плохой, транслабиринтный подход можно использовать даже при небольших опухолях. Небольшие латеральные опухоли у людей с НФ2 и хорошим слухом должны иметь доступ к средней ямке. Если опухоль расположена более медиально, лучше использовать ретросигмовидный доступ.
Декомпрессия слухового прохода — еще один хирургический метод, который может продлить слух, когда вестибулярная шваннома стала слишком большой, чтобы ее можно было удалить без повреждения улиткового нерва. При декомпрессии ВСА (внутреннего слухового прохода) используется доступ средней ямки, чтобы обнажить костную крышу ВСА без каких-либо попыток удалить опухоль. Кость, покрывающая слуховой нерв, удаляется, что позволяет опухоли распространиться вверх, в среднюю черепную ямку. Таким образом, давление на улитковый нерв снижается, что снижает риск дальнейшей потери слуха из-за прямого сдавления или обструкции кровоснабжения нерва.
Радиохирургия является консервативной альтернативой краниальной или другой внутричерепной хирургии. При использовании конформных радиохирургических методов терапевтическое излучение фокусируется на опухоли, не подвергая воздействию окружающие нормальные ткани. Хотя радиохирургия редко может полностью уничтожить опухоль, она часто может остановить ее рост или уменьшить ее размер. Хотя радиация наносит меньший непосредственный вред, чем обычная хирургия, она сопряжена с более высоким риском последующих злокачественных изменений в облученных тканях, и этот риск выше при NF2, чем при спорадических (не NF2) поражениях.
В настоящее время не существует рецептурных препаратов, предназначенных для снижения опухолевой нагрузки у пациентов с НФ2, хотя в исследованиях на пациентах бевацизумаб приводил к снижению скорости роста опухоли и улучшению слуха у некоторых пациентов. [21] [22]
Поскольку потеря слуха у людей с НФ2 обычно постепенная, в конечном итоге глубокая и нейросенсорная, лучшими вариантами лечения потери слуха являются кохлеарные имплантаты и слуховые стволовые имплантаты (ABI), а также дополнение слуха чтением по губам, речью с помощью сигналов или языком жестов. .
Кохлеарный имплантат — это электронное устройство, которое хирургическим путем имплантируется для стимуляции улиткового нерва. [23] Кохлеарные имплантаты будут работать только тогда, когда кохлеовестибулярный нерв (8-й нерв) и улитка все еще функционируют. В исследовании, проведенном Неффом и др. с использованием открытого и закрытого тестирования восприятия речи, они обнаружили, что использование кохлеарных имплантатов у пациентов с НФ2 позволяет значительно улучшить слуховые способности. [24] При тестировании распознавания предложений повседневной речи пять из шести пациентов набрали балл в пределах 90–100%, а при тестировании слуха в шумной обстановке четверо из шести пациентов получили балл в пределах 83–96%. [24] Кроме того, все испытания проводились без чтения по губам.
Слуховые имплантаты ствола мозга, или ABI, используются, когда улитка или какая-либо часть улитково-вестибулярного нерва не функционирует из-за повреждения этих областей или анатомических аномалий. [25] Процедура выполняется путем имплантации устройства, которое посылает электрический сигнал непосредственно в ядро улитки, позволяя звуку миновать периферическую слуховую систему и попасть прямо в ствол мозга. [ нужна цитата ]
NF2 является состоянием, ограничивающим жизнь. Это редкое генетическое заболевание, при котором возникают нераковые опухоли нервов, передающих баланс и звуковые импульсы от внутреннего уха к мозгу. На прогноз влияют ранний возраст, большее количество менингиом и шванном, а также снижение мутаций. [26]
Ранняя диагностика – лучший способ обеспечить улучшение лечения. Хотя даже при ранней диагностике некоторые пациенты все равно умирают очень молодыми. [ нужна цитата ]
Менингиомы и шванномы встречаются примерно у половины пациентов с НФ2. Менингиомы — это опухоли, которые бывают как внутричерепными, так и внутриспинномозговыми. Шванномы — это опухоли, которые часто локализуются во внутреннем слуховом проходе. Пациенты с NF2, у которых есть менингиомы, имеют более высокий риск смертности, и лечение может быть очень сложным. У людей, у которых развивается шваннома, часто развивается потеря слуха и глухота. [26] У этих людей также может развиться шум в ушах после односторонней потери слуха. Первым симптомом, с которым могут столкнуться люди, является головокружение или нарушение равновесия. [ нужна цитата ]
Усекательные мутации приводят к образованию более мелких и нефункциональных белковых продуктов. Исследования показали, что миссенс-мутации и крупные делеции могут вызывать преимущественно легкие фенотипы. Фенотип более изменчив у пациентов с мутациями в сайте сплайсинга и более легкое течение заболевания у пациентов с мутациями в экзонах 9–15. [26] Пациенты с миссенс-мутацией имеют более высокую выживаемость, чем нонсенс-мутации и мутации со сдвигом рамки считывания.
Частота заболевания составляет около 1 на 60 000. [27]
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) {{cite journal}}: Требуется цитировать журнал |journal=( помощь ){{cite book}}: |journal=игнорируется ( помощь )