Щавелоуксусная кислота (также известная как щавелевоуксусная кислота или ОАА ) представляет собой кристаллическое органическое соединение с химической формулой HO 2 CC(O)CH 2 CO 2 H. Щавелоуксусная кислота в форме сопряженного с ней основания оксалоацетата является промежуточным продуктом метаболизма во многих процессы, происходящие у животных. Он принимает участие в глюконеогенезе , цикле мочевины , глиоксилатном цикле , синтезе аминокислот , синтезе жирных кислот и цикле лимонной кислоты . [1]
Щавелосуксусная кислота подвергается последовательному депротонированию с образованием дианиона :
При высоком pH енолизируемый протон ионизируется:
Енольные формы щавелевоуксусной кислоты особенно стабильны. Кето-енольная таутомеризация катализируется ферментом оксалоацетаттаутомеразой . Транс -енол-оксалоацетат также появляется, когда тартрат является субстратом для фумаразы . [2]

Оксалоацетат в природе образуется несколькими способами. Основной путь – окисление L - малата , катализируемое малатдегидрогеназой , в цикле лимонной кислоты. Малат также окисляется сукцинатдегидрогеназой в медленной реакции, исходным продуктом которой является енол-оксалоацетат. [3]
Он также возникает в результате конденсации пирувата с угольной кислотой, вызванной гидролизом АТФ :
Происходя в мезофилле растений, этот процесс протекает через фосфоенолпируват , катализируемый фосфоенолпируваткарбоксилазой .
Оксалоацетат также может образовываться в результате транс- или дезаминирования аспарагиновой кислоты .
Оксалоацетат является промежуточным продуктом цикла лимонной кислоты , где он реагирует с ацетил-КоА с образованием цитрата , катализируемого цитратсинтазой . Он также участвует в глюконеогенезе , цикле мочевины , глиоксилатном цикле , синтезе аминокислот и синтезе жирных кислот . Оксалоацетат также является мощным ингибитором комплекса II .
Глюконеогенез [1] — метаболический путь, состоящий из серии одиннадцати ферментативно-катализируемых реакций, в результате которых образуется глюкоза из неуглеводных субстратов. Начало этого процесса происходит в митохондриальном матриксе , где находятся молекулы пирувата . Молекула пирувата карбоксилируется ферментом пируваткарбоксилазой , активируемым молекулой АТФ и воды. Эта реакция приводит к образованию оксалоацетата. НАДН восстанавливает оксалоацетат до малата . Эта трансформация необходима для транспортировки молекулы из митохондрий . Попав в цитозоль , малат снова окисляется до оксалоацетата с помощью НАД+. Тогда оксалоацетат остается в цитозоле, где и пройдут остальные реакции. Оксалоацетат позже декарбоксилируется и фосфорилируется фосфоенолпируваткарбоксикиназой и превращается в 2 -фосфоенолпируват с использованием гуанозинтрифосфата (GTP) в качестве источника фосфата. Глюкозу получают после дальнейшей переработки.
Цикл мочевины представляет собой метаболический путь, который приводит к образованию мочевины с использованием одной молекулы аммония из расщепленных аминокислот, другой группы аммония из аспартата и одной молекулы бикарбоната. [1] Этот путь обычно происходит в гепатоцитах . Реакции, связанные с циклом мочевины, производят НАДН , а НАДН можно получить двумя разными способами. Один из них использует оксалоацетат . В цитозоле имеются молекулы фумарата . Фумарат может превращаться в малат под действием фермента фумаразы . Малат под действием малатдегидрогеназы превращается в оксалоацетат, образуя молекулу НАДН. После этого оксалоацетат будет переработан в аспартат , поскольку трансаминазы предпочитают именно эти кетокислоты остальным. Эта рециркуляция поддерживает приток азота в клетку.

Глиоксилатный цикл является разновидностью цикла лимонной кислоты. [4] Это анаболический путь, происходящий в растениях и бактериях с использованием ферментов изоцитратлиазы и малатсинтазы . Некоторые промежуточные этапы цикла немного отличаются от цикла лимонной кислоты; тем не менее, оксалоацетат выполняет одну и ту же функцию в обоих процессах. [1] Это означает, что оксалоацетат в этом цикле также выступает в качестве основного реагента и конечного продукта. Фактически оксалоацетат является чистым продуктом глиоксилатного цикла, поскольку его петля цикла включает две молекулы ацетил-КоА.
На предыдущих стадиях ацетил-КоА переносится из митохондрий в цитоплазму, где находится синтаза жирных кислот . Ацетил-КоА транспортируется в виде цитрата, который ранее образовался в митохондриальном матриксе из ацетил-КоА и оксалоацетата. Эта реакция обычно инициирует цикл лимонной кислоты, но когда нет необходимости в энергии, она транспортируется в цитоплазму, где расщепляется до цитоплазматического ацетил-КоА и оксалоацетата.
Другая часть цикла требует НАДФН для синтеза жирных кислот. [5] Часть этой восстанавливающей способности генерируется, когда цитозольный оксалоацетат возвращается в митохондрии, пока внутренний митохондриальный слой непроницаем для оксалоацетата. Сначала оксалоацетат восстанавливается до малата с помощью НАДН. Затем малат декарбоксилируется до пирувата. Теперь этот пируват может легко проникать в митохондрии, где он снова карбоксилируется до оксалоацетата пируваткарбоксилазой. Таким образом, перенос ацетил-КоА из митохондрий в цитоплазму приводит к образованию молекулы НАДН. Общую реакцию, которая является спонтанной, можно резюмировать следующим образом:
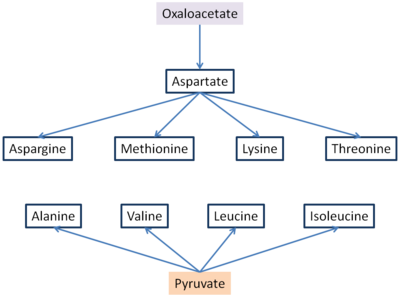
Шесть незаменимых аминокислот и три заменимые синтезируются из оксалоацетата и пирувата . [6] Аспартат и аланин образуются из оксалоацетата и пирувата соответственно путем переаминирования из глутамата . Аспарагин синтезируется путем амидирования аспартата, при этом глутамин отдает NH4. Это заменимые аминокислоты, и их простые пути биосинтеза встречаются во всех организмах. Метионин, треонин, лизин, изолейцин, валин и лейцин являются незаменимыми аминокислотами для человека и большинства позвоночных. Пути их биосинтеза у бактерий сложны и взаимосвязаны.
Оксалоацетат образует оксалат путем гидролиза. [7]
Этот процесс катализируется ферментом оксалоацетазой . Этот фермент встречается у растений, но неизвестен в животном мире. [8]