
Кислота Льюиса (названная в честь американского физико-химика Гилберта Н. Льюиса ) — это химическое вещество, содержащее пустую орбиталь , которая способна принимать электронную пару от основания Льюиса с образованием аддукта Льюиса . Таким образом, основание Льюиса — это любое вещество, имеющее заполненную орбиталь, содержащую электронную пару, которая не участвует в связывании , но может образовывать дативную связь с кислотой Льюиса с образованием аддукта Льюиса. Например, NH 3 является основанием Льюиса, поскольку он может отдавать свою неподеленную пару электронов. Триметилборан [(CH 3 ) 3 B] является кислотой Льюиса, поскольку он способен принимать неподеленную пару электронов. В аддукте Льюиса кислота Льюиса и основание делят электронную пару, предоставленную основанием Льюиса, образуя дативную связь. [1] В контексте конкретной химической реакции между NH 3 и Me 3 B, неподеленная пара из NH 3 будет образовывать дативную связь с пустой орбиталью Me 3 B, образуя аддукт NH 3 •BMe 3 . Терминология относится к вкладу Гилберта Н. Льюиса . [2]
Термины нуклеофил и электрофил иногда взаимозаменяемы с основанием Льюиса и кислотой Льюиса соответственно. Эти термины, особенно их абстрактные формы существительных нуклеофильность и электрофильность , подчеркивают кинетический аспект реакционной способности, в то время как основность Льюиса и кислотность Льюиса подчеркивают термодинамический аспект образования аддукта Льюиса. [3]
Во многих случаях взаимодействие между основанием Льюиса и кислотой Льюиса в комплексе обозначается стрелкой, указывающей на основание Льюиса, отдающее электроны кислоте Льюиса, с использованием обозначения дативной связи — например, Me 3 B ← NH 3 . В некоторых источниках основание Льюиса обозначается парой точек (явно отдаваемые электроны), что позволяет последовательно представить переход от самого основания к комплексу с кислотой:
Центральная точка может также использоваться для представления аддукта Льюиса, например Me 3 B·NH 3 . Другим примером является диэтилэфират трифторида бора , BF 3 ·Et 2 O . В несколько ином использовании центральная точка также используется для представления координации гидрата в различных кристаллах, например MgSO 4 ·7H 2 O для гидратированного сульфата магния , независимо от того, образует ли вода дативную связь с металлом.
Хотя были попытки использовать вычислительные и экспериментальные энергетические критерии для различения дативной связи от недативной ковалентной связи, [4] по большей части, различие просто отмечает источник электронной пары, и дативная связь, однажды образованная, ведет себя просто как другие ковалентные связи, хотя они, как правило, имеют значительный полярный характер. Более того, в некоторых случаях (например, сульфоксиды и аминооксиды как R 2 S → O и R 3 N → O ), использование стрелки дативной связи является просто нотационным удобством для избежания рисования формальных зарядов. В целом, однако, донорно-акцепторная связь рассматривается просто как нечто, находящееся где-то вдоль континуума между идеализированной ковалентной связью и ионной связью . [5]
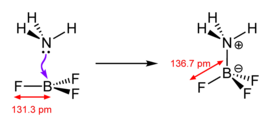
Кислоты Льюиса разнообразны, и этот термин используется свободно. Простейшими являются те, которые реагируют непосредственно с основанием Льюиса, такие как тригалогениды бора и пентагалогениды фосфора, мышьяка и сурьмы.
В том же духе, CH+3можно считать кислотой Льюиса в реакциях метилирования. Однако метильный катион никогда не встречается в виде свободного вида в конденсированной фазе, а реакции метилирования реагентами типа CH 3 I происходят посредством одновременного образования связи между нуклеофилом и углеродом и разрыва связи между углеродом и йодом (реакция S N 2). Учебники расходятся во мнениях по этому вопросу: некоторые утверждают, что алкилгалогениды являются электрофилами, но не кислотами Льюиса, [ 6] в то время как другие описывают алкилгалогениды (например, CH 3 Br) как тип кислоты Льюиса. [7] ИЮПАК утверждает, что кислоты Льюиса и основания Льюиса реагируют с образованием аддуктов Льюиса, [1] и определяет электрофил как кислоты Льюиса. [8]
Некоторые из наиболее изученных примеров таких кислот Льюиса — это тригалогениды бора и органобораны : [9]
В этом аддукте все четыре фторидных центра (точнее, лиганда ) эквивалентны.
Оба соединения BF 4 − и BF 3 OMe 2 являются продуктами присоединения оснований Льюиса трифторида бора.
Многие аддукты нарушают правило октета , например, трииодид- анион:
Изменчивость окраски растворов йода отражает различную способность растворителя образовывать аддукты с кислотой Льюиса I 2 .
Некоторые кислоты Льюиса связываются с двумя основаниями Льюиса, известным примером является образование гексафторсиликата :
Большинство соединений, считающихся кислотами Льюиса, требуют стадии активации перед образованием аддукта с основанием Льюиса. Сложные соединения, такие как Et 3 Al 2 Cl 3 и AlCl 3, рассматриваются как тригональные плоские кислоты Льюиса, но существуют в виде агрегатов и полимеров, которые должны быть разложены основанием Льюиса. [10] Более простой случай — образование аддуктов борана. Мономерный BH 3 не существует в заметном количестве, поэтому аддукты борана образуются путем разложения диборана:
В этом случае промежуточный продукт B 2 H−7может быть изолирован.
Многие комплексы металлов действуют как кислоты Льюиса, но обычно только после диссоциации более слабо связанного основания Льюиса, часто воды.
Протон (H + ) [11] является одной из самых сильных, но также и одной из самых сложных кислот Льюиса. Принято игнорировать тот факт, что протон сильно сольватирован (связан с растворителем ). Имея в виду это упрощение, кислотно-основные реакции можно рассматривать как образование аддуктов:
Типичным примером действия кислоты Льюиса является реакция алкилирования Фриделя-Крафтса . [5] Ключевым этапом является принятие AlCl 3 неподеленной пары ионов хлора, образуя AlCl−4и создание сильнокислотного, то есть электрофильного , карбоний-иона.
Основание Льюиса — это атомный или молекулярный вид, где наивысшая занятая молекулярная орбиталь (HOMO) сильно локализована. Типичные основания Льюиса — это обычные амины, такие как аммиак и алкиламины . Другие распространенные основания Льюиса включают пиридин и его производные. Некоторые из основных классов оснований Льюиса:
Наиболее распространенными основаниями Льюиса являются анионы. Сила основности Льюиса коррелирует с pK a исходной кислоты: кислоты с высоким pK a дают хорошие основания Льюиса. Как обычно, более слабая кислота имеет более сильное сопряженное основание .
Сила оснований Льюиса была оценена для различных кислот Льюиса, таких как I 2 , SbCl 5 и BF 3 . [12]
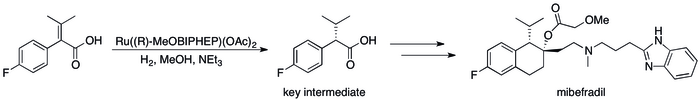
Почти все доноры электронных пар, которые образуют соединения путем связывания переходных элементов, можно рассматривать как лиганды . Таким образом, большое применение оснований Льюиса заключается в изменении активности и селективности металлических катализаторов . Хиральные основания Льюиса, как правило, многодентатные , придают хиральность катализатору, обеспечивая асимметричный катализ , что полезно для производства фармацевтических препаратов . Например, промышленный синтез антигипертензивного препарата мибефрадил использует хиральное основание Льюиса ( R -MeOBIPHEP). [13]
Кислоты и основания Льюиса обычно классифицируются по их твердости или мягкости. В этом контексте твердость подразумевает небольшие и неполяризуемые, а мягкость указывает на более крупные атомы, которые более поляризуемы.
Например, амин вытеснит фосфин из аддукта с кислотой BF 3 . Таким же образом можно классифицировать основания. Например, основания, отдающие неподеленную пару от атома кислорода, тверже, чем основания, отдающие через атом азота. Хотя классификация никогда не была количественно определена, она оказалась очень полезной для прогнозирования прочности образования аддукта, используя ключевые концепции, что взаимодействия жесткая кислота — жесткое основание и мягкая кислота — мягкое основание сильнее, чем взаимодействия жесткая кислота — мягкое основание или мягкая кислота — жесткое основание. Более позднее исследование термодинамики взаимодействия показало, что взаимодействия жесткая — жесткая энтальпийно выгодны, тогда как мягкие — мягкие энтропийно выгодны. [ необходима цитата ]
Было разработано много методов для оценки и прогнозирования кислотности Льюиса. Многие из них основаны на спектроскопических сигнатурах, таких как сдвиги сигналов ЯМР или ИК-полос, например, метод Гутмана-Беккета и метод Чайлдса [14] .
Модель ECW — это количественная модель, описывающая и предсказывающая прочность взаимодействий кислоты и основания Льюиса, −ΔH. Модель присваивает параметры E и C многим кислотам и основаниям Льюиса. Каждая кислота характеризуется E A и C A . Каждое основание также характеризуется своими собственными E B и C B . Параметры E и C относятся, соответственно, к электростатическому и ковалентному вкладу в прочность связей, которые образуют кислота и основание. Уравнение имеет вид
Член W представляет собой постоянный энергетический вклад для реакции кислота-основание, такой как расщепление димерной кислоты или основания. Уравнение предсказывает изменение кислотных и основных сил. Графические представления уравнения показывают, что не существует единого порядка сил оснований Льюиса или кислот Льюиса. [15] [16] и что шкалы отдельных свойств ограничены меньшим диапазоном кислот или оснований.
Концепция возникла у Гилберта Н. Льюиса, который изучал химическую связь . В 1923 году Льюис написал Кислотное вещество — это вещество, которое может использовать неподеленную электронную пару из другой молекулы для завершения стабильной группы одного из своих собственных атомов. [2] [17] Теория кислот и оснований Бренстеда –Лоури была опубликована в том же году. Эти две теории различны, но дополняют друг друга. Основание Льюиса также является основанием Бренстеда–Лоури, но кислота Льюиса не обязательно должна быть кислотой Бренстеда–Лоури. Классификация на жесткие и мягкие кислоты и основания ( теория HSAB ) последовала в 1963 году. Сила взаимодействий кислоты и основания Льюиса, измеряемая стандартной энтальпией образования аддукта, может быть предсказана с помощью двухпараметрического уравнения Драго–Вейланда.
В 1916 году Льюис предположил, что два атома удерживаются вместе в химической связи посредством совместного использования пары электронов. [18] Когда каждый атом вносит один электрон в связь, это называется ковалентной связью . Когда оба электрона исходят от одного из атомов, это называется дативной ковалентной связью или координатной связью . Различие не очень четкое. Например, при образовании иона аммония из аммиака и водорода молекула аммиака отдает пару электронов протону ; [ 11] идентичность электронов теряется в образующемся ионе аммония . Тем не менее, Льюис предположил, что донор электронной пары классифицируется как основание, а акцептор электронной пары классифицируется как кислота.
Более современное определение кислоты Льюиса — это атомный или молекулярный вид с локализованной пустой атомной или молекулярной орбиталью низкой энергии. Эта молекулярная орбиталь с самой низкой энергией ( LUMO ) может вместить пару электронов.
Основание Льюиса часто является основанием Бренстеда–Лоури, поскольку оно может отдавать пару электронов H + ; [11] протон является кислотой Льюиса, поскольку он может принимать пару электронов. Сопряженное основание кислоты Бренстеда–Лоури также является основанием Льюиса, поскольку потеря H + из кислоты оставляет те электроны, которые использовались для связи A—H, в качестве неподеленной пары на сопряженном основании. Однако основание Льюиса может быть очень трудно протонировать , но при этом все еще реагировать с кислотой Льюиса. Например, оксид углерода является очень слабым основанием Бренстеда–Лоури, но он образует сильный аддукт с BF 3 .
В другом сравнении кислотности Льюиса и Бренстеда-Лоури, проведенном Брауном и Каннером [19], 2,6-ди - третбутилпиридин реагирует с образованием гидрохлоридной соли с HCl, но не реагирует с BF 3 . Этот пример демонстрирует, что стерические факторы, в дополнение к факторам электронной конфигурации, играют роль в определении силы взаимодействия между объемным ди - третбутилпиридином и крошечным протоном.
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка )