Транспортер норадреналина ( NET ), также известный как транспортер норадреналина ( NAT ), представляет собой белок , который у людей кодируется геном 2 члена 2 семейства растворенных переносчиков 6 ( SLC6A2 ) . [5]
NET является переносчиком моноаминов и отвечает за зависимый от хлорида натрия обратный захват внеклеточного норадреналина (NE), который также известен как норадреналин . NET также может повторно захватывать внеклеточный дофамин (DA). Обратный захват этих двух нейромедиаторов важен для регулирования концентрации в синаптической щели . NET, наряду с другими переносчиками моноаминов, являются мишенью многих антидепрессантов и рекреационных наркотиков. Кроме того, переизбыток NET связан с СДВГ . [6] [7] Имеются доказательства того, что однонуклеотидный полиморфизм в гене NET ( SLC6A2 ) может быть основным фактором некоторых из этих нарушений. [7]
Ген переносчика норадреналина, SLC6A2, расположен в локусе 16q12.2 16 хромосомы человека. Этот ген кодируется 14 экзонами . [7] Судя по нуклеотидной и аминокислотной последовательности, транспортер NET состоит из 617 аминокислот с 12 трансмембранными доменами. Структурная организация NET очень гомологична другим членам натрий/хлорид-зависимого семейства транспортеров нейромедиаторов, включая транспортеры дофамина, адреналина, серотонина и ГАМК . [7]
Однонуклеотидный полиморфизм (SNP) — это генетическая вариация, при которой последовательность генома изменяется одним нуклеотидом ( A , T , C или G ). Белки NET с измененной аминокислотной последовательностью (точнее, миссенс-мутация ) потенциально могут быть связаны с различными заболеваниями, которые включают аномально высокие или низкие уровни норадреналина в плазме из-за измененной функции NET. NET SNP и возможные связи с различными заболеваниями являются предметом внимания многих исследовательских проектов. Имеются данные, свидетельствующие о связи между NET SNP и различными расстройствами, такими как СДВГ [7] [8] психические расстройства, [7] постуральная тахикардия [7] [9] и ортостатическая непереносимость . [7] [9] SNP rs3785143 и rs11568324 связаны с синдромом дефицита внимания и гиперактивности . [10] Однако на данный момент единственной подтвержденной прямой связью между SNP и клиническим состоянием является связь между SNP, Ala457Pro и ортостатической непереносимостью. [7] На данный момент обнаружено тринадцать миссенс-мутаций NET. [7]
Эпигенетический механизм (гиперметилирование CpG-островков в промоторной области гена NET) , который приводит к снижению экспрессии переносчика норадреналина (норадреналина) и, следовательно, к фенотипу нарушения нейронального обратного захвата норадреналина, вовлечен как в синдром постуральной ортостатической тахикардии , так и в паническое расстройство . [12]
rs5569 является вариантом SLC6A2. [13]

Транспортер норадреналина состоит из 12 трансмембранных доменов (TMD). Внутриклеточная часть содержит амино (- NH
2) группа и карбоксильная (-СООН) группа. Кроме того, существует большая внеклеточная петля, расположенная между TMD 3 и 4. [14] [6] [15] Белок состоит из 617 аминокислот . [14]
Функция NET заключается в транспортировке синаптически высвобождаемого норадреналина обратно в пресинаптический нейрон. До 90% высвободившегося норадреналина будет возвращено в клетку с помощью NET. NET функционирует путем сочетания притока натрия и хлорида (Na + /Cl - ) с транспортом норадреналина. Это происходит при фиксированном соотношении 1:1:1. [16] И NET, и транспортер дофамина (DAT) могут транспортировать норадреналин и дофамин. Обратный захват норадреналина и дофамина важен для регуляции концентрации моноаминовых нейротрансмиттеров в синаптической щели. Транспортер также помогает поддерживать гомеостатический баланс пресинаптического нейрона. [17]
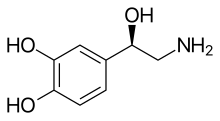
Норадреналин (НЭ) высвобождается норадренергическими нейронами, которые иннервируют как ЦНС , так и ПНС . НЭ, также известный как норадреналин (НА), играет важную роль в контроле настроения, возбуждения, памяти, обучения и восприятия боли. НЭ является частью симпатической нервной системы . [6] [18] Нарушение регуляции выведения норадреналина с помощью NET связано со многими нервно-психическими заболеваниями, обсуждаемыми ниже. Кроме того, многие антидепрессанты и рекреационные наркотики конкурируют за связывание NET с NE. [14]
Транспорт норадреналина обратно в пресинаптическую клетку возможен благодаря котранспорту с Na + и Cl - . Последовательное связывание ионов приводит к возможному обратному захвату норадреналина. Градиенты ионов Na + и Cl − делают этот обратный захват энергетически выгодным. Градиент создается Na+/K+-АТФазой , которая транспортирует три иона натрия и два иона калия в клетку. [17] NET имеют проводимость, аналогичную проводимости лиганд-управляемых ионных каналов . Выражение NET приводит к активности канала утечки. [16] [17]
NETs ограничены норадренергическими нейронами и отсутствуют на нейронах, которые выделяют дофамин или адреналин. [6] [15] [17] Транспортеры можно найти вдоль тела клетки, аксонов и дендритов нейрона. [6] NET расположены вдали от синапса, где высвобождается норадреналин. Они находятся ближе к плазматической мембране клетки. Это требует, чтобы норадреналин диффундировал из места, где он высвобождается, к транспортеру для обратного захвата. [17] Транспортеры норэпинефрина сосредоточены в нейронах симпатической системы, а также в нейронах, иннервирующих мозговое вещество надпочечников, легкие и плаценту. [17]
Регуляция функции NET сложна и находится в центре внимания текущих исследований. NET регулируются как на клеточном, так и на молекулярном уровне после трансляции. Наиболее изученные механизмы включают фосфорилирование протеинкиназой C второго мессенджера (PKC). [15] Было показано, что PKC ингибирует функцию NET путем секвестрации транспортера из плазматической мембраны. [19] Аминокислотная последовательность NET выявила несколько сайтов, связанных с фосфорилированием протеинкиназы. [17] Посттрансляционные модификации могут иметь широкий спектр эффектов на функцию NET, включая скорость слияния NET-содержащих везикул с плазматической мембраной и оборот транспортера. [19]
Ортостатическая непереносимость (ОИ) — заболевание вегетативной нервной системы (подкатегория дисавтономии ), характеризующееся появлением симптомов при вставании. Симптомы включают усталость, головокружение, головную боль, слабость, учащенное сердцебиение/учащенное сердцебиение , беспокойство и изменение зрения. [7] Часто у пациентов наблюдаются высокие концентрации норадреналина (НЭ) в плазме (не менее 600 пг/мл) по отношению к симпатическому оттоку при стоянии, что позволяет предположить, что ОИ является гиперадренергическим состоянием . [7] [9] Обнаружение однояйцевых сестер-близнецов, у которых обе были НО, позволило предположить генетическую основу этого расстройства. [7] [9] Была обнаружена миссенс -мутация гена NET (SLC6A2), при которой остаток аланина был заменен остатком пролина (Ala457Pro) в высококонсервативной области транспортера. [7] Дефектная NET пациентов имела только 2% активности версии гена дикого типа . [7] Генетический дефект белка NET приводит к снижению активности NET, что может объяснять аномально высокие уровни NE в плазме при ОИ. Однако у 40 других пациентов с ОИ не было такой же миссенс-мутации, что указывает на то, что другие факторы способствовали фенотипу однояйцевых близнецов. [7] Это открытие связи с мутациями NET, которое приводит к снижению активности обратного захвата норэпинефрина и ортостатической непереносимости, предполагает, что ошибочные механизмы поглощения NE могут способствовать сердечно-сосудистым заболеваниям. [20]
Ингибирование переносчика норадреналина (NET) имеет потенциальное терапевтическое применение при лечении синдрома дефицита внимания и гиперактивности (СДВГ), злоупотребления психоактивными веществами , нейродегенеративных расстройств (например, болезни Альцгеймера (БА) и болезни Паркинсона (БП)) и клинической депрессии . [18]


Некоторые антидепрессанты повышают уровень норадреналина, например , ингибиторы обратного захвата серотонина и норадреналина (SNRI), ингибиторы обратного захвата норадреналина и дофамина (NDRI), ингибиторы обратного захвата норадреналина (NRI или NERI) и трициклические антидепрессанты (TCA). Механизм действия этих препаратов заключается в том, что ингибиторы обратного захвата предотвращают обратный захват серотонина и норадреналина пресинаптическим нейроном , парализуя нормальную функцию NET. В то же время в синапсе сохраняется более высокий уровень 5-НТ , повышающий концентрацию последних нейротрансмиттеров. Поскольку переносчик норадреналина отвечает за большую часть клиренса дофамина в префронтальной коре [21] , SNRI также блокируют обратный захват дофамина, накапливая дофамин в синапсе. Однако DAT, основной способ транспортировки дофамина из клетки, может снижать концентрацию дофамина в синапсе, когда NET блокируется. [22] В течение многих лет выбором номер один при лечении расстройств настроения, таких как депрессия, было введение ТЦА, таких как дезипрамин (Норпрамин), нортриптилин (Арентил, Памелор), протриптилин (Вивактил) и амоксапин (Асендин). [18] СИОЗС, которые в основном регулируют серотонин, впоследствии заменили трициклики в качестве основного варианта лечения депрессии из-за их лучшей переносимости и меньшей частоты побочных эффектов. [23]
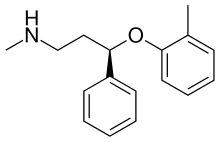
Существует множество лекарств для лечения СДВГ. Декстроамфетамин (декседрин, декстростат), аддералл , метилфенидат (риталин, метадат, концерта, дайтрана) и лиздексамфетамин (выванс) блокируют реабсорбцию катехоламинов дофамина и норадреналина через переносчики моноаминов (включая NET), тем самым повышая уровень этих нейротрансмиттеров в мозге. . Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило сильный селективный ингибитор обратного захвата норэпинефрина (NRI) атомоксетин (Strattera) для лечения СДВГ у взрослых. [24] [25] Роль NET при СДВГ аналогична тому, как она помогает облегчить симптомы депрессии. NET блокируется атомоксетином и повышает уровень NE в мозге. Он может улучшить способность сосредотачиваться, уменьшить импульсивность и гиперактивность как у детей, так и у взрослых с СДВГ. [26]
Кокаин является мощным психостимулятором и известен как одно из наиболее широко используемых веществ в рекреационных целях. [27] Кокаин является неселективным ингибитором обратного захвата переносчиков норадреналина , серотонина и дофамина . Это препятствует абсорбции этих химических веществ в пресинаптическое окончание [27] и позволяет большой концентрации дофамина, серотонина и норадреналина накапливаться в синаптической щели. Считается, что потенциальная зависимость от кокаина является результатом его воздействия на транспортеры дофамина в ЦНС, в то время как было высказано предположение, что опасные для жизни сердечно-сосудистые эффекты кокаина могут включать ингибирование НЭО в симпатических и вегетативных синапсах ЦНС. [28]
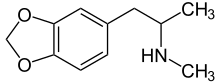
Амфетамины оказывают такое же влияние на уровень норадреналина , как и кокаин , поскольку оба они повышают уровень норадреналина в мозге. [29] Амфетаминоподобные препараты являются субстратами для переносчиков моноаминов , включая NET, которые вызывают изменение направления транспорта нейромедиаторов. [17] [30] Амфетамины вызывают большое накопление внеклеточных НЭ. [29] Высокие уровни НЭ в головном мозге являются причиной большинства глубоких эффектов амфетаминов, включая бдительность и аноректические, локомоторные и симпатомиметические эффекты. [29] Однако воздействие амфетаминов на мозг происходит медленнее, но длится дольше, чем воздействие кокаина на мозг. [29] МДМА (3,4-метилендиоксиметамфетамин или «экстази») представляет собой амфетамин, широко используемый в рекреационных целях. Исследование показало, что ингибитор NET ребоксетин снижает стимулирующее действие МДМА на людей, демонстрируя решающую роль NET в сердечно-сосудистых и стимулирующих эффектах МДМА. [31]
Роль NET при многих заболеваниях головного мозга лежит в основе важности понимания (дис)регуляции транспортера. Полная модель белков, связанных с транспортером, будет полезна при разработке лекарственной терапии таких заболеваний, как шизофрения , аффективные расстройства и вегетативные расстройства. Недавно открытые механизмы NET, включая способность действовать обратимо и в качестве ионного канала, открывают новые области исследований. [15] [17]

Роль НЭ при шизофрении до конца не изучена, но стимулировала исследования по этой теме. [32] [33] [34] [35] Единственная взаимосвязь, которая была понята между исследователями, заключается в том, что существует положительная корреляция между повышенными уровнями NE в мозге и спинномозговой жидкости (СМЖ) и активностью шизофрении. [32] [33] [34] [35] В одном исследовании было показано, что клонидин , препарат, используемый для лечения таких заболеваний, как СДВГ и высокое кровяное давление, вызывает значительное снижение уровня MHPG (3-метокси-4) в плазме. -гидроксифенилгликоль), метаболит НЭ, в нормальной контрольной группе, но не в группе больных шизофренией. [34] Это говорит о том, что при шизофрении альфа-2-адренергический рецептор , пресинаптический тормозной рецептор, может быть менее чувствительным по сравнению с нормально функционирующими альфа-2-рецепторами и, таким образом, связан с повышенными уровнями NE при заболевании. [34] Помимо повышенного уровня NE в мозге и спинномозговой жидкости, повышенный уровень MHPG также связан с диагнозом шизофрении. [35] Нарушение регуляции NE при шизофрении было областью интереса исследователей, и исследования по этой теме все еще продолжаются. [34] [35]
С помощью метода позитронно-эмиссионной томографии был выборочно исследован NET. 11C ME@HAPTHI и 18F-MeNER — два селективных радиоиндикатора NET для ПЭТ-визуализации. [36] Флуоресцентные субстраты для транспортера также можно использовать для мониторинга скорости переноса в изолированных органах или тканях, [37] [38], хотя они не подходят для клинической визуализации.