Дофамин ( DA , сокращение от 3,4- дигидроксифенетиламина ) — это нейромодуляторная молекула , которая играет несколько важных ролей в клетках. Это органическое химическое вещество из семейств катехоламинов и фенэтиламинов . Дофамин составляет около 80 % содержания катехоламинов в мозге. Это амин , синтезируемый путем удаления карбоксильной группы из молекулы его предшественника , L-ДОФА , который синтезируется в мозге и почках. Дофамин также синтезируется в растениях и большинстве животных. В мозге дофамин функционирует как нейромедиатор — химическое вещество, выделяемое нейронами (нервными клетками) для отправки сигналов другим нервным клеткам. Нейромедиаторы синтезируются в определенных областях мозга, но системно влияют на многие области. Мозг включает в себя несколько различных дофаминовых путей , один из которых играет важную роль в мотивационном компоненте поведения, мотивированного вознаграждением . Ожидание большинства видов вознаграждений увеличивает уровень дофамина в мозге, [4] и многие наркотические вещества, вызывающие привыкание , увеличивают высвобождение дофамина или блокируют его обратный захват в нейроны после высвобождения. [5] Другие пути дофамина в мозге участвуют в контроле движений и в контроле высвобождения различных гормонов. Эти пути и группы клеток образуют систему дофамина, которая является нейромодуляторной . [5]
В популярной культуре и средствах массовой информации дофамин часто изображается как основное химическое вещество удовольствия, но в настоящее время в фармакологии существует мнение, что дофамин вместо этого придает мотивационную значимость ; [6] [7] [8] другими словами, дофамин сигнализирует о воспринимаемой мотивационной значимости (т. е. желательности или отвращения) результата, что, в свою очередь, направляет поведение организма к достижению этого результата или от него. [8] [9]
За пределами центральной нервной системы дофамин действует в основном как локальный паракринный мессенджер. В кровеносных сосудах он подавляет высвобождение норадреналина и действует как вазодилататор ; в почках он увеличивает выведение натрия и диуреза; в поджелудочной железе он снижает выработку инсулина; в пищеварительной системе он снижает моторику желудочно-кишечного тракта и защищает слизистую оболочку кишечника ; а в иммунной системе он снижает активность лимфоцитов . За исключением кровеносных сосудов, дофамин в каждой из этих периферических систем синтезируется локально и оказывает свое действие вблизи клеток, которые его выделяют.
Несколько важных заболеваний нервной системы связаны с дисфункциями дофаминовой системы, и некоторые из ключевых лекарств, используемых для их лечения, работают, изменяя эффекты дофамина. Болезнь Паркинсона , дегенеративное состояние, вызывающее тремор и двигательные нарушения, вызвано потерей нейронов, секретирующих дофамин, в области среднего мозга, называемой черной субстанцией . Его метаболический предшественник L-ДОФА может быть изготовлен; Леводопа , чистая форма L-ДОФА, является наиболее широко используемым средством лечения болезни Паркинсона. Существуют доказательства того, что шизофрения связана с измененными уровнями активности дофамина, и большинство антипсихотических препаратов, используемых для ее лечения, являются антагонистами дофамина , которые снижают активность дофамина. [10] Подобные препараты-антагонисты дофамина также являются одними из самых эффективных средств против тошноты . Синдром беспокойных ног и синдром дефицита внимания и гиперактивности (СДВГ) связаны со снижением активности дофамина. [11] Дофаминергические стимуляторы могут вызывать привыкание в больших дозах, но некоторые из них используются в меньших дозах для лечения СДВГ. Сам дофамин доступен в виде готового лекарства для внутривенных инъекций . Он полезен при лечении тяжелой сердечной недостаточности или кардиогенного шока . [12] У новорожденных его можно использовать при гипотонии и септическом шоке . [13]
Молекула дофамина состоит из катехольной структуры ( бензольное кольцо с двумя гидроксильными боковыми группами) с одной аминогруппой , присоединенной через этиловую цепь. [14] Таким образом, дофамин является простейшим возможным катехоламином , семейством, которое также включает нейромедиаторы норадреналин и адреналин . [15] Наличие бензольного кольца с этим присоединением амина делает его замещенным фенэтиламином , семейством, которое включает многочисленные психоактивные препараты . [16]
Как и большинство аминов , дофамин является органическим основанием . [17] Как основание , он обычно протонируется в кислой среде (в кислотно-щелочной реакции ). [17] Протонированная форма хорошо растворима в воде и относительно стабильна, но может окисляться при воздействии кислорода или других окислителей . [17] В основных средах дофамин не протонируется. [17] В этой форме свободного основания он менее растворим в воде, а также более реакционноспособен. [17] Из-за повышенной стабильности и растворимости в воде протонированной формы дофамин поставляется для химического или фармацевтического использования в виде гидрохлорида дофамина , то есть гидрохлоридной соли , которая образуется при соединении дофамина с соляной кислотой . [17] В сухом виде гидрохлорид дофамина представляет собой мелкий порошок от белого до желтого цвета. [18]
Дофамин синтезируется в ограниченном наборе типов клеток, в основном в нейронах и клетках мозгового вещества надпочечников . [ 22] Первичные и второстепенные метаболические пути соответственно следующие:
Прямой предшественник дофамина, L -ДОФА , может быть синтезирован косвенно из незаменимой аминокислоты фенилаланина или напрямую из заменимой аминокислоты тирозина . [25] Эти аминокислоты содержатся почти в каждом белке и поэтому легкодоступны в пище, причем тирозин является наиболее распространенным. Хотя дофамин также содержится во многих видах пищи, он не способен пересекать гематоэнцефалический барьер , который окружает и защищает мозг. [26] Поэтому он должен синтезироваться внутри мозга, чтобы выполнять свою нейронную активность . [26]
L -фенилаланин преобразуется в L -тирозин ферментом фенилаланингидроксилазой с молекулярным кислородом (O2 ) и тетрагидробиоптерином в качестве кофакторов . L -тирозин преобразуется в L -ДОФА ферментом тирозингидроксилазой с тетрагидробиоптерином, O2 и железом (Fe2 + ) в качестве кофакторов. [25] L -ДОФА преобразуется в дофамин ферментом ароматической декарбоксилазой L -аминокислот (также известной как ДОФА-декарбоксилаза) с пиридоксальфосфатом в качестве кофактора. [25]
Дофамин сам по себе используется в качестве предшественника в синтезе нейротрансмиттеров норадреналина и адреналина. [25] Дофамин преобразуется в норадреналин ферментом дофамин β-гидроксилазой с O 2 и L -аскорбиновой кислотой в качестве кофакторов. [25] Норадреналин преобразуется в адреналин ферментом фенилэтаноламин N -метилтрансферазой с S -аденозил -L -метионином в качестве кофактора. [25]
Некоторые из кофакторов также требуют собственного синтеза. [25] Дефицит любой необходимой аминокислоты или кофактора может нарушить синтез дофамина, норадреналина и адреналина. [25]
Дофамин расщепляется на неактивные метаболиты набором ферментов — моноаминоксидазы (МАО), катехол -О -метилтрансферазы (КОМТ) и альдегиддегидрогеназы (АЛДГ), действующих последовательно. [27] Обе изоформы моноаминоксидазы, МАО-А и МАО-В , эффективно метаболизируют дофамин. [25] Существуют различные пути распада, но основным конечным продуктом является гомованилиновая кислота (ГВК), которая не имеет известной биологической активности. [27] Из кровотока гомованилиновая кислота отфильтровывается почками, а затем выводится с мочой. [27] Два основных метаболических пути, которые преобразуют дофамин в ГВК: [28]
В клинических исследованиях шизофрении измерения гомованилиновой кислоты в плазме использовались для оценки уровней активности дофамина в мозге. Однако сложность этого подхода заключается в разделении высокого уровня гомованилиновой кислоты в плазме, обусловленного метаболизмом норадреналина. [29] [30]
Хотя дофамин обычно расщепляется ферментом оксидоредуктазой , он также подвержен окислению путем прямой реакции с кислородом, в результате чего образуются хиноны и различные свободные радикалы в качестве продуктов. [31] Скорость окисления может быть увеличена за счет присутствия трехвалентного железа или других факторов. Хиноны и свободные радикалы, образующиеся при аутоокислении дофамина, могут отравлять клетки , и есть доказательства того, что этот механизм может способствовать потере клеток, которая происходит при болезни Паркинсона и других состояниях. [32]
Дофамин оказывает свое действие, связываясь с рецепторами клеточной поверхности и активируя их . [22] У людей дофамин обладает высокой аффинностью связывания с дофаминовыми рецепторами и человеческим рецептором следовых аминов 1 (hTAAR1). [3] [33] У млекопитающих было идентифицировано пять подтипов дофаминовых рецепторов , обозначенных от D1 до D5 . [22] Все они функционируют как метаботропные рецепторы , сопряженные с G-белком , что означает, что они оказывают свое действие через сложную систему вторичных мессенджеров . [34] Эти рецепторы можно разделить на два семейства, известные как D1 - подобные и D2 - подобные . [22] Для рецепторов, расположенных на нейронах нервной системы, конечным эффектом активации D1 - подобных (D1 и D5 ) может быть возбуждение (через открытие натриевых каналов ) или торможение (через открытие калиевых каналов ); конечным эффектом активации, подобной D 2 (D 2 , D 3 и D 4 ), обычно является ингибирование целевого нейрона. [34] Следовательно, неправильно описывать сам дофамин как возбуждающий или ингибирующий: его воздействие на целевой нейрон зависит от того, какие типы рецепторов присутствуют на мембране этого нейрона и от внутренних реакций этого нейрона на вторичный мессенджер цАМФ . [34] Рецепторы D 1 являются наиболее многочисленными рецепторами дофамина в нервной системе человека; рецепторы D 2 следуют за ними; рецепторы D 3 , D 4 и D 5 присутствуют на значительно более низких уровнях. [34]
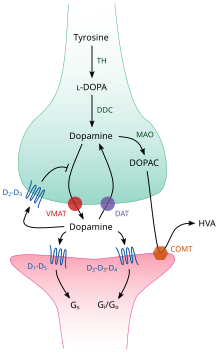
Внутри мозга дофамин функционирует как нейротрансмиттер и нейромодулятор и контролируется набором механизмов, общих для всех моноаминовых нейротрансмиттеров . [22] После синтеза дофамин транспортируется из цитозоля в синаптические пузырьки с помощью переносчика растворенного вещества — везикулярного транспортера моноаминов , VMAT2 . [35] Дофамин хранится в этих пузырьках до тех пор, пока не будет выброшен в синаптическую щель . В большинстве случаев высвобождение дофамина происходит посредством процесса, называемого экзоцитозом , который вызывается потенциалами действия , но он также может быть вызван активностью внутриклеточного рецептора, связанного с следовыми аминами , TAAR1 . [33] TAAR1 — это высокоаффинный рецептор для дофамина, следовых аминов и некоторых замещенных амфетаминов , который расположен вдоль мембран во внутриклеточной среде пресинаптической клетки; [33] Активация рецептора может регулировать передачу сигналов дофамина, вызывая ингибирование обратного захвата дофамина и его отток , а также ингибируя нейронную активность посредством разнообразного набора механизмов. [33] [36]
Попав в синапс, дофамин связывается с дофаминовыми рецепторами и активирует их. [37] Это могут быть постсинаптические дофаминовые рецепторы, которые расположены на дендритах (постсинаптический нейрон), или пресинаптические ауторецепторы (например, рецепторы D 2 sh и пресинаптические D 3 ), которые расположены на мембране терминали аксона (пресинаптический нейрон). [22] [37] После того, как постсинаптический нейрон вызывает потенциал действия, молекулы дофамина быстро отсоединяются от своих рецепторов. Затем они поглощаются обратно в пресинаптическую клетку посредством обратного захвата, опосредованного либо переносчиком дофамина , либо переносчиком моноаминов плазматической мембраны . [38] Вернувшись в цитозоль, дофамин может быть либо расщеплен моноаминоксидазой , либо переупакован в везикулы с помощью VMAT2, что делает его доступным для будущего высвобождения. [35]
В мозге уровень внеклеточного дофамина модулируется двумя механизмами: фазической и тонической передачей . [39] Фазовое высвобождение дофамина, как и большинство высвобождений нейротрансмиттеров в нервной системе, напрямую управляется потенциалами действия в клетках, содержащих дофамин. [39] Тоническая передача дофамина происходит, когда небольшие количества дофамина высвобождаются без предшествующих пресинаптических потенциалов действия. [39] Тоническая передача регулируется различными факторами, включая активность других нейронов и обратный захват нейротрансмиттеров. [39]

Внутри мозга дофамин играет важную роль в исполнительных функциях , контроле движений , мотивации , возбуждении , подкреплении и вознаграждении , а также в функциях более низкого уровня, включая лактацию , сексуальное удовлетворение и тошноту . Группы дофаминергических клеток и пути составляют дофаминергическую систему, которая является нейромодуляторной .
Дофаминергические нейроны (нервные клетки, вырабатывающие дофамин) сравнительно немногочисленны — в общей сложности около 400 000 в человеческом мозге [40] — и их клеточные тела ограничены группами в нескольких относительно небольших областях мозга. [41] Однако их аксоны проецируются во многие другие области мозга, и они оказывают мощное воздействие на свои цели. [41] Эти группы дофаминергических клеток были впервые картированы в 1964 году Анникой Дальстрём и Кьеллом Фуксе, которые дали им обозначения, начинающиеся с буквы «А» (от «аминергический»). [42] На их схеме области с A1 по A7 содержат нейромедиатор норадреналин, тогда как с A8 по A14 содержат дофамин. Дофаминергические области, которые они идентифицировали, — это черная субстанция (группы 8 и 9); вентральная область покрышки (группа 10); задний гипоталамус (группа 11); дугообразное ядро (группа 12); неопределенная зона (группа 13) и перивентрикулярное ядро (группа 14). [42]
Черная субстанция — это небольшая область среднего мозга, которая является компонентом базальных ганглиев . Она состоит из двух частей — входной области, называемой pars reticulata , и выходной области, называемой pars compacta . Дофаминергические нейроны находятся в основном в pars compacta (группа клеток A8) и рядом (группа A9). [41] У людей проекция дофаминергических нейронов из substantia nigra pars compacta в дорсальный стриатум, называемая нигростриатным путем , играет важную роль в контроле двигательной функции и в обучении новым двигательным навыкам . [43] Эти нейроны особенно уязвимы для повреждений, и когда большое их количество погибает, результатом становится паркинсонический синдром . [44]
Вентральная область покрышки (VTA) — это еще одна область среднего мозга. Наиболее заметная группа дофаминергических нейронов VTA проецируется в префронтальную кору через мезокортикальный путь , а другая, меньшая группа, проецируется в прилежащее ядро через мезолимбический путь . Вместе эти два пути называются мезокортиколимбической проекцией . [41] [43] VTA также посылает дофаминергические проекции в миндалевидное тело , поясную извилину , гиппокамп и обонятельную луковицу . [41] [43] Мезокортиколимбические нейроны играют центральную роль в вознаграждении и других аспектах мотивации. [43] Накапливающаяся литература показывает, что дофамин также играет решающую роль в аверсивном обучении посредством его воздействия на ряд областей мозга. [45] [46] [47]
В заднем гипоталамусе есть дофаминовые нейроны, которые проецируются в спинной мозг, но их функция не до конца изучена. [48] Есть некоторые свидетельства того, что патология в этой области играет роль в синдроме беспокойных ног, состоянии, при котором люди испытывают трудности со сном из-за непреодолимой потребности постоянно двигать частями тела, особенно ногами. [48]
Дугообразное ядро и перивентрикулярное ядро гипоталамуса имеют дофаминовые нейроны, которые образуют важную проекцию — тубероинфундибулярный путь , который идет к гипофизу , где он влияет на секрецию гормона пролактина . [49] Дофамин является основным нейроэндокринным ингибитором секреции пролактина из передней доли гипофиза . [49] Дофамин, вырабатываемый нейронами в дугообразном ядре, секретируется в гипофизарную портальную систему срединного возвышения , которая снабжает гипофиз . [49] Пролактиновые клетки , которые вырабатывают пролактин, в отсутствие дофамина секретируют пролактин непрерывно; дофамин ингибирует эту секрецию. [49]
Неопределенная зона, сгруппированная между дугообразным и перивентрикулярным ядрами, проецируется в несколько областей гипоталамуса и участвует в регуляции гонадотропин-рилизинг-гормона , который необходим для активации развития мужской и женской репродуктивной системы после полового созревания. [49]
Дополнительная группа нейронов, секретирующих дофамин, находится в сетчатке глаза. [50] Эти нейроны являются амакриновыми клетками , что означает, что у них нет аксонов. [50] Они выделяют дофамин во внеклеточную среду и особенно активны в дневные часы, замолкая ночью. [50] Этот ретинальный дофамин усиливает активность колбочек сетчатки, подавляя палочки — в результате повышается чувствительность к цвету и контрасту в условиях яркого света за счет снижения чувствительности при тусклом свете. [50]

Самыми крупными и важными источниками дофамина в мозге позвоночных являются черная субстанция и вентральная область покрышки. [41] Обе структуры являются компонентами среднего мозга, тесно связаны друг с другом и функционально схожи во многих отношениях. [41] Самым крупным компонентом базальных ганглиев является полосатое тело. [51] Черная субстанция посылает дофаминергическую проекцию в дорсальный полосатый участок , в то время как вентральная область покрышки посылает аналогичный тип дофаминергической проекции в вентральный полосатый участок . [41]
Прогресс в понимании функций базальных ганглиев был медленным. [51] Наиболее популярные гипотезы, в широком смысле, предполагают, что базальные ганглии играют центральную роль в выборе действия . [52] Теория выбора действия в своей простейшей форме предполагает, что когда человек или животное находится в ситуации, когда возможны несколько вариантов поведения, активность в базальных ганглиях определяет, какой из них будет выполнен, освобождая эту реакцию от торможения, продолжая при этом тормозить другие двигательные системы, которые, если будут активированы, сгенерируют конкурирующее поведение. [53] Таким образом, базальные ганглии, в этой концепции, отвечают за инициирование поведения, но не за определение деталей того, как оно выполняется. Другими словами, они по сути образуют систему принятия решений. [53]
Базальные ганглии можно разделить на несколько секторов, каждый из которых участвует в контроле определенных типов действий. [54] Вентральный сектор базальных ганглиев (содержащий вентральный полосатый участок и вентральную область покрышки) работает на самом высоком уровне иерархии, выбирая действия на уровне всего организма. [53] Дорсальные секторы (содержащие дорсальный полосатый участок и черную субстанцию) работают на более низких уровнях, выбирая определенные мышцы и движения, которые используются для реализации заданной модели поведения. [54]
Дофамин вносит вклад в процесс выбора действия по крайней мере двумя важными способами. Во-первых, он устанавливает «порог» для инициирования действий. [52] Чем выше уровень активности дофамина, тем ниже импульс, необходимый для вызова данного поведения. [52] Как следствие, высокий уровень дофамина приводит к высокому уровню двигательной активности и импульсивному поведению ; низкий уровень дофамина приводит к оцепенению и замедленным реакциям. [52] Болезнь Паркинсона, при которой уровень дофамина в контуре черной субстанции значительно снижен, характеризуется скованностью и трудностью инициирования движения — однако, когда люди с этим заболеванием сталкиваются с сильными стимулами, такими как серьезная угроза, их реакции могут быть такими же энергичными, как и у здорового человека. [55] В противоположном направлении, препараты, которые увеличивают высвобождение дофамина, такие как кокаин или амфетамин, могут вызывать повышенный уровень активности, включая, в крайнем случае, психомоторное возбуждение и стереотипные движения . [56]
Вторым важным эффектом дофамина является его «обучающий» сигнал. [52] Когда действие сопровождается повышением активности дофамина, контур базальных ганглиев изменяется таким образом, что тот же ответ легче вызвать, когда в будущем возникнут похожие ситуации. [52] Это форма оперантного обусловливания , в которой дофамин играет роль сигнала вознаграждения. [53]

На языке, используемом для обсуждения системы вознаграждения, вознаграждение — это привлекательное и мотивационное свойство стимула, которое вызывает аппетитное поведение (также известное как поведение приближения) и потребительское поведение . [57] Вознаграждающий стимул — это стимул, который может побудить организм приблизиться к нему и выбрать его потребление. [57] Удовольствие , обучение (например, классическое и оперантное обусловливание ) и поведение приближения — три основные функции вознаграждения. [57] Как аспект вознаграждения, удовольствие дает определение вознаграждения; [57] однако, хотя все приятные стимулы являются вознаграждениями, не все вознаграждающие стимулы являются приятными (например, внешние вознаграждения, такие как деньги). [57] [58] Мотивационный или желательный аспект вознаграждающих стимулов отражается в поведении приближения, которое они вызывают, тогда как удовольствие от внутренних вознаграждений возникает в результате их потребления после получения. [57] Нейропсихологическая модель, которая различает эти два компонента внутренне вознаграждающего стимула, — это модель значимости стимула , где «желание» или стремление (реже «поиск» [59] ) соответствует аппетитному или приближающему поведению, в то время как «симпатия» или удовольствие соответствуют потребительскому поведению. [57] [6] [60] У людей, страдающих наркотической зависимостью , «желание» становится диссоциированным от «симпатии», поскольку желание использовать вызывающий привыкание наркотик возрастает, в то время как удовольствие, получаемое от его потребления, уменьшается из-за толерантности к наркотику . [6]
В мозге дофамин частично функционирует как глобальный сигнал вознаграждения. Первоначальный ответ дофамина на стимул вознаграждения кодирует информацию о значимости , ценности и контексте вознаграждения. [57] В контексте обучения, связанного с вознаграждением, дофамин также функционирует как сигнал ошибки предсказания вознаграждения , то есть степени, в которой ценность вознаграждения является неожиданной. [57] Согласно этой гипотезе, предложенной Монтегю, Даяном и Сейновски, [61] ожидаемые вознаграждения не вызывают вторую фазовую реакцию дофамина в определенных дофаминергических клетках, но вознаграждения, которые являются неожиданными или больше ожидаемых, вызывают кратковременное увеличение синаптического дофамина, тогда как пропуск ожидаемого вознаграждения фактически приводит к падению выброса дофамина ниже фонового уровня. [57] Гипотеза «ошибки прогнозирования» привлекла особый интерес со стороны вычислительных нейробиологов, поскольку влиятельный метод вычислительного обучения, известный как обучение на основе временных различий, активно использует сигнал, кодирующий ошибку прогнозирования. [57] Это слияние теории и данных привело к плодотворному взаимодействию между нейробиологами и компьютерными учеными, интересующимися машинным обучением . [57]
Данные микроэлектродных записей из мозга животных показывают, что дофаминовые нейроны в вентральной области покрышки (VTA) и черной субстанции сильно активируются широким спектром событий вознаграждения. [57] Эти реагирующие на вознаграждение дофаминовые нейроны в VTA и черной субстанции имеют решающее значение для связанного с вознаграждением познания и служат центральным компонентом системы вознаграждения. [6] [62] [63] Функция дофамина различается в каждой аксональной проекции от VTA и черной субстанции; [6] например, проекция VTA– ядро прилежащего ядра назначает стимульную значимость («хочу») поощрительным стимулам и связанным с ними сигналам , проекция VTA– префронтальная кора обновляет значение различных целей в соответствии с их стимульной значимостью, проекции VTA–миндалина и VTA–гиппокамп опосредуют консолидацию воспоминаний, связанных с вознаграждением, и как пути VTA– ядро прилежащего ядра , так и пути черная субстанция–дорсальный стриатум участвуют в обучении двигательным реакциям, которые облегчают получение поощрительных стимулов. [6] [64] Некоторая активность в дофаминергических проекциях VTA, по-видимому, также связана с прогнозированием вознаграждения. [6] [64]
В то время как дофамин играет центральную роль в возникновении «желания», связанного с аппетитными или поведенческими реакциями приближения к поощрительным стимулам, подробные исследования показали, что дофамин нельзя просто приравнять к гедонистической «симпатии» или удовольствию, что отражается в поведенческой реакции потребления. [58] Нейротрансмиссия дофамина участвует в некоторых, но не во всех аспектах познания, связанного с удовольствием, поскольку центры удовольствия были идентифицированы как в системе дофамина (т. е. в оболочке прилежащего ядра), так и за ее пределами (т. е. в вентральном бледном шаре и парабрахиальном ядре ). [58] [60] [65] Например, прямая электрическая стимуляция дофаминовых путей с использованием электродов, имплантированных в мозг, воспринимается как удовольствие, и многие виды животных готовы работать, чтобы получить его. [66] Антипсихотические препараты снижают уровень дофамина и, как правило, вызывают ангедонию , сниженную способность испытывать удовольствие. [67] Многие виды приятных ощущений, такие как половой акт, еда и видеоигры, увеличивают выброс дофамина. [68] Все наркотические вещества, вызывающие привыкание, напрямую или косвенно влияют на нейротрансмиссию дофамина в прилежащем ядре; [6] [66] эти вещества усиливают «желание» наркотиков, что приводит к компульсивному употреблению наркотиков при многократном приеме в высоких дозах, предположительно через сенсибилизацию стимула-заметности . [60] Препараты, которые увеличивают концентрацию дофамина в синаптических связях, включают психостимуляторы, такие как метамфетамин и кокаин. Они вызывают усиление «желающего» поведения, но не сильно изменяют выражение удовольствия или уровень насыщения. [60] [66] Однако опиатные вещества, такие как героин и морфин, вызывают усиление выражений «симпатичного» и «желающего» поведения. [60] Более того, животные, у которых вентральная тегментальная дофаминовая система стала неактивной, не ищут пищу и умрут от голода, если их предоставить самим себе, но если положить им в рот еду, они ее съедят и покажут выражения, указывающие на удовольствие. [69]
Клиническое исследование, проведенное в январе 2019 года, в котором оценивалось влияние предшественника дофамина ( леводопы ), антагониста дофамина ( рисперидона ) и плацебо на реакцию вознаграждения на музыку, включая степень удовольствия, испытываемого во время музыкального озноба , измеряемую по изменениям электродермальной активности , а также субъективным оценкам, показало, что манипулирование нейротрансмиссией дофамина двунаправленно регулирует познание удовольствия (в частности, гедонистическое воздействие музыки ) у людей. [70] [71] Это исследование продемонстрировало, что повышенная нейротрансмиссия дофамина действует как непременное условие для приятных гедонистических реакций на музыку у людей. [70] [71]
Исследование, опубликованное в журнале Nature в 1998 году, обнаружило доказательства того, что игра в видеоигры высвобождает дофамин в полосатом теле человека. Этот дофамин связан с обучением, подкреплением поведения, вниманием и сенсомоторной интеграцией. [72] Исследователи использовали сканирование позитронно-эмиссионной томографии и меченый 11 C раклоприд для отслеживания уровней дофамина в мозге во время целенаправленных двигательных задач и обнаружили, что высвобождение дофамина положительно коррелировало с выполнением задач и было наибольшим в вентральном полосатом теле . Это было первое исследование, продемонстрировавшее поведенческие условия, при которых дофамин высвобождается у людей. Оно подчеркивает способность позитронно-эмиссионной томографии обнаруживать потоки нейротрансмиттеров во время изменений в поведении. Согласно исследованию, потенциально проблемное использование видеоигр связано с такими чертами личности, как низкая самооценка и низкая самоэффективность, тревожность, агрессия и клинические симптомы депрессии и тревожных расстройств. [73] Кроме того, причины, по которым люди играют в видеоигры, различаются и могут включать совладание , социализацию и личное удовлетворение. DSM -5 определяет интернет-игровое расстройство как психическое расстройство, тесно связанное с игровым расстройством. Это было поддержано некоторыми исследователями, но также вызвало споры.
Дофамин не пересекает гематоэнцефалический барьер, поэтому его синтез и функции в периферических областях в значительной степени независимы от его синтеза и функций в мозге. [26] Значительное количество дофамина циркулирует в кровотоке, но его функции там не совсем ясны. [27] Дофамин обнаруживается в плазме крови на уровнях, сопоставимых с уровнями адреналина, но у людей более 95% дофамина в плазме находится в форме сульфата дофамина , конъюгата, вырабатываемого ферментом сульфотрансферазой 1A3/1A4, действующим на свободный дофамин. [27] Основная часть этого сульфата дофамина вырабатывается в брыжеечных органах. [ 27] Считается, что выработка сульфата дофамина является механизмом детоксикации дофамина, который поступает в организм с пищей или вырабатывается в процессе пищеварения — его уровни в плазме обычно повышаются более чем в пятьдесят раз после еды. [27] Сульфат дофамина не имеет известных биологических функций и выводится с мочой. [27]
Относительно небольшое количество неконъюгированного дофамина в кровотоке может вырабатываться симпатической нервной системой , пищеварительной системой или, возможно, другими органами. [27] Он может действовать на рецепторы дофамина в периферических тканях или метаболизироваться, или преобразовываться в норадреналин ферментом дофамин бета-гидроксилазой , который выделяется в кровоток мозговым веществом надпочечников. [27] Некоторые рецепторы дофамина расположены в стенках артерий, где они действуют как вазодилататор и ингибитор высвобождения норадреналина из постганглионарных симпатических нервных окончаний (дофамин может ингибировать высвобождение норадреналина, воздействуя на пресинаптические рецепторы дофамина, а также на пресинаптические рецепторы α-1, как и сам норадреналин). [74] Эти реакции могут быть активированы дофамином, высвобождаемым из каротидного тельца в условиях низкого содержания кислорода, но неизвестно, выполняют ли артериальные дофаминергические рецепторы другие биологически полезные функции. [74]
Помимо своей роли в регуляции кровотока, существует несколько периферических систем, в которых дофамин циркулирует в ограниченной области и выполняет экзокринную или паракринную функцию. [27] Периферические системы, в которых дофамин играет важную роль, включают иммунную систему , почки и поджелудочную железу .
В иммунной системе дофамин действует на рецепторы, присутствующие на иммунных клетках, особенно лимфоцитах . [75] Дофамин также может влиять на иммунные клетки в селезенке , костном мозге и кровеносной системе . [76] Кроме того, дофамин может синтезироваться и высвобождаться самими иммунными клетками. [75] Основное действие дофамина на лимфоциты заключается в снижении уровня их активации. Функциональное значение этой системы неясно, но она предоставляет возможный путь для взаимодействия между нервной системой и иммунной системой и может иметь отношение к некоторым аутоиммунным расстройствам. [76]
Почечная дофаминергическая система расположена в клетках нефрона в почке, где присутствуют все подтипы дофаминовых рецепторов. [77] Дофамин также синтезируется там, клетками канальцев , и выбрасывается в канальцевую жидкость . Его действия включают увеличение кровоснабжения почек, увеличение скорости клубочковой фильтрации и увеличение выведения натрия с мочой. Следовательно, дефекты функции почечного дофамина могут привести к снижению выведения натрия и, следовательно, к развитию высокого кровяного давления . Существуют веские доказательства того, что сбои в производстве дофамина или в рецепторах могут привести к ряду патологий, включая окислительный стресс , отек и либо генетическую, либо эссенциальную гипертонию. Окислительный стресс сам по себе может вызывать гипертонию. [78] Дефекты в системе также могут быть вызваны генетическими факторами или высоким кровяным давлением. [79]
В поджелудочной железе роль дофамина довольно сложна. Поджелудочная железа состоит из двух частей: экзокринной и эндокринной . Экзокринная часть синтезирует и секретирует пищеварительные ферменты и другие вещества, включая дофамин, в тонкую кишку. [80] Функция этого секретируемого дофамина после того, как он попадает в тонкую кишку, четко не установлена — возможные варианты включают защиту слизистой оболочки кишечника от повреждения и снижение моторики желудочно-кишечного тракта (скорости, с которой содержимое движется через пищеварительную систему). [80]
Островки поджелудочной железы составляют эндокринную часть поджелудочной железы, синтезируют и секретируют гормоны, включая инсулин , в кровоток. [80] Имеются данные о том, что бета-клетки в островках, которые синтезируют инсулин, содержат рецепторы дофамина, и что дофамин действует, уменьшая количество инсулина, которое они выделяют. [80] Источник поступления дофамина в них точно не установлен — он может исходить от дофамина, циркулирующего в кровотоке и вырабатываемого симпатической нервной системой, или он может синтезироваться локально другими типами клеток поджелудочной железы. [80]

Дофамин как лекарственное средство продается под торговыми наименованиями Intropin, Dopastat и Revimine, среди прочих. Он включен в Список основных лекарственных средств Всемирной организации здравоохранения . [81] Он чаще всего используется в качестве стимулирующего препарата при лечении сильного пониженного кровяного давления , замедленного сердечного ритма и остановки сердца . Он особенно важен при лечении этих состояний у новорожденных . [82] [13] Он вводится внутривенно. Поскольку период полураспада дофамина в плазме очень короткий — приблизительно одна минута у взрослых, две минуты у новорожденных и до пяти минут у недоношенных детей — его обычно вводят в виде непрерывной внутривенной капельницы, а не одной инъекции. [83]
Его эффекты, в зависимости от дозировки, включают увеличение выделения натрия почками, увеличение диуреза, увеличение частоты сердечных сокращений и повышение артериального давления . [83] В низких дозах он действует через симпатическую нервную систему, увеличивая силу сокращения сердечной мышцы и частоту сердечных сокращений, тем самым увеличивая сердечный выброс и артериальное давление. [84] Более высокие дозы также вызывают вазоконстрикцию , которая еще больше повышает артериальное давление. [84] [85] В более старой литературе также описываются очень низкие дозы, которые, как считается, улучшают функцию почек без других последствий, но недавние обзоры пришли к выводу, что дозы на таких низких уровнях неэффективны и иногда могут быть вредными. [86] Хотя некоторые эффекты являются результатом стимуляции дофаминовых рецепторов, выраженные сердечно-сосудистые эффекты являются результатом действия дофамина на α 1 , β 1 и β 2 адренорецепторы . [87] [88]
Побочные эффекты дофамина включают отрицательное воздействие на функцию почек и нерегулярное сердцебиение . [84] Было обнаружено, что LD 50 или летальная доза, которая, как ожидается, окажется смертельной для 50% популяции, составляет: 59 мг/кг (мышь; вводится внутривенно ) ; 95 мг/кг (мышь; вводится внутрибрюшинно ); 163 мг/кг (крыса; вводится внутрибрюшинно); 79 мг/кг (собака; вводится внутривенно). [89]
Система дофамина играет центральную роль в нескольких важных медицинских состояниях, включая болезнь Паркинсона , синдром дефицита внимания и гиперактивности , синдром Туретта , шизофрению , биполярное расстройство и зависимость . Помимо самого дофамина, существует множество других важных препаратов, которые действуют на системы дофамина в различных частях мозга или тела. Некоторые из них используются в медицинских или рекреационных целях, но нейрохимики также разработали множество исследовательских препаратов, некоторые из которых связываются с высоким сродством с определенными типами рецепторов дофамина и либо агонизируют , либо противодействуют их эффектам, и многие из них влияют на другие аспекты физиологии дофамина, [90] включая ингибиторы транспортера дофамина , ингибиторы VMAT и ингибиторы ферментов .
В ряде исследований сообщалось о связанном с возрастом снижении синтеза дофамина и плотности рецепторов дофамина (т. е. количества рецепторов) в мозге. [91] Было показано, что это снижение происходит в полосатом теле и экстрастриарных областях. [92] Уменьшение рецепторов D 1 , D 2 и D 3 хорошо документировано. [93] [94] [95] Считается, что снижение дофамина с возрастом является причиной многих неврологических симптомов, частота которых увеличивается с возрастом, таких как уменьшение размаха руками и повышенная ригидность . [96] Изменения уровня дофамина также могут вызывать возрастные изменения когнитивной гибкости. [96]
Исследования показали, что дисбаланс дофамина влияет на утомляемость при рассеянном склерозе . [97] У пациентов с рассеянным склерозом дофамин подавляет выработку ИЛ-17 и ИФН-γ мононуклеарными клетками периферической крови. [98]
Болезнь Паркинсона — это возрастное расстройство, характеризующееся двигательными расстройствами , такими как скованность тела, замедление движений и дрожание конечностей, когда они не используются. [55] На поздних стадиях она прогрессирует до слабоумия и в конечном итоге до смерти. [55] Основные симптомы вызваны потерей клеток, секретирующих дофамин, в черной субстанции. [99] Эти клетки дофамина особенно уязвимы для повреждений, а различные инсульты, включая энцефалит (как показано в книге и фильме «Пробуждение »), повторяющиеся сотрясения, связанные со спортом , и некоторые формы химического отравления, такие как MPTP , могут привести к значительной потере клеток, вызывая паркинсонический синдром , который по своим основным признакам похож на болезнь Паркинсона. [100] Однако большинство случаев болезни Паркинсона являются идиопатическими , что означает, что причину гибели клеток определить невозможно. [100]
Наиболее широко используемым методом лечения паркинсонизма является введение L-ДОФА, метаболического предшественника дофамина. [26] L-ДОФА преобразуется в дофамин в мозге и различных частях тела ферментом ДОФА-декарбоксилазой. [25] L-ДОФА используется вместо самого дофамина, поскольку, в отличие от дофамина, он способен пересекать гематоэнцефалический барьер . [26] Его часто вводят совместно с ингибитором фермента периферического декарбоксилирования , таким как карбидопа или бенсеразид , чтобы уменьшить количество, преобразуемое в дофамин на периферии, и тем самым увеличить количество L-ДОФА, которое поступает в мозг. [26] Когда L-ДОФА вводят регулярно в течение длительного периода времени, часто начинают появляться различные неприятные побочные эффекты, такие как дискинезия ; тем не менее, он считается наилучшим доступным вариантом долгосрочного лечения для большинства случаев болезни Паркинсона. [26]
Лечение L-ДОФА не может восстановить дофаминовые клетки, которые были утрачены, но оно заставляет оставшиеся клетки вырабатывать больше дофамина, тем самым компенсируя потерю по крайней мере в некоторой степени. [26] На поздних стадиях лечение начинает терпеть неудачу, потому что потеря клеток настолько серьезна, что оставшиеся не могут вырабатывать достаточно дофамина независимо от уровней L-ДОФА. [26] Другие препараты, которые усиливают функцию дофамина, такие как бромокриптин и перголид , также иногда используются для лечения паркинсонизма, но в большинстве случаев L-ДОФА, по-видимому, дает наилучший компромисс между положительными эффектами и отрицательными побочными эффектами. [26]
Дофаминергические препараты, которые используются для лечения болезни Паркинсона, иногда связаны с развитием синдрома нарушения регуляции дофамина , который включает в себя чрезмерное использование дофаминергических препаратов и вызванное лекарствами компульсивное вовлечение в естественные вознаграждения , такие как азартные игры и сексуальная активность. [101] [102] Последнее поведение похоже на то, которое наблюдается у людей с поведенческой зависимостью . [101]

Кокаин , замещенные амфетамины (включая метамфетамин ), Аддералл , метилфенидат (продается как Риталин или Концерта ) и другие психостимуляторы оказывают свое действие в первую очередь или частично за счет повышения уровня дофамина в мозге с помощью различных механизмов. [103] Кокаин и метилфенидат являются блокаторами транспортера дофамина или ингибиторами обратного захвата ; [104] они неконкурентно ингибируют обратный захват дофамина, что приводит к повышению концентрации дофамина в синаптической щели. [105] [106] : 54–58 Подобно кокаину, замещенные амфетамины и амфетамин также повышают концентрацию дофамина в синаптической щели , но с помощью других механизмов. [36] [106] : 147–150
Эффекты психостимуляторов включают увеличение частоты сердечных сокращений, температуры тела и потоотделения; улучшение бдительности, внимания и выносливости; увеличение удовольствия, получаемого от вознаграждающих событий; но при более высоких дозах возбуждение, беспокойство или даже потеря контакта с реальностью . [103] Препараты этой группы могут иметь высокий потенциал привыкания из-за их активирующего воздействия на систему вознаграждения, опосредованную дофамином, в мозге. [103] Однако некоторые из них также могут быть полезны в более низких дозах для лечения синдрома дефицита внимания и гиперактивности (СДВГ) и нарколепсии . [107] [108] Важным отличительным фактором является начало и продолжительность действия. [103] Кокаин может подействовать за считанные секунды, если его вводят инъекцией или вдыхают в форме свободного основания; эффект длится от 5 до 90 минут. [109] Это быстрое и кратковременное действие делает его эффекты легко воспринимаемыми и, следовательно, дает ему высокий потенциал привыкания. [103] Метилфенидат, принимаемый в форме таблеток, напротив, может достичь пиковых уровней в кровотоке за два часа, [107] и в зависимости от формулы эффект может длиться до 12 часов. [110] Эти более длительно действующие формулы имеют преимущество в снижении вероятности злоупотребления и улучшении приверженности лечению за счет использования более удобных схем дозировки. [111]

Различные наркотические вещества вызывают увеличение активности дофамина, связанной с вознаграждением. [103] Такие стимуляторы, как никотин , кокаин и метамфетамин, способствуют повышению уровня дофамина, который, по-видимому, является основным фактором, вызывающим зависимость. Для других наркотических веществ, таких как опиоидный героин, повышенный уровень дофамина в системе вознаграждения может играть лишь незначительную роль в возникновении зависимости. [112] Когда люди, пристрастившиеся к стимуляторам, переживают абстинентный синдром, они не испытывают физических страданий, связанных с отменой алкоголя или опиатов; вместо этого они испытывают тягу, сильное желание наркотика, характеризующееся раздражительностью, беспокойством и другими симптомами возбуждения, [113] вызванными психологической зависимостью .
Система дофамина играет решающую роль в нескольких аспектах зависимости. На самой ранней стадии генетические различия, которые изменяют экспрессию дофаминовых рецепторов в мозге, могут предсказать, будут ли стимуляторы привлекательными или отталкивающими для человека. [114] Потребление стимуляторов приводит к повышению уровня дофамина в мозге, которое длится от нескольких минут до нескольких часов. [103] Наконец, хроническое повышение уровня дофамина, которое происходит при повторном потреблении высоких доз стимуляторов, запускает широкий спектр структурных изменений в мозге, которые отвечают за поведенческие отклонения, характерные для зависимости. [115] Лечение зависимости от стимуляторов очень сложно, потому что даже если потребление прекращается, тяга, которая приходит с психологической отменой, остается. [113] Даже когда тяга, кажется, угасла, она может возникнуть снова при столкновении со стимулами, которые связаны с наркотиком, такими как друзья, места и ситуации. [113] Ассоциативные сети в мозге сильно взаимосвязаны. [116]
В начале 1950-х годов психиатры обнаружили, что класс препаратов, известных как типичные антипсихотики (также известных как основные транквилизаторы ), часто эффективен для уменьшения психотических симптомов шизофрении. [117] Введение первого широко используемого антипсихотика, хлорпромазина (Торазина), в 1950-х годах привело к освобождению многих пациентов с шизофренией из учреждений в последующие годы. [117] К 1970-м годам исследователи поняли, что эти типичные антипсихотики действуют как антагонисты на рецепторы D2 . [ 117] [118] Это осознание привело к так называемой дофаминовой гипотезе шизофрении , которая постулирует, что шизофрения в значительной степени вызвана гиперактивностью дофаминовых систем мозга. [119] Дофаминовая гипотеза получила дополнительную поддержку из наблюдения, что психотические симптомы часто усиливались стимуляторами, усиливающими дофамин, такими как метамфетамин, и что эти препараты также могли вызывать психоз у здоровых людей, если их принимать в достаточно больших дозах. [119] В последующие десятилетия были разработаны другие атипичные антипсихотики , которые имели меньше серьезных побочных эффектов. [117] Многие из этих новых препаратов не действуют напрямую на рецепторы дофамина, а вместо этого вызывают изменения в активности дофамина косвенно. [120] Эти препараты также использовались для лечения других психозов. [117] Антипсихотические препараты оказывают широкое подавляющее действие на большинство типов активного поведения и, в частности, уменьшают бредовое и возбужденное поведение, характерное для явного психоза. [118]
Однако более поздние наблюдения привели к тому, что гипотеза дофамина утратила популярность, по крайней мере в ее простой первоначальной форме. [119] Во-первых, у пациентов с шизофренией обычно не наблюдается заметного повышения уровня активности дофамина в мозге. [119] Несмотря на это, многие психиатры и нейробиологи продолжают считать, что шизофрения связана с какой-то дисфункцией дофаминовой системы. [117] Однако по мере того, как «гипотеза дофамина» развивалась с течением времени, виды дисфункций, которые она постулирует, становились все более тонкими и сложными. [117]
Психофармаколог Стивен М. Шталь предположил в обзоре 2018 года, что во многих случаях психоза, включая шизофрению, три взаимосвязанные сети, основанные на дофамине, серотонине и глутамате — каждая по отдельности или в различных комбинациях — способствуют перевозбуждению дофаминовых рецепторов D2 в вентральном полосатом теле . [121]
Измененная нейротрансмиссия дофамина связана с синдромом дефицита внимания и гиперактивности (СДВГ), состоянием, связанным с нарушением когнитивного контроля , что в свою очередь приводит к проблемам с регулированием внимания ( контроль внимания ), подавлением поведения ( ингибиторный контроль ), забыванием вещей или потерей деталей ( рабочая память ) и другими проблемами. [122] Существуют генетические связи между рецепторами дофамина, транспортером дофамина и СДВГ, в дополнение к связям с другими рецепторами и транспортерами нейротрансмиттеров. [123] Наиболее важная связь между дофамином и СДВГ связана с препаратами, которые используются для лечения СДВГ. [124] Некоторые из наиболее эффективных терапевтических средств для лечения СДВГ являются психостимуляторами, такими как метилфенидат (Риталин, Концерта) и амфетамин (Эвекео, Аддералл, Декседрин), препараты, которые повышают уровни как дофамина, так и норадреналина в мозге. [124] Клинические эффекты этих психостимуляторов при лечении СДВГ опосредуются посредством непрямой активации рецепторов дофамина и норадреналина, в частности рецептора дофамина D 1 и адренорецептора α 2 в префронтальной коре. [122] [125] [126]
Дофамин играет роль в обработке боли на нескольких уровнях центральной нервной системы, включая спинной мозг, околоводопроводное серое вещество , таламус , базальные ганглии и поясную кору . [127] Снижение уровня дофамина связано с болевыми симптомами, которые часто возникают при болезни Паркинсона. [127] Нарушения в дофаминергической нейротрансмиссии также возникают при нескольких болезненных клинических состояниях, включая синдром жжения во рту , фибромиалгию и синдром беспокойных ног. [127]
Тошнота и рвота в значительной степени определяются активностью в area postrema в продолговатом мозге ствола мозга , в области, известной как триггерная зона хеморецепторов . [128] Эта область содержит большую популяцию рецепторов дофамина типа D2 . [ 128] Следовательно, препараты, активирующие рецепторы D2 , имеют высокий потенциал вызывать тошноту. [128] В эту группу входят некоторые лекарства, которые назначаются при болезни Паркинсона, а также другие агонисты дофамина , такие как апоморфин . [129] В некоторых случаях антагонисты рецепторов D2, такие как метоклопрамид , полезны в качестве препаратов от тошноты . [128]
Страх и тревога
Одновременная позитронно-эмиссионная томография (ПЭТ) и функциональная магнитно-резонансная томография (фМРТ) показали, что количество высвобожденного дофамина зависит от силы условной реакции страха и линейно связано с активностью миндалевидного тела, вызванной обучением [130] . Дофамин, как правило, связан с обучением на основе вознаграждения, но он также играет ключевую роль в обучении страху и его исчезновении, помогая формировать, хранить и обновлять воспоминания о страхе посредством взаимодействия с другими областями мозга, такими как миндалевидное тело, вентромедиальная префронтальная кора и полосатое тело. [131]
Нет никаких сообщений о дофамине в археях , но он был обнаружен в некоторых типах бактерий и в простейших, называемых Tetrahymena . [132] Возможно, что еще более важно, существуют типы бактерий, которые содержат гомологи всех ферментов, которые животные используют для синтеза дофамина. [133] Было высказано предположение, что животные получили свой аппарат синтеза дофамина от бактерий посредством горизонтального переноса генов , который мог произойти относительно поздно в эволюционном времени, возможно, в результате симбиотического включения бактерий в эукариотические клетки, что дало начало митохондриям . [133]
Дофамин используется в качестве нейротрансмиттера у большинства многоклеточных животных. [134] У губок есть только одно сообщение о наличии дофамина, без указания его функции; [135] однако, дофамин был зарегистрирован в нервной системе многих других радиально-симметричных видов, включая книдарийных медуз , гидру и некоторые кораллы . [136] Это датирует возникновение дофамина как нейротрансмиттера к самому раннему появлению нервной системы, более 500 миллионов лет назад в кембрийский период. Дофамин функционирует как нейротрансмиттер у позвоночных , иглокожих , членистоногих , моллюсков и нескольких типов червей . [137] [138]
У каждого типа животных, которые были исследованы, дофамин, как было замечено, изменяет двигательное поведение. [134] В модельном организме , нематоде Caenorhabditis elegans , он снижает локомоцию и увеличивает движения, направленные на поиск пищи; у плоских червей он производит «винтообразные» движения; у пиявок он подавляет плавание и способствует ползанию. У широкого круга позвоночных дофамин оказывает «активирующее» действие на переключение поведения и выбор реакции, сопоставимое с его действием у млекопитающих. [134] [139]
Дофамин также последовательно демонстрирует свою роль в обучении вознаграждению во всех группах животных. [134] Как и у всех позвоночных, беспозвоночные, такие как круглые черви , плоские черви , моллюски и обычные плодовые мушки, могут быть обучены повторять действие, если за ним последовательно следует повышение уровня дофамина. [134] У плодовых мушек отдельные элементы обучения вознаграждению предполагают модульную структуру системы обработки вознаграждения насекомых, которая в целом аналогична структуре млекопитающих. [140] Например, дофамин регулирует краткосрочное и долгосрочное обучение у обезьян; [141] у плодовых мушек различные группы дофаминовых нейронов опосредуют сигналы вознаграждения для краткосрочных и долгосрочных воспоминаний. [142]
Долгое время считалось, что членистоногие являются исключением из этого правила, и дофамин рассматривался как оказывающий неблагоприятное воздействие. Вместо этого вознаграждение, как считалось, опосредуется октопамином , нейротрансмиттером, тесно связанным с норадреналином. [143] Однако более поздние исследования показали, что дофамин действительно играет роль в обучении вознаграждению у плодовых мушек. Также было обнаружено, что вознаграждающий эффект октопамина обусловлен активацией им набора дофаминергических нейронов, ранее не доступных в исследовании. [143]

Многие растения, включая различные пищевые растения, синтезируют дофамин в разной степени. [144] Самые высокие концентрации наблюдаются в бананах — мякоть плодов красных и желтых бананов содержит дофамин на уровне от 40 до 50 частей на миллион по весу. [144] Картофель, авокадо, брокколи и брюссельская капуста также могут содержать дофамин на уровне 1 части на миллион или более; апельсины, помидоры, шпинат, фасоль и другие растения содержат измеримые концентрации менее 1 части на миллион. [144] Дофамин в растениях синтезируется из аминокислоты тирозина с помощью биохимических механизмов, аналогичных тем, которые используют животные. [144] Он может метаболизироваться различными способами, производя меланин и различные алкалоиды в качестве побочных продуктов. [144] Функции растительных катехоламинов четко не установлены, но есть доказательства того, что они играют роль в ответе на стрессоры, такие как бактериальная инфекция, действуют как факторы, способствующие росту в некоторых ситуациях, и изменяют способ метаболизма сахаров. Рецепторы, которые опосредуют эти действия, еще не идентифицированы, как и внутриклеточные механизмы, которые они активируют. [144]
Дофамин, потребляемый с пищей, не может воздействовать на мозг, поскольку он не может преодолеть гематоэнцефалический барьер. [26] Однако есть также множество растений, которые содержат L-ДОФА, метаболический предшественник дофамина. [145] Самые высокие концентрации обнаружены в листьях и стручках растений рода Mucuna , особенно в Mucuna pruriens (бархатные бобы), которые использовались в качестве источника L-ДОФА как лекарственного средства. [146] Другое растение, содержащее значительные количества L-ДОФА, — это Vicia faba , растение, которое производит конские бобы (также известные как «широкие бобы»). Однако уровень L-ДОФА в бобах намного ниже, чем в оболочках стручков и других частях растения. [147] Семена деревьев Cassia и Bauhinia также содержат значительные количества L-ДОФА. [145]
В виде морских зеленых водорослей Ulvaria obscura , основного компонента некоторых цветущих водорослей , дофамин присутствует в очень высоких концентрациях, оцениваемых в 4,4% от сухого веса. Есть доказательства того, что этот дофамин действует как защита от травоядных , снижая потребление улитками и изоподами . [148]
Меланины — это семейство темнопигментированных веществ, встречающихся во многих организмах. [149] Химически они тесно связаны с дофамином, и существует тип меланина, известный как дофамин-меланин , который может синтезироваться путем окисления дофамина с помощью фермента тирозиназы . [149] Меланин, который темнеет человеческую кожу, не относится к этому типу: он синтезируется путем, который использует L-ДОФА в качестве предшественника, но не дофамин. [149] Однако имеются существенные доказательства того, что нейромеланин , который придает темный цвет черной субстанции мозга, по крайней мере частично является дофамином-меланином. [150]
Дофаминовый меланин, вероятно, также появляется, по крайней мере, в некоторых других биологических системах. Часть дофамина в растениях, вероятно, используется в качестве предшественника дофамина-меланина. [151] Сложные узоры, которые появляются на крыльях бабочек, а также черно-белые полосы на телах личинок насекомых, как полагают, также вызваны пространственно структурированными накоплениями дофамина-меланина. [152]
Дофамин был впервые синтезирован в 1910 году Джорджем Баргером и Джеймсом Юэнсом в лабораториях Wellcome в Лондоне, Англия [153] и впервые идентифицирован в человеческом мозге Катариной Монтегю в 1957 году. Он был назван дофамином, потому что это моноамин , предшественником которого в синтезе Баргера-Юэнса является 3,4- дигидроксифенилаланин ( леводопа или L-ДОФА). Функция дофамина как нейромедиатора была впервые обнаружена в 1958 году Арвидом Карлссоном и Нильсом-Оке Хилларпом в Лаборатории химической фармакологии Национального института сердца Швеции . [154] Карлссон был удостоен Нобелевской премии по физиологии и медицине 2000 года за то, что показал , что дофамин является не только предшественником норэпинефрина (норадреналина) и эпинефрина (адреналина), но и сам по себе является нейромедиатором. [155]
Исследования, мотивированные адгезивными полифенольными белками в мидиях , привели к открытию в 2007 году, что широкий спектр материалов, если их поместить в раствор дофамина при слегка щелочном pH , покроется слоем полимеризованного дофамина, часто называемого полидофамином . [156] [157] Этот полимеризованный дофамин образуется в результате спонтанной реакции окисления и формально является типом меланина. [158] Кроме того, самополимеризация дофамина может быть использована для модуляции механических свойств гелей на основе пептидов. [159] Синтез полидофамина обычно включает реакцию гидрохлорида дофамина с трисом в качестве основания в воде. Структура полидофамина неизвестна. [157]
Полидофаминовые покрытия могут образовываться на объектах размером от наночастиц до больших поверхностей. [158] Полидофаминовые слои обладают химическими свойствами, которые потенциально могут быть чрезвычайно полезными, и многочисленные исследования изучали их возможные применения. [158] На самом простом уровне их можно использовать для защиты от повреждения светом или для формирования капсул для доставки лекарств. [158] На более сложном уровне их адгезивные свойства могут сделать их полезными в качестве субстратов для биосенсоров или других биологически активных макромолекул. [158]
Таким образом, стимулы, вызывающие страх, способны по-разному изменять фазовую передачу дофамина через субрегионы NAcc. Авторы предполагают, что наблюдаемое усиление дофамина оболочки NAcc, вероятно, отражает общую мотивационную значимость, возможно, из-за облегчения состояния страха, вызванного CS, когда US (электрошок стопы) не применяется. Это рассуждение подтверждается отчетом Будыгина и его коллег112
,
показывающим, что у анестезированных крыс прекращение ущипывания хвоста приводит к усиленному высвобождению дофамина в оболочке.
: L-фенилаланин + тетрагидробиоптерин + O2
Продукт: L-тирозин + 3-гидроксифенилаланин [(он же м-тирозин)] + дигидроптеридин + H2O
Организм: Homo sapiens
Субстрат: м-тирозин
Продукт: м-тирамин + CO2
Организм: Homo sapiens
является высокоаффинным рецептором для METH/AMPH и DA
такими как мурашки по коже или дрожь по позвоночнику, обычно называемые «ознобом» или «дрожью». ... В целом, наши результаты прямо показали, что фармакологические вмешательства двунаправленно модулировали реакции вознаграждения, вызванные музыкой. В частности, мы обнаружили, что рисперидон ухудшал способность участников испытывать музыкальное удовольствие, тогда как леводопа усиливал ее. ... Здесь, напротив, изучая реакции на абстрактные вознаграждения у людей, мы показываем, что манипуляция дофаминергической передачей влияет как на удовольствие (т. е. количество времени, в течение которого сообщалось о ознобе и эмоциональном возбуждении, измеренном с помощью EDA), так и на мотивационные компоненты музыкального вознаграждения (деньги, которые готовы потратить). Эти результаты свидетельствуют о том, что дофаминергическая сигнализация является непременным условием не только для мотивационных реакций, как было показано для первичных и вторичных вознаграждений, но и для гедонистических реакций на музыку. Этот результат подтверждает недавние результаты, показывающие, что дофамин также опосредует воспринимаемую приятность, достигаемую другими типами абстрактных вознаграждений (37), и оспаривает предыдущие результаты на животных моделях по первичным вознаграждениям, таким как еда (42, 43).
(1) представляют доказательства того, что усиление или ингибирование передачи сигналов дофамина с помощью леводопы или рисперидона модулирует удовольствие, испытываемое во время прослушивания музыки. ... В заключительном заходе, чтобы установить не только корреляционную, но и причинную роль дофамина в музыкальном удовольствии, авторы обратились к непосредственному манипулированию дофаминергической сигнализацией в полосатом теле, сначала путем применения возбуждающей и ингибирующей транскраниальной магнитной стимуляции к левой дорсолатеральной префронтальной коре участников, области, которая, как известно, модулирует функцию полосатого тела (5), и, наконец, в текущем исследовании путем введения фармацевтических агентов, способных изменять синаптическую доступность дофамина (1), оба из которых влияли на воспринимаемое удовольствие, физиологические показатели возбуждения и денежную стоимость, приписываемую музыке в прогнозируемом направлении. ... Хотя вопрос музыкального выражения эмоций имеет долгую историю исследований, в том числе в PNAS (6), и психофизиологическое направление исследований 1990-х годов уже установило, что музыкальное удовольствие может активировать автономную нервную систему (7), демонстрация авторами роли системы вознаграждения в музыкальных эмоциях была воспринята как первое доказательство того, что это были подлинные эмоции, изучение которых имеет полное право информировать нейробиологию о наших повседневных когнитивных, социальных и аффективных функциях (8). Между прочим, это направление работы, кульминацией которого стала статья Феррери и др. (1), вероятно, сделало больше для привлечения финансирования исследований в области музыкальных наук, чем любое другое в этом сообществе.
Доказательства Феррери и др. (1) предоставляют новейшую поддержку убедительной нейробиологической модели, в которой музыкальное удовольствие возникает из взаимодействия древних систем вознаграждения/оценки (стриатно-лимбической-паралимбической) с более филогенетически продвинутыми системами восприятия/предсказания (височно-фронтальной).
Дофамин связывается с бета-1, бета-2, альфа-1 и дофаминергическими рецепторами .