Хемиосмос — это движение ионов через полупроницаемую мембранную структуру вниз по их электрохимическому градиенту . Важным примером является образование аденозинтрифосфата (АТФ) путем перемещения ионов водорода (H + ) через мембрану во время клеточного дыхания или фотосинтеза .
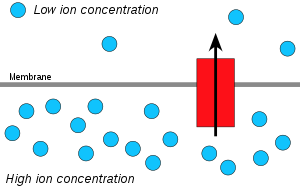
Ионы водорода, или протоны , будут диффундировать из области с высокой концентрацией протонов в область с более низкой концентрацией протонов, а электрохимический градиент концентрации протонов через мембрану можно использовать для образования АТФ. Этот процесс связан с осмосом — движением воды через селективную мембрану, поэтому его называют «хемиосмосом».
АТФ-синтаза – это фермент , который производит АТФ путем хемиосмоса. Он позволяет протонам проходить через мембрану и использует разницу свободной энергии для преобразования фосфорилированного аденозиндифосфата (АДФ) в АТФ. АТФ-синтаза состоит из двух частей: CF0 (присутствует в мембране тилакоида) и CF1 (выступает на внешней поверхности мембраны тилакоида). Нарушение протонного градиента приводит к конформационным изменениям CF1, обеспечивая в процессе достаточно энергии для преобразования АДФ в АТФ. Образование АТФ путем хемиосмоса происходит в митохондриях и хлоропластах , а также у большинства бактерий и архей . Например, в хлоропластах во время фотосинтеза цепь переноса электронов перекачивает ионы H + (протоны) в строме (жидкости) через тилакоидную мембрану в тилакоидные пространства. Запасенная энергия используется для фотофосфорилирования АДФ и образования АТФ, поскольку протоны проходят через АТФ-синтазу.
Питер Д. Митчелл предложил хемиосмотическую гипотезу в 1961 году. [1] Вкратце, гипотеза заключалась в том, что большая часть синтеза аденозинтрифосфата (АТФ) в дышащих клетках происходит за счет электрохимического градиента на внутренних мембранах митохондрий с использованием энергии НАДН и ФАДН . 2 образуется в ходе окислительного распада богатых энергией молекул, таких как глюкоза .
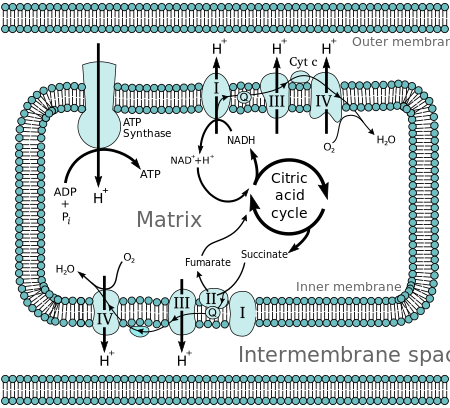
Молекулы, такие как глюкоза, метаболизируются с образованием ацетил-КоА как довольно богатого энергией промежуточного продукта. Окисление ацетил -коэнзима А (ацетил-КоА) в митохондриальном матриксе сопровождается восстановлением молекулы-носителя, такой как никотинамидадениндинуклеотид ( НАД) и флавинадениндинуклеотид (ФАД). [2] Переносчики передают электроны в цепь переноса электронов (ETC) во внутренней мембране митохондрий , которая, в свою очередь, передает их другим белкам в ETC. Энергия на каждом этапе окислительно-восстановительного переноса используется для перекачки протонов из матрицы в межмембранное пространство, сохраняя энергию в виде трансмембранного электрохимического градиента . Протоны движутся обратно через внутреннюю мембрану с помощью фермента АТФ-синтазы . Поток протонов обратно в матрикс митохондрии через АТФ-синтазу обеспечивает достаточно энергии для соединения АДФ с неорганическим фосфатом с образованием АТФ.
В то время это было радикальное предложение, которое не было хорошо принято. Преобладало мнение, что энергия переноса электрона сохраняется как стабильный промежуточный продукт с высоким потенциалом, что является химически более консервативной концепцией. Проблема старой парадигмы заключается в том, что так и не было обнаружено ни одного высокоэнергетического промежуточного соединения, а доказательства существования протонной накачки комплексами цепи переноса электронов стали слишком обширными, чтобы их можно было игнорировать. В конце концов, все доказательства стали свидетельствовать в пользу хемиосмотической гипотезы, и в 1978 году Питер Д. Митчелл был удостоен Нобелевской премии по химии . [3]
Хемиосмотическое соединение важно для производства АТФ в митохондриях , хлоропластах [4] и многих бактериях и археях . [5]
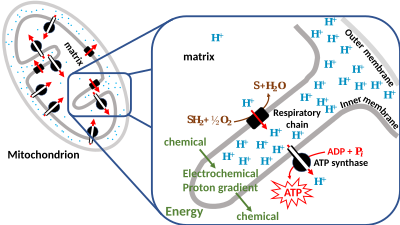
Движение ионов через мембрану зависит от сочетания двух факторов:
Эти два градиента, взятые вместе, можно выразить как электрохимический градиент .
Однако липидные бислои биологических мембран являются барьерами для ионов. Вот почему энергия может храниться в виде комбинации этих двух градиентов на мембране. Только специальные мембранные белки, такие как ионные каналы , иногда могут позволять ионам перемещаться через мембрану (см. Также: Мембранный транспорт ). В хемиосмотической гипотезе трансмембранная АТФ-синтаза играет центральную роль в преобразовании энергии спонтанного потока протонов через них в химическую энергию АТФ-связей.
Поэтому исследователи создали термин протон-движущая сила (ПМФ), полученный из упомянутого ранее электрохимического градиента. Его можно описать как меру запасенной потенциальной энергии ( хемиосмотического потенциала ) как комбинации градиентов протонов и напряжения (электрического потенциала) на мембране. Электрический градиент является следствием разделения зарядов через мембрану (когда протоны H + движутся без противоиона , например хлорида Cl- ) .
В большинстве случаев протондвижущая сила генерируется цепью переноса электронов, которая действует как протонный насос, используя свободную энергию Гиббса окислительно -восстановительных реакций для перекачки протонов (ионов водорода) через мембрану, разделяя заряд на мембране. В митохондриях энергия, выделяемая цепью переноса электронов, используется для перемещения протонов из митохондриального матрикса (сторона N) в межмембранное пространство (сторона P). Вывод протонов из митохондрии создает более низкую концентрацию положительно заряженных протонов внутри нее, что приводит к избыточному отрицательному заряду на внутренней стороне мембраны. Градиент электрического потенциала составляет около -170 мВ [6] , внутри отрицательный (Н). Эти градиенты — разность зарядов и разница в концентрации протонов — создают комбинированный электрохимический градиент на мембране, часто выражаемый как протон-движущая сила (PMF). В митохондриях ПМП почти полностью состоит из электрического компонента, но в хлоропластах ПМП состоит в основном из градиента pH, поскольку заряд протонов H + нейтрализуется движением Cl - и других анионов. В любом случае PMF должен быть больше примерно 460 мВ (45 кДж/моль), чтобы АТФ-синтаза могла производить АТФ.
Протондвижущая сила получается из свободной энергии Гиббса . Пусть N обозначает внутреннюю часть ячейки, а P — внешнюю. Тогда [6]
где
Молярное изменение свободной энергии Гиббса часто интерпретируют как молярный электрохимический потенциал иона .
Для электрохимического протонного градиента и как следствие:
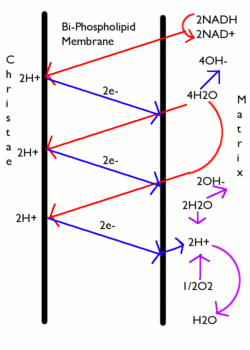
где
Митчелл определил протон-движущую силу (ПМП) как
Например, подразумевается . При этом уравнение принимает вид:
.
Обратите внимание, что спонтанный импорт протонов со стороны P (относительно более положительной и кислой) на сторону N (относительно более отрицательной и щелочной) является отрицательным (аналогично ), тогда как PMF положителен (аналогично окислительно-восстановительному потенциалу клетки ).
Стоит отметить, что, как и любой процесс трансмембранного транспорта, PMF является направленным. Знак трансмембранной разности электрических потенциалов выбирается так, чтобы представлять изменение потенциальной энергии на единицу заряда, поступающего в клетку, как указано выше. Более того, из-за окислительно-восстановительной перекачки протонов в местах связывания градиент протонов всегда внутрищелочной. По обеим этим причинам протоны текут самопроизвольно со стороны P на сторону N; доступная свободная энергия используется для синтеза АТФ (см. ниже). По этой причине PMF определяется для импорта протонов, который является спонтанным. PMF для экспорта протонов, т. е. перекачка протонов, катализируемая сайтами связывания, является просто отрицанием PMF (импорта).
Спонтанность импорта протонов (со стороны P на сторону N) универсальна для всех биоэнергетических мембран. [8] Этот факт не был признан до 1990-х годов, поскольку просвет тилакоида хлоропласта интерпретировался как внутренняя фаза, но на самом деле он топологически эквивалентен внешней части хлоропласта. Аззон и др. подчеркнул, что внутренней фазой (N-сторона мембраны) является бактериальная цитоплазма, митохондриальный матрикс или строма хлоропласта; внешняя сторона (P) представляет собой бактериальное периплазматическое пространство, митохондриальное межмембранное пространство или просвет хлоропласта. Кроме того, 3D-томография внутренней мембраны митохондрий показывает, что ее обширные впячивания расположены друг над другом, подобно тилакоидным дискам; следовательно, межмембранное пространство митохондрий топологически очень похоже на просвет хлоропласта: [9]
Энергия, выраженная здесь как свободная энергия Гиббса, электрохимический протонный градиент или протон-движущая сила (ПМФ), представляет собой комбинацию двух градиентов через мембрану:
Когда система достигает равновесия, ; тем не менее, концентрации по обе стороны мембраны не обязательно должны быть равными. Спонтанное движение через потенциальную мембрану определяется как градиентами концентрации, так и электрическим потенциалом.
Молярная свободная энергия Гиббса синтеза АТФ.
еще называют потенциалом фосфорилирования. Равновесное соотношение концентраций можно рассчитать путем сравнения и , например, в случае митохондрий млекопитающих: [9]
H + /АТФ = ΔG p /(Δp/10,4 кДж·моль -1 /мВ) = 40,2 кДж·моль -1 /(173,5 мВ/10,4 кДж·моль -1 /мВ) = 40,2/16,7 = 2,4. Фактическое соотношение числа копий протон-связывающей c-субъединицы к числу копий бета-субъединицы, синтезирующей АТФ, составляет 8/3 = 2,67, что показывает, что в этих условиях митохондрия функционирует с эффективностью 90% (2,4/2,67). [9]
Фактически, термодинамическая эффективность в эукариотических клетках в основном ниже, поскольку АТФ должен экспортироваться из матрикса в цитоплазму, а АДФ и фосфат должны импортироваться из цитоплазмы. Это «стоит» одного «дополнительного» импорта протона на АТФ, [6] [7] , следовательно, фактическая эффективность составляет всего 65% (= 2,4/3,67).

Полный распад глюкозы с высвобождением ее энергии называется клеточным дыханием . Последние этапы этого процесса происходят в митохондриях. Восстановленные молекулы НАДН и ФАДН 2 образуются в результате цикла Кребса , гликолиза и переработки пирувата . Эти молекулы передают электроны в цепь переноса электронов , которая высвобождает энергию кислорода для создания протонного градиента через внутреннюю митохондриальную мембрану . АТФ-синтаза затем использует энергию, запасенную в этом градиенте, для производства АТФ. Этот процесс называется окислительным фосфорилированием, поскольку он использует энергию, выделяемую при окислении НАДН и ФАДН 2, для фосфорилирования АДФ в АТФ .
Световые реакции фотосинтеза производят АТФ под действием хемиосмоса. Фотоны солнечного света принимаются антенным комплексом Фотосистемы II , который возбуждает электроны на более высокий энергетический уровень . Эти электроны перемещаются по цепи переноса электронов , вызывая активную перекачку протонов через тилакоидную мембрану в просвет тилакоида . Затем эти протоны текут по градиенту электрохимического потенциала через фермент, называемый АТФ-синтазой, создавая АТФ путем фосфорилирования АДФ в АТФ. Электроны от первоначальной световой реакции достигают Фотосистемы I , затем поднимаются на более высокий энергетический уровень за счет энергии света, а затем принимаются акцептором электронов и восстанавливают НАДФ + до НАДФН . Электроны, потерянные из Фотосистемы II, заменяются в результате окисления воды, которая «расщепляется» на протоны и кислород с помощью комплекса, выделяющего кислород (OEC, также известного как WOC, или водоокисляющий комплекс). Для образования одной молекулы двухатомного кислорода фотосистемы I и II должны поглотить 10 фотонов, пройти через две фотосистемы должны четыре электрона и образоваться 2 НАДФН (позже используемые для фиксации углекислого газа в цикле Кальвина).
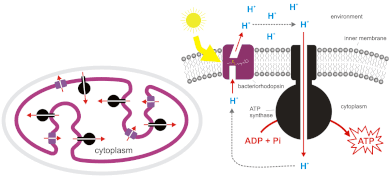
Бактерии и археи также могут использовать хемиосмос для выработки АТФ. Цианобактерии , зеленые серобактерии и пурпурные бактерии синтезируют АТФ посредством процесса, называемого фотофосфорилированием . [6] [7] Эти бактерии используют энергию света для создания протонного градиента с помощью фотосинтетической цепи переноса электронов . Нефотосинтезирующие бактерии, такие как E. coli, также содержат АТФ-синтазу . Фактически, митохондрии и хлоропласты являются продуктом эндосимбиоза и восходят к встроенным прокариотам. Этот процесс описан в эндосимбиотической теории . Происхождение митохондрий послужило толчком к возникновению эукариот, а происхождение пластид — к возникновению архепластид, одной из основных супергрупп эукариот. [ нужна цитата ]
Хемиосмотическое фосфорилирование — третий путь производства АТФ из неорганического фосфата и молекулы АДФ. Этот процесс является частью окислительного фосфорилирования.
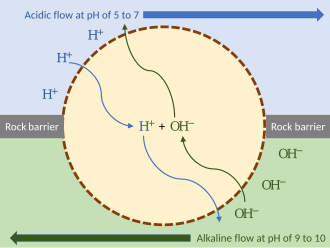
Пошаговая модель возникновения хемиосмоса, ключевого элемента возникновения жизни на Земле, предполагает, что первобытные организмы использовали термоциклирование в качестве источника энергии (термосинтез), действуя по существу как тепловой двигатель: [11]
Глубоководные гидротермальные источники , испускающие горячую кислую или щелочную воду, могли создать внешние протонные градиенты. Они давали энергию, которую могли использовать первобытные организмы. Чтобы разделить потоки, такой организм мог заклиниться в скале гидротермального источника, подвергаясь воздействию гидротермального потока с одной стороны и более щелочной воды с другой. Пока мембрана организма (или пассивные ионные каналы внутри нее) проницаема для протонов, механизм может функционировать без ионных насосов. Такой протоорганизм мог затем развить дополнительные механизмы, такие как ионные насосы и АТФ-синтаза. [10]
Предлагаемый альтернативный источник хемиосмотической энергии, развивающейся через мембранные структуры, заключается в том, что если акцептор электронов, феррицианид, находится внутри пузырька, а донор электронов находится снаружи, то хиноны, переносимые углеродистыми метеоритами, забирают электроны и протоны от донора. Они будут высвобождать электроны через липидную мембрану путем диффузии к феррицианиду внутри везикул и высвобождать протоны, что создает градиенты pH выше 2. Этот процесс способствует развитию протонных градиентов. [12] [13]