Метастазирование — это распространение патогенного агента из начального или первичного участка в другой или вторичный участок в организме хозяина; [1] этот термин обычно используется применительно к метастазам раковой опухоли . [2] Таким образом, новые патологические участки представляют собой метастазы ( мет ). [3] [4] Его обычно отличают от раковой инвазии , которая представляет собой прямое распространение и проникновение раковых клеток в соседние ткани. [5]
Рак возникает после того, как клетки генетически изменяются и начинают быстро и бесконечно размножаться. Эта неконтролируемая пролиферация путем митоза приводит к образованию первичной гетерогенной опухоли . Клетки, составляющие опухоль, в конечном итоге подвергаются метаплазии , за которой следует дисплазия , а затем анаплазия , что приводит к злокачественному фенотипу. Это злокачественное новообразование допускает инвазию в кровообращение с последующей инвазией во второй участок онкогенеза .
Некоторые раковые клетки, известные как циркулирующие опухолевые клетки, приобретают способность проникать через стенки лимфатических или кровеносных сосудов , после чего они могут циркулировать через кровоток в другие участки и ткани организма. [6] Этот процесс известен (соответственно) как лимфатическое или гематогенное распространение. После того как опухолевые клетки останавливаются на другом участке, они вновь проникают в сосуд или стенки и продолжают размножаться, в конечном итоге образуя другую клинически обнаруживаемую опухоль. [ нужна цитация ] Эта новая опухоль известна как метастатическая (или вторичная ) опухоль. Метастазирование является одним из признаков рака , отличающим его от доброкачественных опухолей . [7] Большинство видов рака могут метастазировать, хотя и в разной степени. Например, базальноклеточная карцинома редко метастазирует. [7]
Когда опухолевые клетки метастазируют, новая опухоль называется вторичной или метастатической опухолью, и ее клетки аналогичны клеткам исходной или первичной опухоли . [8] Это означает, что если рак молочной железы метастазирует в легкие, вторичная опухоль состоит из аномальных клеток молочной железы, а не из аномальных клеток легких. Опухоль в легком тогда называется метастатическим раком молочной железы , а не раком легких . Метастазирование является ключевым элементом в системах стадирования рака , таких как система стадирования TNM , где он обозначает букву «М». В общей группе стадий метастазы помещают рак в стадию IV. Возможности радикального лечения значительно уменьшаются или часто полностью исчезают, когда рак метастазирует.

Вначале рано поражаются близлежащие лимфатические узлы. [9] Легкие , печень , мозг и кости являются наиболее распространенными местами метастазирования солидных опухолей . [9]
Хотя запущенный рак может вызывать боль , часто это не первый симптом.
Однако у некоторых пациентов никаких симптомов не наблюдается. [9] Когда орган получает метастатическое заболевание, он начинает сжиматься до тех пор, пока его лимфатические узлы не лопнут или не подвергнутся лизису .
Метастатические опухоли очень распространены на поздних стадиях рака. Распространение метастазов может происходить по крови, лимфе или обоими путями. Наиболее распространенными местами метастазов являются легкие , печень , мозг и кости . [10]
В настоящее время предложены три основные теории для объяснения метастатического пути рака: гипотеза эпителиально-мезенхимального перехода (ЕМТ) и мезенхимально-эпителиального перехода (МЕТ) (1), гипотеза раковых стволовых клеток (2) и гипотеза макрофагально-эпителиального перехода (МЭТ) (1). Гибридная гипотеза слияния раковых клеток (3). Были также выдвинуты некоторые новые гипотезы, а именно: под действием определенных биохимических и/или физических стрессоров раковые клетки могут подвергаться изгнанию ядра с последующим поглощением макрофагов и слиянием с образованием раковых слитых клеток (CFC). [11] Понимание загадки распространения раковых клеток на отдаленные участки, что является причиной более 90% смертей, связанных с раком, требует всесторонних исследований. Ключевые нерешенные вопросы вращаются вокруг выживания и миграции раковых клеток, таких как ядро, поскольку они сталкиваются с проблемами прохождения через капиллярные клапаны и гидродинамическими сдвиговыми силами в системе кровообращения, что делает ЦОК маловероятным источником метастазирования. Более того, понимание того, как раковые клетки адаптируются к метастатической нише и остаются в состоянии покоя (спячка опухоли) в течение длительных периодов времени, представляет собой трудные вопросы, требующие дальнейшего изучения. [12]
Метастазирование включает в себя сложную серию этапов, на которых раковые клетки покидают исходное место опухоли и мигрируют в другие части тела через кровоток, лимфатическую систему или путем прямого распространения. Для этого злокачественные клетки отрываются от первичной опухоли, прикрепляются к белкам , которые составляют окружающий внеклеточный матрикс (ECM), который отделяет опухоль от прилегающих тканей, и разрушают их. Разрушая эти белки, раковые клетки способны проникнуть во внеклеточный матрикс и уйти. Расположение метастазов не всегда случайно: различные типы рака имеют тенденцию распространяться на определенные органы и ткани со скоростью, превышающей ожидаемую только по статистической случайности. [13] Рак молочной железы, например, имеет тенденцию метастазировать в кости и легкие. Эта специфичность, по-видимому, опосредована растворимыми сигнальными молекулами, такими как хемокины [14] и трансформирующий фактор роста бета . [15] Организм противостоит метастазам с помощью различных механизмов посредством действия класса белков, известных как супрессоры метастазирования , из которых известно около дюжины. [16]
Клетки человека демонстрируют различные виды движения: коллективную подвижность , движение мезенхимального типа и амебоидное движение . Раковые клетки часто произвольно переключаются между разными видами движения. Некоторые исследователи рака надеются найти методы лечения, которые смогут остановить или хотя бы замедлить распространение рака, каким-то образом блокируя необходимый этап в одном или нескольких видах движений. [17] [18]
Все этапы метастатического каскада включают ряд физических процессов. Миграция клеток требует генерации сил, и когда раковые клетки мигрируют через сосудистую сеть, это требует образования физических разрывов в кровеносных сосудах. [19] Помимо сил, во время метастазирования решающее значение имеет регуляция различных типов межклеточных и межклеточных спаек.
Стадии метастазирования критически регулируются различными типами клеток, включая клетки кровеносных сосудов (эндотелиальные клетки), иммунные клетки или стромальные клетки. Рост новой сети кровеносных сосудов, называемый опухолевым ангиогенезом , [20] является важнейшим признаком рака. Поэтому было высказано предположение, что ингибиторы ангиогенеза предотвращают рост метастазов. [7] Было показано, что эндотелиальные клетки-предшественники оказывают сильное влияние на метастазирование и ангиогенез. [21] [22] Эндотелиальные клетки-предшественники играют важную роль в росте опухоли, ангиогенезе и метастазировании, и их можно пометить с помощью ингибитора связывания ДНК 1 (ID1). Это новое открытие означало, что исследователи получили возможность отслеживать эндотелиальные клетки-предшественники от костного мозга до крови, стромы опухоли и даже включаться в сосудистую сеть опухоли. Эндотелиальные клетки-предшественники, включенные в сосудистую сеть опухоли, позволяют предположить, что этот тип клеток важен для развития кровеносных сосудов в условиях опухоли и метастазирования. Кроме того, абляция эндотелиальных клеток-предшественников в костном мозге может привести к значительному замедлению роста опухоли и развития сосудистой сети. Следовательно, эндотелиальные клетки-предшественники важны в биологии опухолей и представляют собой новые терапевтические мишени. [23] При раке иммунная система обычно не регулируется и влияет на многие стадии прогрессирования опухоли, включая метастазирование.
Эпигенетическая регуляция также играет важную роль в метастатическом росте диссеминированных опухолевых клеток. Метастазы демонстрируют изменения в модификациях гистонов, такие как H3K4-метилирование и H3K9-метилирование, по сравнению с соответствующими первичными опухолями. [24] Эти эпигенетические модификации метастазов могут способствовать пролиферации и выживанию диссеминированных опухолевых клеток в отдаленных органах. [25]
Недавнее исследование показывает, что PKC-йота способствует инвазии клеток меланомы путем активации виментина во время ЕМТ. Ингибирование или нокдаун PKC-йота приводили к увеличению уровней E-кадгерина и RhoA при одновременном снижении общего количества виментина, фосфорилированного виментина (S39) и Par6 в метастатических клетках меланомы. Эти результаты позволяют предположить, что PKC-ι участвует в сигнальных путях, которые активируют ЕМТ при меланоме, тем самым непосредственно стимулируя метастазирование. [26]
Недавно серия громких экспериментов показала, что коопция межклеточного перекрестного взаимодействия, опосредованного экзосомными везикулами, является критическим фактором, участвующим во всех этапах каскада инвазии-метастазирования. [27]
Метастазирование происходит следующими четырьмя путями:
Распространение злокачественного новообразования в полости тела может происходить путем проникновения на поверхность брюшины , плевры , перикарда или субарахноидального пространства. Например, опухоли яичников могут распространяться трансперитонеально на поверхность печени.
Лимфатическое распространение позволяет транспортировать опухолевые клетки в регионарные лимфатические узлы вблизи первичной опухоли и, в конечном итоге, в другие части тела. Это называется поражением узлов, положительными узлами или регионарным заболеванием. «Положительные узлы» — это термин, который медицинские специалисты будут использовать для описания регионарных лимфатических узлов, которые дали положительный результат на злокачественное новообразование. Обычной медицинской практикой является биопсия по крайней мере одного лимфатического узла рядом с местом опухоли при проведении операции по исследованию или удалению опухоли. Этот лимфатический узел затем называется сторожевым лимфатическим узлом . Лимфатическое распространение является наиболее частым путем начального метастазирования карцином . [7] Напротив, саркома редко метастазирует по этому пути. Локализованное распространение на регионарные лимфатические узлы рядом с первичной опухолью обычно не считается метастазированием, хотя это является признаком худшего исхода . Лимфатическая система в конечном итоге дренируется из грудного протока и правого лимфатического протока в системную венозную систему в венозном углу и в брахиоцефальные вены , и поэтому эти метастатические клетки также могут в конечном итоге распространяться гематогенным путем.

Это типичный путь метастазирования сарком, но он также является предпочтительным путем для некоторых типов карциномы, таких как почечно-клеточный рак , возникающий в почках , и фолликулярный рак щитовидной железы. Из-за более тонких стенок вены инвазируются чаще, чем артерии, и метастазы имеют тенденцию следовать образцу венозного оттока . То есть гематогенное распространение часто происходит по разным закономерностям в зависимости от местоположения первичной опухоли. Например, колоректальный рак распространяется преимущественно через воротную вену в печень.
Некоторые опухоли, особенно карциномы , могут метастазировать в анатомические канальцевые пространства. Эти пространства включают, например, желчные протоки, мочевую систему, дыхательные пути и субарахноидальное пространство . Этот процесс аналогичен трансцеломному распространению. Однако зачастую остается неясным, являются ли одновременно диагностированные опухоли канальцевой системы одним метастатическим процессом или же фактически самостоятельными опухолями, вызванными одним и тем же возбудителем ( полевая канцеризация ).
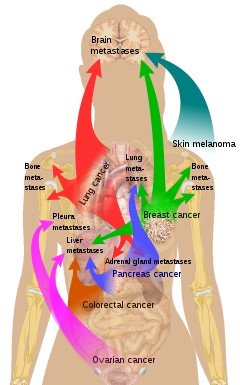
Существует склонность к образованию определенных опухолей в определенных органах. Впервые это обсуждалось как теория «семени и почвы» Стивеном Пейджетом в 1889 году. [29] Склонность метастатической клетки к распространению в определенный орган называется «органотропизмом». Например, рак простаты обычно метастазирует в кости. Аналогичным образом рак толстой кишки имеет тенденцию к метастазированию в печень. Рак желудка часто метастазирует в яичник у женщин, тогда его называют опухолью Крукенберга .
Согласно теории «семени и почвы», раковым клеткам трудно выжить за пределами региона их происхождения, поэтому для метастазирования им необходимо найти место со схожими характеристиками. [30] Например, клетки опухоли молочной железы, которые собирают ионы кальция из грудного молока, метастазируют в костную ткань, где они могут собирать ионы кальция из костей. Злокачественная меланома распространяется на мозг, предположительно потому, что нервная ткань и меланоциты возникают из одной и той же клеточной линии эмбриона . [31]
В 1928 году Джеймс Юинг бросил вызов теории «семени и почвы» и предположил, что метастазирование происходит исключительно анатомическим и механическим путем. Эта гипотеза недавно была использована для того, чтобы предложить несколько гипотез о жизненном цикле циркулирующих опухолевых клеток (ЦОК) и постулировать, что закономерности распространения можно лучше понять с точки зрения «фильтрации и потока». [32] Однако современные данные указывают на то, что первичная опухоль может диктовать органотропные метастазы, вызывая образование преметастатических ниш на отдаленных участках, где поступающие метастатические клетки могут приживляться и колонизироваться. [27] В частности, было показано, что везикулы экзосом, секретируемые опухолями, локализуются в преметастатических участках, где они активируют прометастатические процессы, такие как ангиогенез, и изменяют иммунную среду, чтобы создать благоприятную микросреду для роста вторичной опухоли. [27]
Предполагается, что метастазы всегда совпадают с первичным раком и, как таковые, представляют собой опухоль, возникшую из раковой клетки или клеток в другой части тела. Однако более 10% пациентов, поступающих в онкологические отделения, будут иметь метастазы без обнаружения первичной опухоли. В этих случаях врачи называют первичную опухоль «неизвестной» или «скрытой», а у пациента говорят, что у пациента рак неизвестного первичного происхождения (CUP) или неизвестные первичные опухоли (UPT). [33] По оценкам, 3% всех видов рака имеют неизвестное первичное происхождение. [34] Исследования показали, что, если простой опрос не выявляет источник рака (кашель с кровью — «вероятно, легкие », мочеиспускание с кровью — «вероятно, мочевой пузырь »), сложные методы визуализации тоже не помогут. [34] В некоторых из этих случаев первичная опухоль может появиться позже.
Использование иммуногистохимии позволило патологам идентифицировать многие из этих метастазов. Однако визуализация указанной области лишь иногда выявляет первичный очаг. В редких случаях (например, при меланоме ) первичная опухоль не обнаруживается даже на аутопсии . Поэтому считается, что некоторые первичные опухоли могут полностью регрессировать, но оставить метастазы. В других случаях опухоль может быть слишком маленькой и/или располагаться в необычном месте, чтобы ее можно было диагностировать.

Клетки метастатической опухоли напоминают клетки первичной опухоли. После того как раковую ткань исследуют под микроскопом для определения типа клеток, врач обычно может сказать, обычно ли этот тип клеток обнаруживается в той части тела, из которой был взят образец ткани.
Например, клетки рака молочной железы выглядят одинаково независимо от того, обнаружены ли они в груди или распространились на другую часть тела. Так, если образец ткани, взятый из опухоли легкого, содержит клетки, похожие на клетки молочной железы, врач определяет, что опухоль легкого является вторичной опухолью. Тем не менее, определение первичной опухоли часто может быть очень трудным, и патологу, возможно, придется использовать несколько адъювантных методов, таких как иммуногистохимия , FISH ( флуоресцентная гибридизация in situ ) и другие. Несмотря на использование методик, в ряде случаев первичная опухоль остается неидентифицированной.
Метастатический рак может быть обнаружен одновременно с первичной опухолью или через несколько месяцев или лет. Когда вторая опухоль обнаруживается у пациента, который ранее лечился от рака, чаще всего это метастаз, чем другая первичная опухоль.
Ранее считалось, что большинство раковых клеток имеют низкий метастатический потенциал и что существуют редкие клетки, которые развивают способность метастазировать за счет развития соматических мутаций. [35] Согласно этой теории, диагностика метастатического рака возможна только после появления метастазов. Традиционные методы диагностики рака (например, биопсия ) позволяют исследовать только субпопуляцию раковых клеток и, скорее всего, не позволяют брать образцы из субпопуляции с метастатическим потенциалом. [36]
Соматическая мутационная теория развития метастазов при раке человека не подтверждена. Скорее, кажется, что генетическое состояние первичной опухоли отражает способность этого рака метастазировать. [36] Исследования, сравнивающие экспрессию генов между первичными и метастатическими аденокарциномами , выявили подмножество генов, экспрессия которых может отличать первичные опухоли от метастатических опухолей, получивших название «метастатическая сигнатура». [36] Гены с повышенным уровнем экспрессии в сигнатуре включают: SNRPF , HNRPAB , DHPS и секурин . С этой сигнатурой также было связано снижение регуляции актина , миозина и MHC класса II . Кроме того, метастатическая экспрессия этих генов также наблюдалась в некоторых первичных опухолях, что указывает на то, что клетки, способные метастазировать, могут быть идентифицированы одновременно с диагностикой первичной опухоли. [37] Недавняя работа выявила форму генетической нестабильности при раке, называемую хромосомной нестабильностью (CIN), как движущую силу метастазирования. [38] В агрессивных раковых клетках свободные фрагменты ДНК нестабильных хромосом попадают в цитозоль, что приводит к хронической активации врожденных иммунных путей, которые перехватываются раковыми клетками и распространяются на отдаленные органы.
Выражение этой метастатической сигнатуры коррелирует с плохим прогнозом и, как было показано, является постоянным при нескольких типах рака. Было показано, что прогноз хуже для лиц, первичные опухоли которых имеют метастатические признаки. [36] Кроме того, было показано, что экспрессия этих метастатических генов применима и к другим типам рака, помимо аденокарциномы . Метастазы рака молочной железы , медуллобластомы и рака простаты имели сходные паттерны экспрессии этих генов, связанных с метастазами. [36]
Идентификация этой сигнатуры, связанной с метастазами, дает надежду на идентификацию клеток с метастатическим потенциалом внутри первичной опухоли и надежду на улучшение прогноза этих метастазированных видов рака. Кроме того, идентификация генов, экспрессия которых изменяется при метастазировании, предлагает потенциальные мишени для ингибирования метастазирования. [36]
Лечение и выживаемость в значительной степени определяются тем, остается ли рак локализованным или распространяется на другие участки тела. Если рак метастазирует в другие ткани или органы, это обычно резко увеличивает вероятность смерти пациента. Некоторые виды рака, такие как некоторые формы лейкемии , рак крови или злокачественные новообразования головного мозга , могут привести к смерти, не распространяясь вообще.
После того, как рак дал метастазы, его все равно можно лечить с помощью радиохирургии , химиотерапии , лучевой терапии , биологической терапии , гормональной терапии , хирургического вмешательства или комбинации этих вмешательств («мультимодальная терапия»). Выбор лечения зависит от многих факторов, включая тип первичного рака, размер и расположение метастазов, возраст и общее состояние здоровья пациента, а также виды лечения, применявшиеся ранее. У пациентов с диагнозом CUP часто все еще возможно вылечить заболевание, даже если не удается обнаружить первичную опухоль.
Современные методы лечения редко способны вылечить метастатический рак, хотя некоторые опухоли, такие как рак яичек и рак щитовидной железы , обычно излечимы.
Паллиативная помощь , помощь, направленная на улучшение качества жизни людей с тяжелыми заболеваниями, рекомендуется как часть программ лечения метастазов. [39] Результаты систематического обзора литературы по лучевой терапии метастазов в головной мозг показали, что существует мало доказательств, подтверждающих сравнительную эффективность и ориентированные на пациента результаты в отношении качества жизни, функционального статуса и когнитивных эффектов. [40]
Хотя широко распространено мнение, что метастазы являются результатом миграции опухолевых клеток, существует гипотеза, согласно которой некоторые метастазы являются результатом воспалительных процессов со стороны аномальных иммунных клеток. [41] Существование метастатического рака при отсутствии первичных опухолей также предполагает, что метастазы не всегда вызваны злокачественными клетками, покидающими первичные опухоли. [42]
Исследование, проведенное командой Сарны, доказало, что сильно пигментированные клетки меланомы имеют модуль Юнга около 4,93, тогда как у непигментированных клеток он составляет всего 0,98. [43] В другом эксперименте они обнаружили, что эластичность клеток меланомы важна для ее метастазирования и роста: непигментированные опухоли были больше, чем пигментированные, и им было гораздо легче распространяться. Они показали, что в опухолях меланомы есть как пигментированные, так и непигментированные клетки , поэтому они могут быть как устойчивыми к лекарствам, так и метастатическими. [43]
Первым врачом, сообщившим о возможности локального метастазирования из первичного источника рака в близлежащие ткани, был Ибн Сина . Он описал случай рака молочной железы и метастатического состояния в «Каноне медицины» . Его гипотеза основывалась на клиническом течении больного. [44] [45]
В марте 2014 года исследователи обнаружили старейший полный пример человека с метастатическим раком. Опухоли возникли в 3000-летнем скелете, найденном в 2013 году в гробнице в Судане , датируемой 1200 годом до нашей эры. Скелет был проанализирован с помощью рентгенографии и сканирующего электронного микроскопа. Эти результаты были опубликованы в журнале Public Library of Science . [46] [47] [48]
Метастаз — греческое слово, означающее «смещение», от μετά, мета , «следующий», и στάσις, застой , «размещение».