Равновесие растворимости — это тип динамического равновесия , которое существует, когда химическое соединение в твердом состоянии находится в химическом равновесии с раствором этого соединения. Твердое вещество может растворяться в неизмененном виде, путем диссоциации или в результате химической реакции с другим компонентом раствора, например кислотой или щелочью. Каждое равновесие растворимости характеризуется зависящим от температуры произведением растворимости , которое действует как константа равновесия . Равновесие растворимости важно в фармацевтических, экологических и многих других сценариях.
Равновесие растворимости существует, когда химическое соединение в твердом состоянии находится в химическом равновесии с раствором , содержащим это соединение. Этот тип равновесия является примером динамического равновесия , при котором некоторые отдельные молекулы мигрируют между твердой фазой и фазой раствора, так что скорости растворения и осаждения равны друг другу. Когда равновесие установлено и твердое вещество еще не полностью растворилось, раствор называют насыщенным. Концентрация растворенного вещества в насыщенном растворе называется растворимостью . Единицами растворимости могут быть молярные (моль дм -3 ) или выраженные как масса на единицу объема, например мкг мл -1 . Растворимость зависит от температуры. Раствор, содержащий более высокую концентрацию растворенного вещества, чем его растворимость, называется перенасыщенным . Пересыщенный раствор можно привести в равновесие путем добавления «затравки», которая может представлять собой крошечный кристалл растворенного вещества или крошечную твердую частицу, которая инициирует осаждение. [ нужна цитата ]
Существует три основных типа равновесия растворимости.
В каждом случае константу равновесия можно определить как частное от активности . Эта константа равновесия безразмерна , поскольку активность является безразмерной величиной. Однако использование активностей очень неудобно, поэтому константу равновесия обычно делят на частное коэффициентов активности, чтобы получить частное от концентраций. Подробности см. в разделе «Равновесная химия» # «Константа равновесия» . Более того, активность твердого тела по определению равна 1, поэтому ее опускают в определяющее выражение.
Для химического равновесия

Растворимость чувствительна к изменениям температуры . Например, сахар более растворим в горячей воде, чем в прохладной. Это происходит потому, что продукты растворимости, как и другие типы констант равновесия, являются функциями температуры. В соответствии с принципом Ле Шателье , когда процесс растворения является эндотермическим (поглощается тепло), растворимость увеличивается с повышением температуры. Этот эффект лежит в основе процесса перекристаллизации , который можно использовать для очистки химического соединения. Когда растворение экзотермическое (выделяется тепло), растворимость снижается с повышением температуры. [1] Сульфат натрия демонстрирует увеличение растворимости при температуре ниже 32,4 ° C, но снижение растворимости при более высокой температуре. [2] Это связано с тем, что твердая фаза представляет собой декагидрат ( Na
2ТАК
4·10 ч.
2O ) ниже температуры перехода, но другой гидрат выше этой температуры. [ нужна цитата ]
Зависимость от температуры растворимости идеального раствора (достигаемая для малорастворимых веществ) дается следующим выражением, содержащим энтальпию плавления Δm H и мольную долю растворенного вещества при насыщении:
Это дифференциальное выражение для неэлектролита можно проинтегрировать по температурному интервалу и получить: [4]
Для неидеальных растворов вместо растворимости мольной доли в производном по температуре появляется активность растворенного вещества при насыщении:
Эффект общего иона — это эффект снижения растворимости одной соли, когда также присутствует другая соль, имеющая с ней общий ион. Например, растворимость хлорида серебра AgCl снижается, когда к суспензии AgCl в воде добавляется хлорид натрия, источник обычного хлорида иона. [5]
Теперь предположим, что также присутствует хлорид натрия в концентрации 0,01 моль дм -3 = 0,01 М. Растворимость, игнорируя любое возможное влияние ионов натрия, теперь рассчитывается по формуле
Термодинамическая константа растворимости определена для крупных монокристаллов. Растворимость будет увеличиваться с уменьшением размера частицы (или капли) растворенного вещества из-за дополнительной поверхностной энергии. Этот эффект обычно невелик, если частицы не становятся очень маленькими, обычно меньше 1 мкм. Влияние размера частиц на константу растворимости можно количественно оценить следующим образом:
Солевые эффекты [7] ( всаливание и высаливание ) относятся к тому факту, что присутствие соли, не имеющей общего с растворенным ионом, оказывает влияние на ионную силу раствора и, следовательно, на коэффициенты активности . так что константа равновесия, выраженная как коэффициент концентрации, изменяется.
Равновесия определены для конкретных кристаллических фаз . Следовательно, ожидается, что произведение растворимости будет различным в зависимости от фазы твердого вещества. Например, арагонит и кальцит будут иметь разные продукты растворимости, хотя оба они имеют одинаковую химическую идентичность ( карбонат кальция ). При любых данных условиях одна фаза будет термодинамически более стабильной, чем другая; следовательно, эта фаза образуется, когда установится термодинамическое равновесие. Однако кинетические факторы могут способствовать образованию неблагоприятного осадка (например, арагонита), который тогда считается метастабильным . [ нужна цитата ]
В фармакологии метастабильное состояние иногда называют аморфным состоянием. Аморфные лекарства обладают более высокой растворимостью, чем их кристаллические аналоги, благодаря отсутствию дальнодействующих взаимодействий, присущих кристаллической решетке. Таким образом, для сольватации молекул в аморфной фазе требуется меньше энергии. Влияние аморфной фазы на растворимость широко используется для повышения растворимости лекарств. [8] [9]
Для конденсированных фаз (твердых и жидких) зависимость растворимости от давления обычно слабая, и на практике ею обычно пренебрегают. Предполагая идеальное решение , зависимость можно количественно выразить как:
Зависимость растворимости от давления иногда имеет практическое значение. Например, загрязнение нефтяных месторождений и скважин осадками сульфатом кальция (который снижает его растворимость при снижении давления) со временем может привести к снижению производительности.
Растворение органического твердого вещества можно описать как равновесие между веществом в твердой и растворенной формах. Например, когда сахароза (столовый сахар) образует насыщенный раствор.
Ионные соединения обычно диссоциируют на составляющие их ионы при растворении в воде. Например, для хлорида серебра :
При очень низкой растворимости соли коэффициенты активности ионов в растворе почти равны единице. Установив их фактически равными единице, это выражение сводится к выражению произведения растворимости :
Для солей 2:2 и 3:3, таких как CaSO 4 и FePO 4 , общее выражение для произведения растворимости такое же, как и для электролита 1:1.
Для несимметричной соли, такой как Ca(OH) 2 , выражение растворимости определяется выражением
В общем случае при химическом равновесии
Произведения растворимости часто выражают в логарифмической форме. Так, для сульфата кальция при K sp =4,93 × 10 -5 моль 2 дм -6 , log K sp = -4,32 . Чем меньше значение K sp или чем более отрицательное значение log, тем ниже растворимость.
Некоторые соли не полностью диссоциируют в растворе. Примеры включают MgSO 4 , который, как известно, был открыт Манфредом Эйгеном и присутствует в морской воде как в виде комплекса внутренней сферы , так и комплекса внешней сферы . [12] Растворимость таких солей рассчитывают методом, изложенным в разделе «Растворение с реакцией».
Произведение растворимости гидроксида иона металла M n + обычно определяется следующим образом:
Для гидроксидов продукты растворимости часто даются в модифицированной форме K * sp , используя концентрацию ионов водорода вместо концентрации гидроксид-ионов. Эти два значения связаны константой самоионизации воды K w . [13]
Типичная реакция растворения включает растворение слабого основания B в кислом водном растворе .
Выщелачивание солей алюминия из камней и почвы кислотными дождями является еще одним примером растворения с реакцией: алюмосиликаты представляют собой основания, которые реагируют с кислотой с образованием растворимых соединений, таких как Al 3+ (водный).
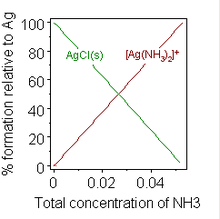
Образование химического комплекса также может изменить растворимость. Известный пример — добавление к суспензии хлорида серебра концентрированного раствора аммиака , растворению которого способствует образование аммиачного комплекса.
Определение растворимости сопряжено с трудностями. [6] Прежде всего, это трудность установления того, что система находится в равновесии при выбранной температуре. Это связано с тем, что реакции как осаждения, так и растворения могут протекать чрезвычайно медленно. Если процесс протекает очень медленно, проблемой может стать испарение растворителя. Возможно перенасыщение. Концентрация очень нерастворимых веществ в растворе очень мала и ее трудно определить. Используемые методы делятся на две категории: статические и динамические.
В статических методах смесь доводят до равновесия и концентрацию веществ в фазе раствора определяют химическим анализом . Обычно для этого требуется разделение твердой фазы и фазы раствора. Для этого уравновешивание и разделение следует проводить в термостатируемом помещении. [15] Очень низкие концентрации могут быть измерены, если радиоактивный индикатор включен в твердую фазу.
Разновидностью статического метода является добавление раствора вещества в неводном растворителе, например диметилсульфоксиде , к водной буферной смеси. [16] Может сразу же выпасть осадок, образуя мутную смесь. Растворимость, измеренная для такой смеси, известна как «кинетическая растворимость». Мутность возникает из-за того, что частицы осадка очень малы, что приводит к рассеянию Тиндаля . Фактически частицы настолько малы, что в игру вступает эффект размера частиц, а кинетическая растворимость часто превышает равновесную растворимость. Со временем мутность исчезнет по мере увеличения размера кристаллитов, и в конечном итоге будет достигнуто равновесие в процессе, известном как старение преципитата. [17]
Значения растворимости органических кислот, оснований и амфолитов, представляющих фармацевтический интерес, можно получить с помощью процесса, называемого «поиск равновесной растворимости». [18] В этой процедуре некоторое количество вещества сначала растворяется при pH, при котором оно существует преимущественно в ионизированной форме, а затем при изменении pH образуется осадок нейтральных (неионизированных) частиц. Впоследствии отслеживают скорость изменения pH из-за осаждения или растворения и добавляют титрант сильной кислоты и основания для корректировки pH и обнаружения условий равновесия, когда эти две скорости равны. Преимущество этого метода в том, что он относительно быстрый, поскольку количество образующегося осадка довольно мало. Однако на производительность метода может повлиять образование пересыщенных растворов.
Для проведения расчетов существует ряд компьютерных программ. Они включают: