
Calcium metabolism is the movement and regulation of calcium ions (Ca2+) in (via the gut) and out (via the gut and kidneys) of the body, and between body compartments: the blood plasma, the extracellular and intracellular fluids, and bone. Bone acts as a calcium storage center for deposits and withdrawals as needed by the blood via continual bone remodeling.[1]: 276–277
An important aspect of calcium metabolism is plasma calcium homeostasis, the regulation of calcium ions in the blood plasma within narrow limits.[2] The level of the calcium in plasma is regulated by the hormones parathyroid hormone (PTH) and calcitonin. PTH is released by the chief cells of the parathyroid glands when the plasma calcium level falls below the normal range in order to raise it; calcitonin is released by the parafollicular cells of the thyroid gland when the plasma level of calcium is above the normal range in order to lower it.
Calcium is the most abundant mineral in the human body.[3] The average adult body contains in total approximately 1 kg, 99% in the skeleton in the form of calcium phosphate salts.[3] The extracellular fluid (ECF) contains approximately 22 mmol, of which about 9 mmol is in the plasma.[4] Approximately 10 mmol of calcium is exchanged between bone and the ECF over a period of twenty-four hours.[5]
The concentration of calcium ions inside cells (in the intracellular fluid) is more than 7,000 times lower than in the blood plasma (i.e. at <0.0002 mmol/L, compared with 1.4 mmol/L in the plasma)
Концентрация общего кальция в плазме находится в диапазоне 2,2–2,6 ммоль/л (9–10,5 мг/дл), а нормальная концентрация ионизированного кальция – 1,3–1,5 ммоль/л (4,5–5,6 мг/дл). [4] Количество общего кальция в крови варьируется в зависимости от уровня альбумина плазмы , наиболее распространенного белка в плазме и, следовательно, основного переносчика связанного с белками кальция в крови. Однако биологический эффект кальция определяется количеством ионизированного кальция , а не общего кальция. Таким образом, именно уровень ионизированного кальция в плазме жестко регулируется , чтобы оставаться в очень узких пределах с помощью гомеостатических систем отрицательной обратной связи .
От 35 до 50% кальция в плазме связано с белками, а 5–10% находится в форме комплексов с органическими кислотами и фосфатами. Остальная часть (50–60%) ионизирована. Ионизированный кальций может быть определен непосредственно колориметрически или считан по номограммам , хотя полезность последнего ограничена, когда pH и содержание белка в плазме сильно отклоняются от нормы. [4]
Кальций выполняет несколько основных функций в организме.
Он легко связывается с белками, особенно с белками, боковые цепи которых оканчиваются карбоксильными (-COOH) группами (например, остатками глутамата). Когда происходит такое связывание, электрические заряды в белковой цепи изменяются, вызывая изменение третичной структуры белка (т.е. трехмерной формы). Хорошими примерами этого являются некоторые факторы свертывания крови в плазме крови, которые не функционируют в отсутствие ионов кальция, но становятся полностью функциональными при добавлении солей кальция в правильной концентрации.
Потенциал -управляемые ионные каналы натрия в клеточных мембранах нервов и мышц особенно чувствительны к концентрации ионов кальция в плазме. [6] Относительно небольшое снижение уровня ионизированного кальция в плазме ( гипокальциемия ) приводит к тому, что эти каналы пропускают натрий в нервные клетки или аксоны, делая их гипервозбудимыми ( положительный батмотропный эффект ), вызывая тем самым спонтанные мышечные спазмы ( тетания ) и парестезии ( ощущение «иголок») в конечностях и вокруг рта. [7] Когда уровень ионизированного кальция в плазме повышается выше нормы ( гиперкальциемия ), больше кальция связывается с этими натриевыми каналами, оказывая на них отрицательное батмотропное действие, вызывая летаргию, мышечную слабость, анорексию, запоры и лабильные эмоции. [7]
Поскольку внутриклеточная концентрация ионов кальция чрезвычайно низка (см. выше), поступление незначительных количеств ионов кальция из эндоплазматического ретикулума или из внеклеточной жидкости вызывает быстрые, очень заметные и легко обратимые изменения относительной концентрации этих ионов в клетках. цитозоль . Таким образом, он может служить очень эффективным внутриклеточным сигналом (или « вторым мессенджером ») при различных обстоятельствах, включая сокращение мышц , высвобождение гормонов (например, инсулина из бета-клеток в островках поджелудочной железы ) или нейротрансмиттеров (например, ацетилхолина из клеток поджелудочной железы). -синаптические окончания нервов) и другие функции.
Кальций структурно действует как поддерживающий материал в костях как гидроксиапатит кальция (Ca 10 (PO 4 ) 6 (OH) 2 ).
В скелетных и сердечных мышцах ионы кальция, высвобождаемые из саркоплазматической сети ( эндоплазматической сети поперечнополосатых мышц ), связываются с белком тропонином С , присутствующим на актинсодержащих тонких нитях миофибрилл . В результате изменяется трехмерная структура тропонина , в результате чего тропомиозин , к которому он прикреплен, откатывается от мест связывания миозина на молекулах актина , которые образуют основу тонких нитей. Затем миозин может связываться с открытыми участками связывания миозина на тонкой нити, подвергаясь повторяющейся серии конформационных изменений, называемых циклом поперечных мостиков , для которых АТФ обеспечивает энергию. В течение цикла каждый миозиновый белок «движется» вдоль тонкой актиновой нити, неоднократно связываясь с участками связывания миозина вдоль актиновой нити, щелкая и отпуская ее. Фактически, толстая нить перемещается или скользит вдоль тонкой нити, что приводит к сокращению мышц . Этот процесс известен как модель мышечного сокращения скользящей нити . [8] [9] [10] [11] [12]
Не весь кальций, содержащийся в рационе, легко усваивается из кишечника. Наиболее легко усваиваемый кальций содержится в молочных продуктах (72 %), овощах (7 %), зерновых (5 %), бобовых (4 %), фруктах (3 %), белке (3 %). Кальций, содержащийся в растительных веществах, часто образует комплексы с фитатами , [13] оксалатами , [14] цитратом и другими органическими кислотами, такими как длинноцепочечные жирные кислоты (например, пальмитиновая кислота ), с которыми кальций связывается с образованием нерастворимых кальциевых мыл. [15]
Поток кальция в кость и из кости может быть положительным, отрицательным или нейтральным. Когда он нейтральный, в сутки перерабатывается около 5–10 ммоль. Кости служат важным местом хранения кальция, поскольку они содержат 99% общего количества кальция в организме. Высвобождение кальция из костей регулируется паратгормоном совместно с кальцитриолом , вырабатываемым в почках под влиянием ПТГ. Кальцитонин (гормон, секретируемый щитовидной железой, когда уровни ионизированного кальция в плазме высоки или растут; не путать с «кальцитриолом», который вырабатывается в почках) стимулирует включение кальция в кость.
Нормальный рацион взрослого человека содержит около 25 ммоль кальция в день. Лишь около 5 ммоль этого вещества всасывается в организм в день (см. ниже). [16]
Кальций всасывается через мембрану щеточной каймы эпителиальных клеток кишечника . Было высказано предположение, что канал TRPV6 является основным игроком в поглощении Ca 2+ в кишечнике . [17] Однако у мышей Trpv6 KO не наблюдалось значительного снижения уровня кальция в сыворотке и наблюдалось лишь незначительное снижение [17] или даже неизмененное всасывание Ca 2+ в кишечнике , [18] [19] что указывает на то, что должны существовать другие пути всасывания. Недавно TRPM7 был связан с поглощением кальция в кишечнике. Авторы смогли показать, что кишечная делеция TRPM7 приводит к сильному снижению уровня кальция в сыворотке и костях [20] и интенсивному повышению уровней кальцитриола и ПТГ , что указывает на то, что TRPM7 необходим для общего поглощения кальция в кишечнике. После клеточного поглощения кальций немедленно связывается с кальбиндином , витамин D-зависимым кальцийсвязывающим белком . Кальбиндин переносит кальций непосредственно в эндоплазматический ретикулум эпителиальной клетки , через который кальций переносится к базальной мембране на противоположной стороне клетки, не попадая в ее цитозоль или внутриклеточную жидкость. Оттуда кальциевые насосы ( PMCA1 ) активно транспортируют кальций в организм. [21] Активный транспорт кальция происходит преимущественно в двенадцатиперстной кишке, когда потребление кальция низкое; и посредством пассивного парацеллюлярного транспорта в тощей и подвздошной кишке при высоком потреблении кальция, независимо от уровня витамина D. [22]
Активное всасывание кальция из кишечника регулируется концентрацией кальцитриола (или 1,25-дигидроксихолекальциферола, или 1,25-дигидроксивитамина D 3 ) в крови. Кальцитриол – производное холестерина. Под воздействием ультрафиолета на кожу холестерин превращается в превитамин D3, который спонтанно изомеризуется в витамин D3 ( или холекальциферол). Затем в печени он преобразуется из холекальциферола в кальцифедиол. [23] Под влиянием паратиреоидного гормона почки превращают кальцифедиол в активный гормон кальцитриол, который действует на эпителиальные клетки ( энтероциты ) , выстилающие тонкий кишечник, увеличивая скорость всасывания кальция из содержимого кишечника. Вкратце цикл следующий:
Низкие уровни ПТГ в крови (которые возникают в физиологических условиях, когда уровень ионизированного кальция в плазме высок) ингибируют превращение холекальциферола в кальцитриол, что, в свою очередь, ингибирует всасывание кальция из кишечника. Обратное происходит, когда уровень ионизированного кальция в плазме низкий: паратиреоидный гормон секретируется в кровь, и почки превращают больше кальцифедиола в активный кальцитриол, увеличивая всасывание кальция из кишечника. [24]
Поскольку около 15 ммоль кальция выводится в кишечник с желчью в день, [4] общее количество кальция, которое ежедневно достигает двенадцатиперстной и тощей кишки, составляет около 40 ммоль (25 ммоль с пищей плюс 15 ммоль с желчью). , из которых в среднем 20 ммоль всасывается (обратно) в кровь. Конечным результатом является то, что из кишечника всасывается примерно на 5 ммоль больше кальция, чем выводится в него с желчью. Если нет активного формирования костной ткани (как в детстве) или повышенная потребность в кальции во время беременности и лактации, 5 ммоль кальция, всасывающегося из кишечника, компенсируют потери с мочой, которые регулируются лишь частично. [16]
Почки фильтруют 250 ммоль ионов кальция в день в промоче (или клубочковый фильтрат ) и резорбируют 245 ммоль, что приводит к чистой средней потере с мочой около 5 ммоль/сут. Количество ионов кальция, выделяемых с мочой за сутки, частично находится под влиянием уровня паратгормона (ПТГ) в плазме: высокие уровни ПТГ снижают скорость выведения ионов кальция, а низкие уровни ее увеличивают. [примечание 1] Однако паратиреоидный гормон оказывает большее влияние на количество ионов фосфата (HPO 4 2- ), выделяющихся с мочой. [25] Фосфаты в сочетании с ионами кальция образуют нерастворимые соли. Таким образом, высокие концентрации HPO 4 2- в плазме снижают уровень ионизированного кальция во внеклеточных жидкостях. Таким образом, выделение с мочой большего количества фосфатов, чем ионов кальция, повышает уровень ионизированного кальция в плазме, хотя общая концентрация кальция может быть снижена.
Почки влияют на концентрацию ионизированного кальция в плазме еще одним способом. Он перерабатывает витамин D3 в кальцитриол , активную форму, которая наиболее эффективно способствует всасыванию кальция в кишечнике. Этому превращению витамина D3 в кальцитриол также способствует высокий уровень паратгормона в плазме. [24] [26]
Большая часть избытка кальция выводится через желчь и кал, поскольку уровни кальцитриола в плазме (которые в конечном итоге зависят от уровня кальция в плазме) регулируют, сколько кальция в желчи реабсорбируется из содержимого кишечника.
Экскреция кальция с мочой обычно составляет около 5 ммоль (200 мг)/день. Это меньше по сравнению с тем, что выводится с калом (15 ммоль/сут).
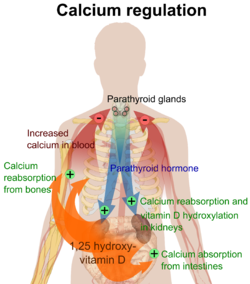
Концентрация ионизированного кальция в плазме регулируется в узких пределах (1,3–1,5 ммоль/л). Это достигается за счет того, что как парафолликулярные клетки щитовидной железы, так и паращитовидные железы постоянно воспринимают (т. е. измеряют) концентрацию ионов кальция в протекающей через них крови.
Когда концентрация кальция повышается, парафолликулярные клетки щитовидной железы увеличивают секрецию в кровь кальцитонина — полипептидного гормона. В то же время паращитовидные железы снижают секрецию в кровь паратиреоидного гормона (ПТГ), также полипептидного гормона. Возникающий в результате высокий уровень кальцитонина в крови стимулирует остеобласты костей удалять кальций из плазмы крови и откладывать его в кости.
Сниженный уровень ПТГ препятствует удалению кальция из скелета. Низкий уровень ПТГ имеет несколько других эффектов: увеличивается потеря кальция с мочой, но, что более важно, подавляется потеря ионов фосфата с мочой. Таким образом, ионы фосфата будут удерживаться в плазме, где они образуют нерастворимые соли с ионами кальция, тем самым удаляя их из пула ионизированного кальция в крови. Низкие уровни ПТГ также ингибируют образование кальцитриола (не путать с кальцитонином ) из холекальциферола (витамина D3 ) почками.
Снижение концентрации кальцитриола в крови действует (сравнительно медленно) на эпителиальные клетки ( энтероциты ) двенадцатиперстной кишки, подавляя их способность усваивать кальций из кишечного содержимого. [2] [5] [28] [29] Низкие уровни кальцитриола также действуют на кости, заставляя остеокласты выделять меньше ионов кальция в плазму крови. [25]

Когда уровень ионизированного кальция в плазме низкий или падает, происходит обратное. Секреция кальцитонина ингибируется и стимулируется секреция ПТГ, в результате чего кальций выводится из костей, что позволяет быстро корректировать уровень кальция в плазме. Высокие уровни ПТГ в плазме ингибируют потерю кальция с мочой, одновременно стимулируя выведение ионов фосфата этим путем. Они также стимулируют почки вырабатывать кальцитриол (стероидный гормон), который повышает способность клеток, выстилающих кишечник, поглощать кальций из содержимого кишечника в кровь, стимулируя выработку кальбиндина в этих клетках. Стимулируемая ПТГ выработка кальцитриола также вызывает высвобождение кальция из кости в кровь за счет высвобождения RANKL ( цитокина или местного гормона ) из остеобластов , что увеличивает резорбтивную активность кости остеокластами. Однако это относительно медленные процессы [2] [5] [25] [28] [29]
Таким образом, быстрая краткосрочная регуляция уровня ионизированного кальция в плазме в первую очередь предполагает быстрое перемещение кальция в скелет или из него. Долгосрочная регуляция достигается за счет регулирования количества кальция, всасываемого из кишечника или выводимого с калом. [2] [5] [28] [29]
Гипокальциемия (низкий уровень кальция в крови) и гиперкальциемия (высокий уровень кальция в крови) являются серьезными заболеваниями. Остеопороз , остеомаляция и рахит представляют собой заболевания костей, связанные с нарушениями обмена кальция и воздействием витамина D. Почечная остеодистрофия является следствием хронической почечной недостаточности , связанной с нарушением обмена кальция.
Диета, достаточно богатая кальцием, может уменьшить потерю кальция из костей с возрастом (постменопаузой ) . [30] Низкое потребление кальция с пищей может быть фактором риска развития остеопороза в более позднем возрасте; а диета с постоянным достаточным количеством кальция может снизить риск остеопороза.
Роль, которую кальций может играть в снижении заболеваемости колоректальным раком, была предметом многих исследований. Однако, учитывая его скромную эффективность, в настоящее время не существует медицинских рекомендаций по использованию кальция для уменьшения рака.
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка )