Стрептавидин / ˌ s t r ɛ p ˈ t æ v ɪ d ɪ n / представляет собой 52 кДа белок (тетрамер), очищенный из бактерии Streptomyces avidinii . Гомо-тетрамеры стрептавидина обладают необычайно высоким сродством к биотину (также известному как витамин B7 или витамин H). При константе диссоциации (K d ) порядка ≈10 −14 моль/л [1] связывание биотина со стрептавидином является одним из самых сильных нековалентных взаимодействий, известных в природе. Стрептавидин широко используется в молекулярной биологии и бионанотехнологии благодаря устойчивости комплекса стрептавидин-биотин к органическим растворителям, денатурантам (например, хлориду гуанидиния ), детергентам (например, SDS , Тритону X-100 ), протеолитическим ферментам и экстремальным значениям температуры и pH.
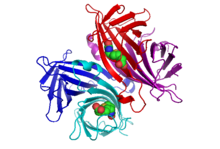
Кристаллическая структура стрептавидина со связанным биотином была сообщена двумя группами в 1989 году. Структура была решена с помощью многоволновой аномальной дифракции Хендриксоном и др. [2] в Колумбийском университете и с помощью множественной изоморфной замены Вебером и др. [3] в Центральном отделе исследований и разработок EI DuPont. По состоянию на сентябрь 2017 года в Банке данных белков депонирована 171 структура . Полный список см. по этой ссылке. Концы N и C полноразмерного белка из 159 остатков обрабатываются для получения более короткого «ядра» стрептавидина, обычно состоящего из остатков 13–139; удаление концов N и C необходимо для наивысшей аффинности связывания биотина. Вторичная структура мономера стрептавидина состоит из восьми антипараллельных β-нитей, которые складываются, образуя антипараллельную третичную структуру β-цилиндра . Сайт связывания биотина расположен на одном конце каждого β-ствола. Четыре идентичных мономера стрептавидина (т. е. четыре идентичных β-ствола) ассоциируются, образуя тетрамерную четвертичную структуру стрептавидина. Сайт связывания биотина в каждом стволе состоит из остатков из внутренней части ствола вместе с консервативным Trp120 из соседней субъединицы. Таким образом, каждая субъединица вносит вклад в сайт связывания на соседней субъединице, и поэтому тетрамер также можно считать димером функциональных димеров.
Многочисленные кристаллические структуры комплекса стрептавидин-биотин пролили свет на происхождение замечательного сродства. Во-первых, существует высокая комплементарность формы между связывающим карманом и биотином. Во-вторых, существует обширная сеть водородных связей, образованных с биотином, когда он находится в месте связывания. Существует восемь водородных связей, непосредственно созданных с остатками в месте связывания (так называемая «первая оболочка» водородных связей), включающая остатки Asn23, Tyr43, Ser27, Ser45, Asn49, Ser88, Thr90 и Asp128. Существует также «вторая оболочка» водородных связей, включающая остатки, которые взаимодействуют с остатками первой оболочки. Однако сродство стрептавидин-биотин превышает то, которое можно было бы предсказать только из взаимодействий водородных связей, что предполагает другой механизм, способствующий высокому сродству. [4] Карман связывания биотина является гидрофобным , и существуют многочисленные контакты, опосредованные силами Ван-дер-Ваальса , и гидрофобные взаимодействия, возникающие с биотином, когда он находится в кармане, что, как полагают, также объясняет высокое сродство. В частности, карман выстлан консервативными остатками триптофана. Наконец, связывание биотина сопровождается стабилизацией гибкой петли, соединяющей β-нити 3 и 4 (L3/4), которая закрывается над связанным биотином, действуя как «крышка» над карманом связывания и способствуя чрезвычайно медленной скорости диссоциации биотина.
Большинство попыток мутации стрептавидина приводят к снижению сродства связывания биотина, что и следовало ожидать в такой высокооптимизированной системе. Однако недавно созданный мутант стрептавидина, названный траптавидином, показал более чем десятикратную более медленную диссоциацию биотина, а также более высокую термическую и механическую стабильность. [5] Это снижение скорости диссоциации сопровождалось двукратным снижением скорости ассоциации.
Сродство к связыванию биотина может быть нарушено путем химической маркировки стрептавидина, например, с помощью аминореактивных флуорофоров ; флавидин представляет собой мутант стрептавидина без боковых цепей лизина, который сохраняет хорошие характеристики связывания биотина после такой маркировки флуоресцентным красителем, когда краситель соединяется с аминоконцом. [6]
Среди наиболее распространенных применений стрептавидина — очистка или обнаружение различных биомолекул. Сильное взаимодействие стрептавидина и биотина может использоваться для прикрепления различных биомолекул друг к другу или к твердой подложке. Для разрыва взаимодействия стрептавидина и биотина необходимы жесткие условия, что часто денатурирует очищаемый интересующий белок. Однако было показано, что кратковременная инкубация в воде при температуре выше 70 °C обратимо разорвет взаимодействие (по крайней мере, для биотинилированной ДНК) без денатурации стрептавидина, что позволяет повторно использовать твердую подложку стрептавидина. [7] Еще одним применением стрептавидина является очистка и обнаружение белков, генетически модифицированных с помощью пептида Strep-tag . Стрептавидин широко используется в вестерн-блоттинге и иммуноанализах, конъюгированных с некоторой репортерной молекулой, такой как пероксидаза хрена . Стрептавидин также использовался в развивающейся области нанобиотехнологии , использовании биологических молекул, таких как белки или липиды, для создания наномасштабных устройств/структур. В этом контексте стрептавидин может использоваться в качестве строительного блока для связывания биотинилированных молекул ДНК для создания однослойных углеродных нанотрубчатых каркасов [8] или даже сложных ДНК-полиэдров. [9] Тетрамерный стрептавидин также использовался в качестве концентратора, вокруг которого могут быть организованы другие белки, либо с помощью аффинной метки, такой как Strep-tag или AviTag , либо путем генетического слияния со SpyTag . [10] Слияние со SpyTag позволило создать сборки с 8 или 20 субъединицами стрептавидина. Помимо молекулярно-силового зонда для исследований с помощью атомно-силовой микроскопии , [11] также были созданы новые материалы, такие как трехмерные кристаллические решетки [12] . Стрептавидин имеет слабокислую изоэлектрическую точку (pI) около 5, но в продаже также имеется рекомбинантная форма стрептавидина с почти нейтральной pI.
Предварительно направленная иммунотерапия использует стрептавидин, конъюгированный с моноклональным антителом против антигенов, специфичных для раковых клеток, с последующей инъекцией радиоактивно меченого биотина для доставки радиации только к раковой клетке. Первоначальные препятствия включают насыщение участков связывания биотина на стрептавидине эндогенным биотином вместо введенного радиоактивно меченого биотина и высокую степень радиоактивного воздействия на почки из-за сильных клеточных адсорбционных свойств стрептавидина. В настоящее время считается, что этот высокий уровень связывания с адгезивными типами клеток, такими как активированные тромбоциты и меланомы, является результатом связывания интегрина , опосредованного последовательностью RYD в стрептавидине. [13]

Стрептавидин является тетрамером, и каждая субъединица связывает биотин с равным сродством. Мультивалентность является преимуществом в таких приложениях, как окрашивание тетрамеров MHC , где эффекты авидности улучшают способность молекул MHC, прикрепленных к стрептавидину, обнаруживать определенные Т-клетки. [14] В других случаях, таких как использование стрептавидина для визуализации определенных белков на клетках, мультивалентность может нарушить функцию интересующего белка. Моновалентный стрептавидин является сконструированной рекомбинантной формой стрептавидина, которая является тетрамером, но только один из четырех участков связывания является функциональным. Этот единственный участок связывания имеет сродство 10−14 моль /л и не может вызывать сшивание. [15] Применения моновалентного стрептавидина включают флуоресцентное отслеживание рецепторов клеточной поверхности , декорирование ДНК-оригами и использование в качестве указателя для идентификации определенных областей для криоэлектронной микроскопии .
Мономерный стрептавидин — это рекомбинантная форма стрептавидина с мутациями, которые разбивают тетрамер на мономер и повышают растворимость полученной изолированной субъединицы. Мономерные версии стрептавидина имеют сродство к биотину 10−7 моль /л 10−8 моль /л и поэтому не являются идеальными для маркировки, но полезны для очистки, где желательна обратимость. [16] [17]

Стрептавидин с двумя сайтами связывания биотина на тетрамер может быть получен путем смешивания субъединиц с функциональным сайтом связывания биотина и без него и очистки с помощью ионообменной хроматографии . Функциональные сайты связывания здесь имеют ту же стабильность связывания биотина, что и стрептавидин дикого типа. Двухвалентный стрептавидин с двумя сайтами связывания биотина вместе (цис-дивалент) или порознь (транс-дивалент) может быть очищен отдельно. [18]
Стрептавидин с тремя сайтами связывания биотина на тетрамер также может быть получен с использованием того же принципа, что и для получения двухвалентных стрептавидинов. [19]
Стрептавидины более высокой валентности были получены путем использования химии конъюгации изопептидных связей с использованием технологии SpyTag/SpyCatcher . [20] Это включает в себя наличие тетрамера стрептавидина с тремя сайтами связывания биотина и мертвого стрептавидина, слитого либо со SpyTag, либо со SpyCatcher. Когда различные тетрамеры смешиваются вместе, происходит ковалентная связь, что обеспечивает большее количество сайтов связывания биотина. С помощью этого метода было получено шесть и двенадцать сайтов связывания биотина на молекулу.
Стрептавидин — не единственный белок, способный связываться с биотином с высокой аффинностью. Авидин — другой наиболее заметный биотинсвязывающий белок. Первоначально выделенный из яичного желтка, авидин имеет только 30% идентичности последовательности со стрептавидином, но почти идентичную вторичную, третичную и четвертичную структуру. Авидин имеет более высокую аффинность к биотину ( Kd ~ 10−15 M ), но в отличие от стрептавидина, авидин гликозилирован, положительно заряжен, обладает псевдокаталитической активностью (авидин может усиливать щелочной гидролиз сложноэфирной связи между биотином и нитрофенильной группой) и имеет более высокую тенденцию к агрегации. С другой стороны, стрептавидин является лучшим связывателем конъюгата биотина; Авидин имеет более низкую аффинность связывания, чем стрептавидин, когда биотин конъюгирован с другой молекулой, несмотря на то, что авидин имеет более высокую аффинность к свободному, неконъюгированному биотину. Поскольку стрептавидин не имеет никаких углеводных модификаций и имеет почти нейтральный pI , он имеет преимущество в виде гораздо более низкого неспецифического связывания, чем авидин. Дегликозилированный авидин (NeutrAvidin) более сопоставим с размером, pI и неспецифическим связыванием стрептавидина.
Группы, исследующие и разрабатывающие стрептавидин или белки семейства авидина (в алфавитном порядке)