Сфингомиелинфосфодиэстераза (EC 3.1.4.12, также известная как нейтральная сфингомиелиназа , сфингомиелиназа или SMase ; систематическое название сфингомиелинхолинфосфогидролаза ) представляет собой фермент гидролазу , который участвует в реакциях метаболизма сфинголипидов . SMase является членом суперсемейства ферментов ДНКазы I и отвечает за расщепление сфингомиелина (SM) на фосфохолин и церамид . Активация SMase была предложена как основной путь производства церамидов в ответ на клеточный стресс. [2]
Идентифицировано пять типов SMase. Они классифицируются в зависимости от катионной зависимости и оптимального значения pH и включают:
Из них лизосомальная кислая SMase и магнийзависимая нейтральная SMase считаются основными кандидатами на выработку церамидов в клеточном ответе на стресс.
Активность нейтральной сфингомиелиназы (N-SMase) была впервые описана в фибробластах пациентов с болезнью Нимана-Пика – лизосомальной болезнью накопления, характеризующейся дефицитом кислой SMase. [3] Последующее исследование показало, что этот фермент является продуктом отдельного гена, имеет оптимальный pH 7,4, активность зависит от ионов Mg 2+ и его особенно много в мозге. [4] Однако более недавнее исследование на головном мозге крупного рогатого скота показало существование множества изоформ N-SMase с различными биохимическими и хроматографическими свойствами. [5]
Крупный прорыв произошел в середине 1980-х годов с клонированием первых N-SMase из Bacillus cereus и Staphylococcus aureus . [6] [7] Использование последовательностей этих бактериальных сфингомиелиназ в поиске гомологии в конечном итоге привело к идентификации дрожжевых N-SMase ISC1 в почкующихся дрожжах Saccharomyces cerevisiae [8] и ферментов N-SMase млекопитающих, nSMase1 и nSMase2. [9] [10] Идентичность между SMase млекопитающих, дрожжей и бактерий очень низка - она составляет примерно 20% между nSMase2 и SMase B. cereus. Однако выравнивание последовательностей (см. рисунок) указывает на наличие ряда консервативных остатков во всем семействе, особенно в каталитической области ферментов. [11] Это привело к предположению об общем каталитическом механизме для семейства N-SMase.
Третий белок N-SMase, названный nSMase3 , был клонирован и охарактеризован в 2006 году. [12] nSMase3 имеет незначительное сходство последовательностей ни с nSMase1, ни с nSMase2. Однако, по-видимому, существует высокая степень эволюционной консервативности от низших к высшим организмам, что позволяет предположить, что он может содержать уникальную и отличную N-SMase. Высокая экспрессия nSMase3 в сердце и скелетных мышцах также предполагает потенциальную роль в функции сердца. [13]

Решение кристаллической структуры нейтральной сфингомиелиназы Listeria ivanovii и Bacillus cereus позволило более полно понять их ферментативный сайт. Активный центр SMазы B. cereus содержит остатки Asn -16, Glu -53, Asp -195, Asn-197 и His -296. Известно, что из них остатки Glu-53, Asp-195 и His-296 необходимы для активности. Относительная каталитическая активность SMase при связывании ионов металлов с активным центром была изучена для ионов двухвалентных металлов Co 2+ , Mn 2+ , Mg 2+ , Ca 2+ и Sr 2+ . Из этих пяти ионов металлов Co 2+ , Mn 2+ и Mg 2+ , связанные с активным центром, приводят к высокой каталитической активности SMase. Ca 2+ и Sr 2+ , связанные с активным центром, проявляют значительно меньшую каталитическую активность SMase. Когда один ион Mg 2+ или два иона Co 2+ связываются с активным центром, возникает двойная гексакоординированная геометрия с двумя октаэдрическими бипирамидами для Co 2+ и одной октаэдрической бипирамидой для Mg 2+ . Когда один ион Ca 2+ связывается с активным центром, возникает гепта-координированная геометрия. Таким образом, предполагается, что разница в каталитической активности ионов металлов обусловлена геометрическими различиями. Из Co 2+ и Mg 2+ SMase обладает лучшей реакционной способностью, когда два иона Co 2+ связаны с SMase; когда эти ионы Co 2+ связаны, Glu-53 и His-296 связывают по одному катиону двухвалентного металла. Эти катионы окружены мостиковыми молекулами воды и действуют как кислоты Льюиса . [1]
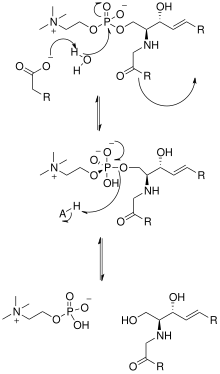
Решение кристаллической структуры нейтральной сфингомиелиназы Listeria ivanovii и Bacillus cereus также пролило свет на их каталитические механизмы. Активный центр SMase содержит остатки Glu и His, каждый из которых связан с одним или двумя катионами двухвалентных металлов, обычно Co 2+ , Mg 2+ или Ca 2+ для оптимальной работы. Эти два катиона участвуют в катализе, привлекая SM к активному центру SMase. Двухвалентный катион, связанный с остатком Glu, взаимодействует с амидокислородом и сложноэфирным кислородом между С1 и фосфатной группой СМ; Остаток Asn и катион двухвалентного металла, связанный с остатком His, связываются с атомами кислорода фосфатной группы СМ. Это стабилизирует отрицательный заряд фосфатной группы. Катион металла, связанный с остатком His и боковыми цепями Asp и Asn, снижает значение pKa одной из мостиковых молекул воды, тем самым активируя молекулу воды. Эта молекула воды затем действует как нуклеофил и атакует фосфатную группу SM, создавая пятивалентный атом фосфора, отрицательный заряд которого стабилизируется катионами двухвалентных металлов. Затем фосфат преобразует свою тетраэдрическую конформацию и приводит к образованию продуктов церамида и фосфохолина . [1] В 2016 году была предложена модель, основанная на исследовании кристаллической структуры кислой сфингомиелиназы млекопитающих, согласно которой ASMase существует в равновесии между открытой и закрытой формами домена сапозина . В отсутствие мембран закрытый ASMasesap, отделенный от ASMasecat, будет преобладать и делать фермент неактивным. В присутствии анионных мембран открытый ASMasesap становится преобладающим, прикрепляется к поверхности мембраны и одновременно образует интерфейс с каталитическим доменом, активируя его для гидролиза сфингомиелина . [14]