Тантал — химический элемент ; он имеет символ Та и атомный номер 73. Ранее известный как танталий , он назван в честь Тантала , персонажа греческой мифологии. [7] Тантал — очень твердый, пластичный , блестящий , сине-серый переходный металл , обладающий высокой коррозионной стойкостью. Он входит в группу тугоплавких металлов , которые широко используются в качестве компонентов прочных тугоплавких сплавов . Это элемент 5-й группы , наряду с ванадием и ниобием , и он всегда встречается в геологических источниках вместе с химически близким ниобием, главным образом в минеральных группах танталита , колумбита и колтана .
Химическая инертность и очень высокая температура плавления тантала делают его ценным для лабораторного и промышленного оборудования, такого как реакционные сосуды и вакуумные печи . Он используется в танталовых конденсаторах для электронного оборудования, такого как компьютеры . Его исследуют на предмет использования в качестве материала для высококачественных сверхпроводящих резонаторов в квантовых процессорах. [8] [9] Европейская комиссия считает тантал технологически важным элементом . [10]
Тантал был открыт в Швеции в 1802 году Андерсом Экебергом в двух образцах минералов — одном из Швеции и другом из Финляндии. [11] [12] Годом ранее Чарльз Хэтчетт открыл колумбий (ныне ниобий), [13] а в 1809 году английский химик Уильям Хайд Волластон сравнил его оксид, колумбит с плотностью 5,918 г/см 3 , с плотностью тантал, танталит плотностью 7,935 г/см 3 . Он пришел к выводу, что два оксида, несмотря на разницу в измеренной плотности, идентичны, и сохранил название «тантал». [14] После того, как Фридрих Вёлер подтвердил эти результаты, считалось, что колумбий и тантал — один и тот же элемент. Этот вывод был оспорен в 1846 году немецким химиком Генрихом Розе , который утверждал, что в образце танталита было два дополнительных элемента, и назвал их в честь детей Тантала : ниобий (от Ниобы , богини слез) и пелопий ( от Пелопса ). [15] [16] Предполагаемый элемент «пелопий» позже был идентифицирован как смесь тантала и ниобия, и было обнаружено, что ниобий идентичен колумбию, уже открытому в 1801 году Хэтчеттом.
Различия между танталом и ниобием были однозначно продемонстрированы в 1864 году Кристианом Вильгельмом Бломстрандом [17] и Анри Этьеном Сент-Клер Девилем , а также Луи Дж. Тростом , определившим эмпирические формулы некоторых их соединений в 1865 году . [ 17] [18] Дальнейшее подтверждение пришло от швейцарского химика Жана Шарля Галиссара де Мариньяка , [19] в 1866 году, который доказал, что существует только два элемента. Эти открытия не мешали ученым публиковать статьи о так называемом ильмениуме до 1871 года . [20] Де Мариньяк был первым, кто получил металлическую форму тантала в 1864 году, когда он восстановил хлорид тантала, нагревая его в атмосфере водорода . [21] Первые исследователи могли производить только нечистый тантал, а первый относительно чистый пластичный металл был произведен Вернером фон Болтоном в Шарлоттенбурге в 1903 году. Провода, изготовленные из металлического тантала, использовались для нитей накаливания лампочек , пока вольфрам не заменил его в широком использовании. . [22]
Название тантал произошло от имени мифологического Тантала, отца Ниобеи в греческой мифологии . По сюжету, после смерти он был наказан тем, что был приговорен стоять по колено в воде, а над его головой росли прекрасные плоды, и то и другое вечно мучило его. (Если он наклонялся, чтобы выпить воду, она стекала ниже уровня, которого он мог достать, а если он тянулся к фруктам, ветки уходили из его рук.) [23] Андерс Экеберг писал: «Этот металл я называю танталом … отчасти намеком на его неспособность при погружении в кислоту поглощать ее и насыщаться». [24]
На протяжении десятилетий коммерческая технология отделения тантала от ниобия включала фракционную кристаллизацию гептафторотанталата калия из моногидрата оксипентафторниобата калия - процесс, открытый Жаном Шарлем Галиссаром де Мариньяком в 1866 году. Этот метод был вытеснен экстракцией растворителем из фторидсодержащих веществ. растворы тантала. [18]
Тантал темный (сине-серый), [25] плотный, пластичный, очень твердый, легко поддающийся обработке и обладающий высокой проводимостью тепла и электричества. Металл известен своей устойчивостью к коррозии кислотами ; Фактически, при температуре ниже 150 ° C тантал почти полностью невосприимчив к воздействию обычно агрессивной царской водки . Его можно растворить плавиковой кислотой или кислыми растворами, содержащими фторид- ион и триоксид серы , а также расплавленным гидроксидом калия . Высокая температура плавления тантала 3017 ° C (точка кипения 5458 ° C) среди элементов превышает только вольфрам , рений и осмий для металлов, а также углерод .
Тантал существует в двух кристаллических фазах: альфа и бета. Альфа-фаза относительно пластична и мягка; имеет объемноцентрированную кубическую структуру ( пространственная группа Im3m , постоянная решетки a = 0,33058 нм), твердость по Кнупу 200–400 HN и удельное сопротивление 15–60 мкОм⋅см. Бета-фаза твердая и хрупкая; его кристаллическая симметрия тетрагональная (пространственная группа P42/mnm , a = 1,0194 нм, c = 0,5313 нм), твердость по Кнупу составляет 1000–1300 HN, а удельное электросопротивление относительно высокое и составляет 170–210 мкОм⋅см. Бета-фаза метастабильна и переходит в альфа-фазу при нагревании до 750–775 °С. Объемный тантал почти полностью представляет собой альфа-фазу, а бета-фаза обычно существует в виде тонких пленок [26] , полученных магнетронным распылением , химическим осаждением из паровой фазы или электрохимическим осаждением из эвтектического раствора расплавленной соли. [27]
Природный тантал состоит из двух стабильных изотопов : 180m Ta (0,012%) и 181 Ta (99,988%). Прогнозируется, что 180m Ta ( m обозначает метастабильное состояние) распадется тремя способами: изомерный переход в основное состояние 180 Ta , бета-распад до 180 W или захват электрона до 180 Hf . Однако радиоактивность этого ядерного изомера никогда не наблюдалась, и установлен лишь нижний предел его периода полураспада — 2,0 × 10 16 лет. [28] Основное состояние 180 Та имеет период полураспада всего 8 часов. 180m Ta — единственный встречающийся в природе ядерный изомер (исключая радиогенные и космогенные короткоживущие нуклиды). Это также самый редкий первичный изотоп во Вселенной, если принять во внимание элементное содержание тантала и изотопное содержание 180m Ta в естественной смеси изотопов (и опять-таки исключая радиогенные и космогенные короткоживущие нуклиды). [29]
Тантал теоретически рассматривался как « солевой » материал для ядерного оружия ( более известным гипотетическим солевым материалом является кобальт ). Внешняя оболочка из 181 Та будет облучена интенсивным потоком нейтронов высокой энергии от гипотетического взрывающегося ядерного оружия. Это превратило бы тантал в радиоактивный изотоп 182 Та, который имеет период полураспада 114,4 дня и производит гамма-лучи с энергией примерно 1,12 миллиона электрон-вольт (МэВ) каждое, что значительно увеличит радиоактивность ядерных осадков от взрыв в течение нескольких месяцев. Насколько общеизвестно, такое «просоленное» оружие никогда не создавалось и не испытывалось, и уж точно никогда не использовалось в качестве оружия. [30]
Тантал может быть использован в качестве мишенного материала для ускоренных протонных пучков для производства различных короткоживущих изотопов, в том числе 8 Li, 80 Rb и 160 Yb. [31]
Тантал образует соединения в степенях окисления от –III до +V. Чаще всего встречаются оксиды Та(V), в состав которого входят все минералы. Химические свойства Та и Nb очень схожи. В водной среде Та проявляет только степень окисления +V. Как и ниобий, тантал плохо растворяется в разбавленных растворах соляной , серной , азотной и фосфорной кислот из-за выпадения в осадок водного оксида Та(V). [32] В основных средах Та может растворяться за счет образования полиоксотанталатных форм. [33]
Пятиокись тантала (Ta 2 O 5 ) является наиболее важным соединением с точки зрения приложений. Оксиды тантала в низших степенях окисления многочисленны, в том числе имеют множество дефектных структур , малоизучены или плохо охарактеризованы. [34]
Танталаты, соединения, содержащие [TaO 4 ] 3- или [TaO 3 ] -, многочисленны. Танталат лития (LiTaO 3 ) имеет структуру перовскита. Танталат лантана (LaTaO 4 ) содержит изолированный TaO .3−
4тетраэдры. [35]
Как и в случае с другими тугоплавкими металлами , наиболее твердыми известными соединениями тантала являются нитриды и карбиды. Карбид тантала TaC, как и более часто используемый карбид вольфрама , представляет собой твердую керамику , которая используется в режущих инструментах. Нитрид тантала (III) используется в качестве тонкопленочного изолятора в некоторых процессах производства микроэлектроники. [36]
Наиболее изученным халькогенидом является TaS 2 , слоистый полупроводник , как и другие дихалькогениды переходных металлов . Сплав тантала и теллура образует квазикристаллы . [35]
Галогениды тантала имеют степени окисления +5, +4 и +3. Пентафторид тантала (TaF 5 ) представляет собой белое твердое вещество с температурой плавления 97,0 °С. Анион [TaF 7 ] 2- используется для его отделения от ниобия. [37] Хлорид TaCl
5, существующий в виде димера, является основным реагентом при синтезе новых соединений Та. Он легко гидролизуется до оксихлорида . Низшие галогениды TaX
4и налог
3, имеют связи Ta-Ta. [35] [32]
Танталорганические соединения включают пентаметилтантал , смешанные хлориды алкилтантала, гидриды алкилтантала, алкилиденовые комплексы, а также их циклопентадиенильные производные. [38] [39] Для гексакарбонила [Ta(CO) 6 ] - и родственных изоцианидов известны различные соли и замещенные производные .


По оценкам, тантал составляет около 1 ppm [40] или 2 ppm [32] земной коры по весу . Существует множество разновидностей минералов тантала, лишь некоторые из которых пока используются промышленностью в качестве сырья: танталит (ряд, состоящий из танталита-(Fe), танталита-(Mn) и танталита-(Mg)), микролита ( теперь название группы), воджинит , эвксенит (на самом деле эвксенит-(Y)) и поликраз (на самом деле поликраз-(Y)). [41] Танталит ( Fe , Mn )Ta 2 O 6 является наиболее важным минералом для добычи тантала. Танталит имеет ту же минеральную структуру, что и колумбит ( Fe , Mn ) (Ta, Nb ) 2 O 6 ; когда тантала больше, чем ниобия, его называют танталитом, а когда ниобия больше, чем тантала, его называют колумбитом (или ниобитом ). Высокая плотность танталита и других танталсодержащих минералов делает использование гравитационного разделения лучшим методом. Другие минералы включают самарскит и фергюсонит .
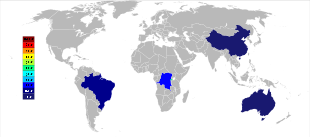
До 2010-х годов Австралия была основным производителем тантала, а Global Advanced Metals (ранее известная как Talison Minerals ) была крупнейшей компанией по добыче тантала в этой стране. Они управляют двумя рудниками в Западной Австралии: Гринбушес на юго-западе и Водгина в регионе Пилбара . Рудник Воджина был вновь открыт в январе 2011 года после того, как добыча на нем была приостановлена в конце 2008 года из-за мирового финансового кризиса . [42] Менее чем через год после возобновления работы компания Global Advanced Metals объявила, что из-за нового «… смягчения спроса на тантал…» и других факторов операции по добыче тантала должны быть прекращены в конце февраля 2012 года. [43] ] Wodgina производит первичный танталовый концентрат, который подвергается дальнейшей переработке на предприятии в Гринбушесе перед продажей покупателям. [44] Хотя крупные производители ниобия находятся в Бразилии и Канаде , руда там также дает небольшой процент тантала. Некоторые другие страны, такие как Китай , Эфиопия и Мозамбик , добывают руды с более высоким содержанием тантала и производят значительную часть его мировой добычи. Тантал также производится в Таиланде и Малайзии как побочный продукт добычи олова . При гравитационном отделении руд россыпных месторождений обнаруживается не только касситерит (SnO 2 ), но и небольшой процент танталита. Шлак оловянных заводов содержит экономически полезные количества тантала, который выщелачивается из шлака. [18] [45]
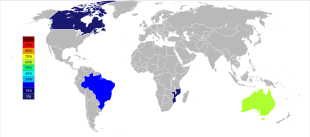
Мировое производство тантала претерпело важный географический сдвиг с начала 21 века, когда добыча осуществлялась преимущественно в Австралии и Бразилии. Начиная с 2007 года и по 2014 год основные источники добычи тантала из рудников резко переместились в Демократическую Республику Конго , Руанду и некоторые другие африканские страны. [46] Будущие источники поставок тантала (в порядке предполагаемого размера) изучаются в Саудовской Аравии , Египте , Гренландии , Китае, Мозамбике, Канаде, Австралии, США , Финляндии и Бразилии. [47] [48]
Тантал считается конфликтным ресурсом . Колтан , промышленное название минерала колумбит - танталит , из которого добывают ниобий и тантал, [49] также можно найти в Центральной Африке , поэтому тантал связывают с войной в Демократической Республике Конго (бывший Заир ). . Согласно докладу Организации Объединенных Наций от 23 октября 2003 г. , [50] контрабанда и экспорт колтана способствовали разжиганию войны в Конго, кризиса, в результате которого с 1998 года погибло около 5,4 миллиона человек [51] – что сделало его самым смертоносным в мире. задокументированный конфликт со времен Второй мировой войны . Были подняты этические вопросы об ответственном корпоративном поведении, правах человека и угрозе дикой природе из-за эксплуатации таких ресурсов, как колтан, в регионах вооруженного конфликта в бассейне Конго . [52] [53] [54] [55] Геологическая служба США сообщает в своем ежегоднике, что в этом регионе производилось чуть менее 1% мирового производства тантала в 2002–2006 годах, достигнув пика в 10% в 2000 и 2008 годах. [45] Данные Геологической службы США, опубликованные в январе 2021 года, показали, что около 40% мировой добычи тантала приходится на Демократическую Республику Конго, а еще 18% — на соседние Руанду и Бурунди . [56]

Извлечение тантала из танталита включает несколько этапов. Сначала минерал измельчается и концентрируется гравитационным разделением . Обычно это делается недалеко от рудника .
Очистка тантала из его руд является одним из наиболее сложных процессов разделения в промышленной металлургии. Основная проблема состоит в том, что танталовые руды содержат значительные количества ниобия , химические свойства которого почти идентичны свойствам Та. Для решения этой проблемы было разработано большое количество процедур.
В наше время разделение достигается с помощью гидрометаллургии . [58] Добыча начинается с выщелачивания руды плавиковой кислотой совместно с серной или соляной кислотой . Этот этап позволяет отделить тантал и ниобий от различных неметаллических примесей в породе. Хотя Та встречается в виде различных минералов, его удобно представлять в виде пентаоксида, поскольку большинство оксидов тантала (V) ведут себя в этих условиях аналогичным образом. Таким образом, упрощенное уравнение для его извлечения выглядит следующим образом:
Совершенно аналогичные реакции происходят с ниобиевым компонентом, но в условиях экстракции обычно преобладает гексафторид.
Эти уравнения упрощены: предполагается, что бисульфат (HSO 4 - ) и хлорид конкурируют как лиганды за ионы Nb(V) и Ta(V) при использовании серной и соляной кислот соответственно. [58] Комплексы фторида тантала и ниобия затем удаляются из водного раствора жидкостно-жидкостной экстракцией в органические растворители , такие как циклогексанон , октанол и метилизобутилкетон . Эта простая процедура позволяет удалить большинство металлосодержащих примесей (например, железа, марганца, титана, циркония), которые остаются в водной фазе в виде их фторидов и других комплексов.
Отделение тантала от ниобия затем достигается за счет снижения ионной силы смеси кислот, что приводит к растворению ниобия в водной фазе. Предполагается, что в этих условиях образуется оксифторид H 2 [NbOF 5 ]. После удаления ниобия раствор очищенного H 2 [TaF 7 ] нейтрализуют водным раствором аммиака для осаждения гидратированного оксида тантала в виде твердого вещества, которое можно прокалить до пятиокиси тантала (Ta 2 O 5 ). [59]
Вместо гидролиза H 2 [TaF 7 ] можно обработать фторидом калия с получением гептафторотанталата калия :
В отличие от H 2 [TaF 7 ], калиевая соль легко кристаллизуется и с ней обращаются как с твердым веществом.
K 2 [TaF 7 ] можно превратить в металлический тантал восстановлением натрием при температуре примерно 800°C в расплавленной соли . [60]
В более старом методе, называемом процессом Мариньяка , смесь H 2 [TaF 7 ] и H 2 [NbOF 5 ] превращалась в смесь K 2 [TaF 7 ] и K 2 [NbOF 5 ], которую затем разделяли. путем фракционной кристаллизации , используя их различную растворимость в воде.
Тантал также можно очистить электролизом, используя модифицированную версию процесса Холла-Эру . Вместо того, чтобы требовать, чтобы входной оксид и выходной металл находились в жидкой форме, электролиз тантала работает с нежидкими порошкообразными оксидами. Первое открытие было сделано в 1997 году, когда исследователи из Кембриджского университета погрузили небольшие образцы некоторых оксидов в ванну с расплавленной солью и восстановили оксид электрическим током. В качестве катода используется порошкообразный оксид металла. Анод изготовлен из углерода. Расплавленная соль при температуре 1000 ° C (1830 ° F) является электролитом. Мощности первого нефтеперерабатывающего завода достаточны для удовлетворения 3–4% годового мирового спроса. [61]
Вся сварка тантала должна производиться в инертной атмосфере аргона или гелия , чтобы защитить его от загрязнения атмосферными газами. Тантал не паяется . Измельчить тантал сложно, особенно отожженный тантал. В отожженном состоянии тантал чрезвычайно пластичен и из него можно легко формовать металлические листы. [62]

Тантал в качестве металлического порошка в основном используется в производстве электронных компонентов, в основном конденсаторов и некоторых мощных резисторов . Танталовые электролитические конденсаторы используют склонность тантала образовывать защитный оксидный поверхностный слой, используя танталовый порошок, спрессованный в форме гранул, в качестве одной «обкладки» конденсатора, оксид в качестве диэлектрика , а электролитический раствор или проводящее твердое вещество в качестве другая «тарелка». Поскольку диэлектрический слой может быть очень тонким (тоньше, чем аналогичный слой, например, в алюминиевом электролитическом конденсаторе), высокая емкость может быть достигнута в небольшом объеме. Благодаря преимуществам в размере и весе танталовые конденсаторы привлекательны для портативных телефонов , персональных компьютеров , автомобильной электроники и фотоаппаратов . [63]
Тантал также используется для производства различных сплавов , которые имеют высокие температуры плавления, прочность и пластичность. Сплавленный другими металлами, он также используется при изготовлении твердосплавных инструментов для металлообрабатывающего оборудования и в производстве суперсплавов для компонентов реактивных двигателей, химического технологического оборудования, ядерных реакторов , деталей ракет, теплообменников, резервуаров и сосудов. [64] [63] [65] Благодаря своей пластичности тантал можно вытягивать в тонкую проволоку или нити, которые используются для испарения таких металлов, как алюминий . Поскольку тантал устойчив к воздействию жидкостей организма и не вызывает раздражений, он широко используется при изготовлении хирургических инструментов и имплантатов. Например, пористые танталовые покрытия используются при изготовлении ортопедических имплантатов из-за способности тантала образовывать прямую связь с твердыми тканями. [66]
Тантал инертен по отношению к большинству кислот, за исключением плавиковой кислоты и горячей серной кислоты , а горячие щелочные растворы также вызывают коррозию тантала. Это свойство делает его полезным металлом для изготовления сосудов для химических реакций и труб для агрессивных жидкостей. Теплообменные змеевики для парового нагрева соляной кислоты изготовлены из тантала. [67] Тантал широко использовался в производстве электронных ламп сверхвысокой частоты для радиопередатчиков. Тантал способен захватывать кислород и азот путем образования нитридов и оксидов и, следовательно, помогает поддерживать высокий вакуум, необходимый для трубок, когда они используются для внутренних частей, таких как решетки и пластины. [37] [67]

Тантал использовался НАСА для защиты компонентов космических кораблей, таких как «Вояджер-1» и «Вояджер-2» , от радиации. [68] Высокая температура плавления и стойкость к окислению привели к использованию металла в производстве деталей вакуумных печей . Тантал чрезвычайно инертен, поэтому из него изготавливают различные коррозионностойкие детали, такие как защитные гильзы , корпуса клапанов и танталовые крепежные детали. Из-за его высокой плотности кумулятивный заряд и вкладыши пенетратора, формируемые взрывным способом, были изготовлены из тантала. [69] Тантал значительно увеличивает бронепробиваемость кумулятивного заряда из-за его высокой плотности и высокой температуры плавления. [70] [71]
Его также иногда используют в драгоценных часах , например, от Audemars Piguet , FP Journe , Hublot , Montblanc , Omega и Panerai . Медицинский исследователь Джеральд Л. Берк впервые заметил в 1940 году, что тантал также обладает высокой биоинертностью и может безопасно использоваться в качестве материала для ортопедических имплантатов. [72] Высокая жесткость тантала делает необходимым использовать его в качестве высокопористой пены или каркаса с более низкой жесткостью для имплантатов замены тазобедренного сустава, чтобы избежать защиты от напряжений . [73] Поскольку тантал является цветным немагнитным металлом, эти имплантаты считаются приемлемыми для пациентов, проходящих процедуры МРТ. [74] Оксид используется для изготовления специального стекла с высоким показателем преломления для объективов фотоаппаратов . [75]
Танталу уделяется гораздо меньше внимания в области окружающей среды, чем в других науках о Земле. Концентрация верхней коры (UCC) и соотношение Nb/Ta в верхней коре и минералах доступны, поскольку эти измерения полезны в качестве геохимического инструмента. [76] Последнее значение концентрации верхней коры составляет 0,92 ppm, а соотношение Nb/Ta(w/w) составляет 12,7. [77]
Имеется мало данных о концентрациях тантала в различных частях окружающей среды, особенно в природных водах, где даже не были получены надежные оценки концентраций «растворенного» тантала в морской и пресной воде. [78] Некоторые значения концентрации растворенных веществ в океанах были опубликованы, но они противоречивы. Значения в пресной воде немного лучше, но во всех случаях они, вероятно, ниже 1 нг/л , поскольку «растворенные» концентрации в природных водах значительно ниже большинства современных аналитических возможностей. [79] Анализ требует процедур предварительного концентрирования, которые на данный момент не дают последовательных результатов. И в любом случае, тантал, по-видимому, присутствует в природных водах в основном в виде твердых частиц, а не в растворенном виде. [78]
Легче определить значения концентраций в почвах, донных отложениях и атмосферных аэрозолях. [78] Значения в почвах близки к 1 ppm и, следовательно, к значениям UCC. Это указывает на детритное происхождение. Для атмосферных аэрозолей имеющиеся значения разрознены и ограничены. Когда наблюдается обогащение тантала, это, вероятно, связано с потерей большего количества водорастворимых элементов в аэрозолях в облаках. [80]
Загрязнения, связанного с использованием этого элемента человеком, не обнаружено. [81] Тантал, по-видимому, является очень консервативным элементом с биогеохимической точки зрения, но его круговорот и реакционная способность до сих пор полностью не изучены.
Соединения, содержащие тантал, редко встречаются в лаборатории. Металл обладает высокой биосовместимостью [72] и используется для изготовления имплантатов и покрытий для тела , поэтому внимание может быть сосредоточено на других элементах или физической природе химического соединения . [82]
Люди могут подвергнуться воздействию тантала на рабочем месте при вдыхании, контакте с кожей или глазами. Управление по охране труда (OSHA) установило законный предел ( допустимый предел воздействия ) для воздействия тантала на рабочем месте на уровне 5 мг/м 3 в течение 8-часового рабочего дня. Национальный институт охраны труда (NIOSH) установил рекомендуемый предел воздействия (REL) 5 мг/м 3 в течение 8-часового рабочего дня и краткосрочный предел 10 мг/м 3 . Танталовая пыль при концентрации 2500 мг/м 3 представляет непосредственную опасность для жизни и здоровья . [83]
Упоминается и является ключевой темой сериала Amazon Prime «Джек Райан» Тома Клэнси (2-й сезон). [84]
{{cite journal}}: Требуется цитировать журнал |journal=( помощь )Снижение спроса на тантал во всем мире и задержки в получении одобрения правительства на установку необходимого дробильного оборудования являются одними из факторов, способствующих принятию этого решения.
{{cite book}}: |journal=игнорируется ( помощь )