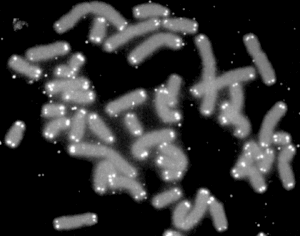
Теломера ( / ˈ t ɛ l ə m ɪər , ˈ t iː l ə -/ ; от древнегреческого τέλος ( télos ) «конец» и μέρος ( méros ) «часть») — это область повторяющихся нуклеотидных последовательностей, связанных со специализированными белки на концах линейных хромосом (см. Последовательности). Теломеры — широко распространенная генетическая особенность, чаще всего встречающаяся у эукариот . У большинства, если не у всех видов, обладающих ими, они защищают концевые участки хромосомной ДНК от прогрессирующей деградации и обеспечивают целостность линейных хромосом, не позволяя системам репарации ДНК принять самые концы цепи ДНК за двухцепочечный разрыв .
Существование особой структуры на концах хромосом было независимо предположено в 1938 году Германом Йозефом Мюллером , изучавшим плодовую мушку Drosophila melanogaster , и в 1939 году Барбарой МакКлинток , работавшей с кукурузой. [1] Мюллер заметил, что на концах облученных хромосом плодовых мух не наблюдалось таких изменений, как делеции или инверсии. Он выдвинул гипотезу о наличии защитного колпачка, который он назвал «теломеры» от греческого « телос» (конец) и «мерос » (часть). [2]
В начале 1970-х годов советский теоретик Алексей Оловников впервые осознал, что хромосомы не могут полностью воспроизводить свои концы; это известно как «проблема конечной репликации». Основываясь на этом и принимая во внимание идею Леонарда Хейфлика об ограниченном делении соматических клеток , Оловников предположил, что последовательности ДНК теряются каждый раз, когда клетка реплицируется, пока потеря не достигнет критического уровня, после чего деление клетки прекращается. [3] [4] [5] Согласно его теории маргинотомии, последовательности ДНК на концах теломер представлены тандемными повторами, которые создают буфер, определяющий количество делений, которым может подвергнуться определенный клеточный клон. Более того, было предсказано, что специализированная ДНК-полимераза (первоначально называвшаяся тандемной ДНК-полимеразой) может удлинять теломеры в иммортализованных тканях, таких как зародышевая линия, раковые клетки и стволовые клетки. Из этой гипотезы также следовало, что организмы с кольцевым геномом, такие как бактерии, не имеют проблемы конечной репликации и, следовательно, не стареют.
В 1975–1977 годах Элизабет Блэкберн , работавшая научным сотрудником в Йельском университете вместе с Джозефом Г. Галлом , открыла необычную природу теломер с их простыми повторяющимися последовательностями ДНК, составляющими концы хромосом. [6] Блэкберн, Кэрол Грейдер и Джек Шостак были удостоены Нобелевской премии по физиологии и медицине 2009 года за открытие того, как хромосомы защищаются теломерами и ферментом теломеразой . [7]

Во время репликации ДНК ДНК-полимераза не может реплицировать последовательности, присутствующие на 3'-концах родительских цепей. Это следствие его однонаправленного способа синтеза ДНК: он может присоединять новые нуклеотиды только к существующему 3'-концу (то есть синтез продолжается 5'-3'), и поэтому для инициации репликации ему требуется праймер . На ведущей цепи (ориентированной 5'-3' внутри репликационной вилки) ДНК-полимераза непрерывно реплицируется от точки инициации до конца цепи с праймером (состоящим из РНК ), который затем вырезается и заменяется ДНК. Однако отстающая цепь ориентирована 3'-5' относительно репликационной вилки, поэтому непрерывная репликация ДНК-полимеразой невозможна, что приводит к необходимости прерывистой репликации, включающей повторный синтез праймеров дальше 5' от места инициации (см . репликация цепи ). Последний праймер, участвующий в репликации отстающей цепи, находится рядом с 3'-концом матрицы (что соответствует потенциальному 5'-концу отстающей цепи). Первоначально считалось, что последний праймер будет находиться в самом конце матрицы, поэтому после его удаления ДНК-полимераза, заменяющая праймеры ДНК (DNA-Pol δ у эукариот) [примечание 1] , не сможет синтезировать праймеры. «замещающая ДНК» с 5'-конца отстающей цепи, чтобы матричные нуклеотиды, ранее спаренные с последним праймером, не реплицировались. [8] С тех пор был поставлен вопрос о том, расположен ли праймер последней отстающей цепи точно на 3'-конце матрицы, и было продемонстрировано, что он скорее синтезируется на расстоянии примерно 70–100 нуклеотидов, что согласуется с открытием. что ДНК в культивируемых клетках человека укорачивается на 50–100 пар оснований за одно деление клетки . [9]
Если в этом процессе кодирующие последовательности деградируют, потенциально жизненно важный генетический код будет потерян. Теломеры представляют собой некодирующие повторяющиеся последовательности, расположенные на концах линейных хромосом и выступающие в качестве буфера для тех кодирующих последовательностей, которые находятся дальше. Они «закрывают» концевые последовательности и постепенно разрушаются в процессе репликации ДНК.
«Проблема репликации концов» характерна исключительно для линейных хромосом, поскольку у кольцевых хромосом нет концов, находящихся вне досягаемости ДНК-полимераз. Большинство прокариот , опирающихся на кольцевые хромосомы, соответственно, не обладают теломерами. [10] Однако небольшая часть бактериальных хромосом (например, у Streptomyces , Agrobacterium и Borrelia ) линейна и обладает теломерами, которые сильно отличаются от хромосом эукариот по структуре и функциям. Известные структуры бактериальных теломер представляют собой белки , связанные с концами линейных хромосом, или шпильки одноцепочечной ДНК на концах линейных хромосом. [11]

На самом 3'-конце теломеры имеется выступ длиной 300 пар оснований, который может проникать в двухцепочечную часть теломеры, образуя структуру, известную как Т-петля. Эта петля аналогична узлу, который стабилизирует теломеры и предотвращает распознавание концов теломер как точек разрыва механизмом восстановления ДНК. Если на концах теломер произойдет негомологическое соединение концов, это приведет к слиянию хромосом. Т-петля поддерживается несколькими белками, которые вместе называются комплексом шелтерина. У человека комплекс шелтерина состоит из шести белков, идентифицированных как TRF1 , TRF2 , TIN2 , POT1 , TPP1 и RAP1 . [12] У многих видов повторы последовательности обогащены гуанином , например, TTAGGG у позвоночных , [13] что позволяет образовывать G-квадруплексы , особую конформацию ДНК, включающую спаривание оснований, отличное от Уотсона-Крика. Существуют различные подтипы в зависимости, среди прочего, от участия одно- или двухцепочечной ДНК. Есть доказательства того, что 3'-выступ у инфузорий (которые обладают повторами теломер, сходными с теми, что обнаружены у позвоночных ) образует такие G-квадруплексы, которые вмещают его, а не Т-петлю. G-квадруплексы представляют собой препятствие для таких ферментов, как ДНК-полимеразы, и поэтому считается, что они участвуют в регуляции репликации и транскрипции. [14]

У многих организмов есть фермент рибонуклеопротеин, называемый теломеразой, который выполняет задачу добавления повторяющихся нуклеотидных последовательностей к концам ДНК. Теломераза «пополняет» «шапочку» теломер и не требует АТФ [15] . В большинстве многоклеточных эукариотических организмов теломераза активна только в зародышевых клетках , некоторых типах стволовых клеток , таких как эмбриональные стволовые клетки , и некоторых лейкоцитах . Теломераза может быть реактивирована, и теломеры возвращаются в эмбриональное состояние путем переноса ядра соматической клетки . [16] Постоянное укорочение теломер при каждой репликации в соматических клетках (тела) может играть роль в старении [17] и предотвращении рака . [18] [19] Это связано с тем, что теломеры действуют как своего рода «предохранитель» с задержкой во времени, который в конечном итоге заканчивается после определенного количества клеточных делений и приводит к возможной потере жизненно важной генетической информации из хромосомы клетки при будущих делениях. . [20] [21]
Длина теломер сильно различается у разных видов: от примерно 300 пар оснований у дрожжей [22] до многих тысяч оснований у человека, и обычно состоит из массивов богатых гуанином повторов длиной от шести до восьми пар оснований. Теломеры эукариот обычно оканчиваются 3'-выступающим одноцепочечным ДНК длиной от 75 до 300 оснований, что важно для поддержания и укупоривания теломер. Было идентифицировано множество белков, связывающих одно- и двухцепочечную теломерную ДНК. [23] Они участвуют как в поддержании, так и в закрытии теломер. Теломеры образуют большие петлевые структуры, называемые теломерными петлями или Т-петлями. Здесь одноцепочечная ДНК закручивается в длинный круг, стабилизированный белками, связывающими теломеры . [24] В самом конце Т-петли одноцепочечная теломерная ДНК удерживается на участке двухцепочечной ДНК за счет того, что цепь теломер разрушает двухспиральную ДНК и спаривает основания с одной из двух цепей. Эта трехцепочечная структура называется петлей смещения или D-петлей. [25]
Помимо проблемы конечной репликации, исследования in vitro показали, что теломеры накапливают повреждения из-за окислительного стресса и что повреждение ДНК, опосредованное окислительным стрессом, оказывает большое влияние на укорочение теломер in vivo . Существует множество способов, которыми окислительный стресс, опосредованный активными формами кислорода (АФК), может привести к повреждению ДНК; однако пока неясно, вызвана ли повышенная скорость теломеров их присущей восприимчивостью или сниженной активностью систем репарации ДНК в этих регионах. [26] Несмотря на широкое согласие с выводами, были отмечены широко распространенные недостатки в измерениях и отборе проб; например, считается, что предполагаемая видовая и тканевая зависимость окислительного повреждения теломер недостаточно объяснена. [27] Популяционные исследования показали взаимосвязь между потреблением антиоксидантов и длиной теломер. В рамках проекта по изучению рака молочной железы на Лонг-Айленде (LIBCSP) авторы обнаружили умеренное увеличение риска рака молочной железы среди женщин с самыми короткими теломерами и более низким потреблением с пищей бета-каротина, витамина С или Е. [28] Эти результаты [29] позволяют предположить, что Риск рака из-за укорочения теломер может взаимодействовать с другими механизмами повреждения ДНК, в частности с окислительным стрессом.
Хотя теломеры укорачиваются в течение жизни особи, именно скорость укорочения теломер, а не длина теломер, связана с продолжительностью жизни вида. [30] Критически короткие теломеры вызывают реакцию повреждения ДНК и клеточное старение . [30] Мыши имеют гораздо более длинные теломеры, но скорость их укорочения значительно выше, а продолжительность жизни значительно сокращается по сравнению с людьми и слонами. [31]
Укорочение теломер связано со старением, смертностью и возрастными заболеваниями у экспериментальных животных. [6] [32] Хотя на продолжительность жизни человека могут влиять многие факторы, такие как курение, диета и физические упражнения, по мере того, как люди приближаются к верхнему пределу ожидаемой продолжительности жизни , более длинные теломеры могут быть связаны с продолжительностью жизни. [33]
Мета-анализ показал, что усиление воспринимаемого психологического стресса было связано с небольшим уменьшением длины теломер, но эти ассоциации ослабевают до отсутствия значимой связи при учете систематической ошибки публикации . В литературе, посвященной теломерам как интегративным биомаркерам воздействия стресса и невзгод, преобладают перекрестные и корреляционные исследования, что делает причинно-следственную интерпретацию проблематичной. [29] [34] В обзоре 2020 года утверждается, что связь между психосоциальным стрессом и длиной теломер оказывается наиболее сильной для стресса, испытанного в утробе матери или в раннем возрасте. [35]

Явление ограниченного клеточного деления было впервые обнаружено Леонардом Хейфликом и теперь называется пределом Хейфлика . [36] [37] Значительные открытия были впоследствии сделаны группой ученых, организованной в корпорации Geron основателем Geron Майклом Д. Уэстом , которые связали укорочение теломер с пределом Хейфлика. [38] Клонирование каталитического компонента теломеразы позволило провести эксперименты, чтобы проверить, способна ли экспрессия теломеразы на уровнях, достаточных для предотвращения укорочения теломер, к иммортализации клеток человека. В публикации в журнале Science 1998 года было продемонстрировано, что теломераза способна продлевать продолжительность жизни клеток, а теперь общепризнано, что она способна иммортализовать соматические клетки человека. [39]
Два исследования морских птиц -долгожителей показывают, что роль теломер далека от понимания. В 2003 году ученые заметили, что теломеры качурок Лича ( Oceanodroma leucorhoa ), по-видимому, удлиняются с возрастом, что стало первым наблюдаемым примером такого поведения теломер. [40]
Исследование показало, что длина теломер у разных видов млекопитающих коррелирует с продолжительностью жизни скорее обратно, чем напрямую, и пришло к выводу, что вклад длины теломер в продолжительность жизни остается спорным. [41] Существует мало доказательств того, что у людей длина теломер является важным биомаркером нормального старения в отношении важных когнитивных и физических способностей. [42]
Экспериментально проверенные и предсказанные мотивы последовательностей теломер более чем 9000 видов собраны в базе данных TeloBase, курируемой исследовательским сообществом. [43] Некоторые из экспериментально подтвержденных нуклеотидных последовательностей теломер также перечислены на веб-сайте базы данных теломеразы (буквенные обозначения см. в обозначении нуклеиновых кислот ).
Предварительные исследования показывают, что риск заболеваний при старении может быть связан с укорочением теломер, старением клеток или SASP ( секреторный фенотип, связанный со старением ). [30]
В настоящее время используется несколько методов для оценки средней длины теломер в эукариотических клетках. Одним из методов является саузерн-блоттинг терминального рестрикционного фрагмента (TRF). [47] [48] Существует веб-анализатор длины теломер (WALTER), программное обеспечение, обрабатывающее изображения TRF. [49] ПЦР в реальном времени для определения длины теломер включает определение соотношения теломер к однокопийному гену (T/S), которое, как показано, пропорционально средней длине теломер в клетке. [50]
Также были разработаны инструменты для оценки длины теломер на основе экспериментов по полногеномному секвенированию (WGS). Среди них TelSeq, [51] Telomerecat [52] и telomereHunter. [53] Оценка длины с помощью WGS обычно работает путем дифференцирования чтений секвенирования теломер, а затем определения длины теломер, которая произвела это количество чтений. Было показано, что эти методы коррелируют с ранее существовавшими методами оценки, такими как ПЦР и TRF. Flow-FISH используется для количественной оценки длины теломер в лейкоцитах человека. Полуавтоматический метод измерения средней длины теломер с помощью Flow FISH был опубликован в журнале Nature Protocols в 2006 году. [54]
Хотя многие компании предлагают услуги по измерению длины теломер, полезность этих измерений для широкого клинического или личного использования подвергается сомнению. [55] [56] Лауреат Нобелевской премии Элизабет Блэкберн , которая была соучредителем одной компании, пропагандировала клиническую полезность измерения длины теломер. [57]
В течение последних двух десятилетий экоэволюционные исследования изучали влияние особенностей жизненного цикла и условий окружающей среды на теломеры дикой природы. Большинство этих исследований было проведено на эндотермных животных , то есть на птицах и млекопитающих. Они предоставили доказательства наследования длины теломер; однако оценки наследственности сильно различаются внутри и между видами. [58] Возраст и длина теломер часто отрицательно коррелируют у позвоночных, но это снижение варьируется среди таксонов и связано с методом, используемым для оценки длины теломер. [59] Напротив, имеющаяся информация не показывает половых различий в длине теломер у позвоночных. [60] Особенности филогении и истории жизни, такие как размер тела или темп жизни, также могут влиять на динамику теломер. Например, он был описан у разных видов птиц и млекопитающих. [61] В 2019 году метаанализ подтвердил, что воздействие стрессоров (например, патогенной инфекции, конкуренции, репродуктивных усилий и высокого уровня активности) было связано с более короткими теломерами у различных таксонов животных. [62]
Исследования эктотермных животных и других организмов, не относящихся к млекопитающим, показывают, что не существует единой универсальной модели эрозии теломер; скорее, существуют большие различия в соответствующей динамике среди Metazoa , и даже внутри более мелких таксономических групп эти закономерности кажутся разнообразными. [63]