Температура – это физическая величина , количественно выражающая признак жары или холода. Температуру измеряют термометром . _ Он отражает среднюю кинетическую энергию колеблющихся и сталкивающихся атомов , составляющих вещество.
Термометры калибруются по различным температурным шкалам , которые исторически основывались на различных контрольных точках и термометрических веществах для определения. Наиболее распространенными шкалами являются шкала Цельсия с символом единицы измерения °C (ранее называвшаяся стоградусной ), шкала Фаренгейта (°F) и шкала Кельвина (K), причем последняя используется преимущественно в научных целях. Кельвин — одна из семи основных единиц Международной системы единиц (СИ).
Абсолютный ноль , то есть ноль Кельвина или -273,15 °C, является самой низкой точкой термодинамической температурной шкалы. Экспериментально к этому можно приблизиться очень близко, но на самом деле не достичь, как это признается в третьем законе термодинамики . Было бы невозможно извлечь энергию в виде тепла из тела при такой температуре.
Температура важна во всех областях естествознания , включая физику , химию , науку о Земле , астрономию , медицину , биологию , экологию , материаловедение , металлургию , машиностроение и географию , а также в большинстве аспектов повседневной жизни.
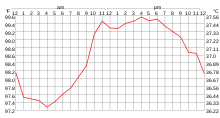
Многие физические процессы связаны с температурой; некоторые из них приведены ниже:
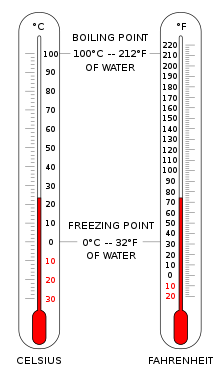
Для определения температурных шкал необходимы два значения: точка, выбранная за ноль градусов, и величина приращенной единицы температуры.
Шкала Цельсия (°C) используется для обычных измерений температуры в большинстве стран мира . Это эмпирическая шкала, сложившаяся исторически, которая привела к ее нулевой точке.0 °C определяется как точка замерзания воды , и100 °C — точка кипения воды, как при атмосферном давлении , так и на уровне моря. Ее назвали стоградусной шкалой из-за интервала в 100 градусов. [3] После стандартизации кельвина в Международной системе единиц он впоследствии был переопределен с точки зрения эквивалентных точек фиксации по шкале Кельвина, так что приращение температуры на один градус Цельсия равнозначно приращению на один градус Цельсия. Кельвина, хотя численно шкалы различаются точным смещением 273,15.
Шкала Фаренгейта широко используется в Соединенных Штатах . Вода замерзает при32 °F и кипит при212 ° F при атмосферном давлении на уровне моря.
При абсолютном нуле температуры никакая энергия не может быть отведена от материи в виде тепла, и этот факт выражен в третьем законе термодинамики . При этой температуре вещество не содержит макроскопической тепловой энергии, но все же имеет квантовомеханическую нулевую энергию , как предсказывает принцип неопределенности , хотя это не входит в определение абсолютной температуры. Экспериментально к абсолютному нулю можно приблизиться лишь очень близко; она никогда не может быть достигнута (самая низкая температура, достигнутая экспериментом, составляет 38 пК). [4] Теоретически в теле при температуре абсолютного нуля все классические движения его частиц прекращаются и они находятся в полном покое в этом классическом смысле. Абсолютный ноль, определяемый как0 K , в точности равно−273,15 °С , или−459,67 ° F.
Ссылаясь на константу Больцмана , на распределение Максвелла-Больцмана и на статистико-механическое определение энтропии Больцмана , в отличие от определения Гиббса, [ 5] для независимо движущихся микроскопических частиц, без учета межчастичной потенциальной энергии, по международному соглашению, температура Масштаб определяется и называется абсолютным, поскольку он не зависит от характеристик конкретных термометрических веществ и механизмов термометра . Кроме абсолютного нуля, у него нет эталонной температуры. Она известна как шкала Кельвина , широко используемая в науке и технике. Кельвин (название единицы пишется с маленькой буквы «к») — единица температуры в Международной системе единиц (СИ). Температура тела в состоянии термодинамического равновесия всегда положительна относительно абсолютного нуля.
Помимо международно признанной шкалы Кельвина, существует также термодинамическая температурная шкала , изобретенная лордом Кельвином , также с ее числовым нулем при абсолютном нуле температуры, но напрямую относящаяся к чисто макроскопическим термодинамическим концепциям, включая макроскопическую энтропию , хотя с микроскопической точки зрения ее можно отнести к Статистическое механическое определение Гиббса энтропии для канонического ансамбля , которое учитывает межчастичную потенциальную энергию, а также независимое движение частиц, так что оно может учитывать измерения температур, близких к абсолютному нулю. [5] Эта шкала имеет эталонную температуру в тройной точке воды, числовое значение которой определяется измерениями с использованием вышеупомянутой международно-согласованной шкалы Кельвина.
Во многих научных измерениях используется температурная шкала Кельвина (обозначение единицы измерения: К), названная в честь физика, который первым ее определил . Это абсолютная шкала. Его числовая нулевая точка,0 К – это абсолютный ноль температуры. С мая 2019 года кельвин определяется с помощью кинетической теории частиц и статистической механики. В Международной системе единиц (СИ) величина кельвина определяется с помощью постоянной Больцмана , значение которой определяется как установленное международным соглашением. [6] [7]
С мая 2019 года величина Кельвина определяется применительно к микроскопическим явлениям, характеризуемым с точки зрения статистической механики. Ранее, но с 1954 года, Международная система единиц определяла шкалу и единицу измерения кельвина как термодинамическую температуру , используя надежно воспроизводимую температуру тройной точки воды в качестве второй контрольной точки, причем первой контрольной точкой была0 К при абсолютном нуле. [ нужна цитата ]
Исторически температура тройной точки воды определялась как ровно 273,16 К. Сегодня это эмпирически измеряемая величина. Точка замерзания воды при атмосферном давлении на уровне моря происходит при температуре, очень близкой к273,15 К (0 °С ).
Существуют различные виды температурной шкалы. Возможно, будет удобно классифицировать их как эмпирически и теоретически обоснованные. Эмпирические температурные шкалы исторически старше, а теоретически обоснованные шкалы возникли в середине девятнадцатого века. [8] [9]
Эмпирически обоснованные температурные шкалы основаны непосредственно на измерениях простых макроскопических физических свойств материалов. Например, длина столбика ртути, заключенного в капиллярной трубке со стеклянными стенками, во многом зависит от температуры и является основой очень полезного ртутного термометра в стекле. Такие шкалы действительны только в удобных диапазонах температур. Например, при температуре выше точки кипения ртути ртутный стеклянный термометр непригоден. Большинство материалов расширяются при повышении температуры, но некоторые материалы, такие как вода, сжимаются при повышении температуры в определенном диапазоне, и тогда их вряд ли можно использовать в качестве термометрических материалов. Материал бесполезен в качестве термометра вблизи одной из температур фазового перехода, например, точки кипения.
Несмотря на эти ограничения, наиболее часто используемые на практике термометры относятся к эмпирическому типу. В частности, его использовали для калориметрии , что внесло большой вклад в открытие термодинамики. Тем не менее, эмпирическая термометрия имеет серьезные недостатки, если рассматривать ее как основу теоретической физики. Термометры, основанные на эмпирическом опыте, помимо простых прямых измерений обычных физических свойств термометрических материалов, могут быть перекалиброваны с использованием теоретических физических рассуждений, и это может расширить диапазон их адекватности.
Теоретически обоснованные температурные шкалы основаны непосредственно на теоретических аргументах, особенно на аргументах кинетической теории и термодинамики. Они более или менее идеально реализованы в практически осуществимых физических устройствах и материалах. Теоретически обоснованные температурные шкалы используются в качестве калибровочных стандартов для практических термометров, основанных на эмпирическом опыте.
В физике принятая на международном уровне общепринятая шкала температур называется шкалой Кельвина. Он калибруется по согласованному на международном уровне и предписанному значению постоянной Больцмана, [6] [7] относящейся к движению микроскопических частиц, таких как атомы, молекулы и электроны, входящих в состав тела, температуру которого необходимо измерить. В отличие от термодинамической температурной шкалы, изобретенной Кельвином, общепринятая в настоящее время температура Кельвина не определяется ни путем сравнения с температурой эталонного состояния стандартного тела, ни с точки зрения макроскопической термодинамики.
Помимо абсолютного нуля температуры, температура Кельвина тела в состоянии внутреннего термодинамического равновесия определяется измерениями подходящим образом выбранных его физических свойств, которые имеют точное известное теоретическое объяснение в терминах постоянной Больцмана . [ нужна цитата ] Эта константа относится к выбранным видам движения микроскопических частиц в составе тела. При таких видах движения частицы движутся индивидуально, без взаимного взаимодействия. Такие движения обычно прерываются столкновениями между частицами, но для измерения температуры движения выбираются так, чтобы между столкновениями неинтерактивные участки их траекторий были известны как доступные для точного измерения. При этом межчастичная потенциальная энергия не учитывается.
В идеальном газе и других теоретически понятных телах температура Кельвина определяется как пропорциональная средней кинетической энергии неинтерактивно движущихся микроскопических частиц, которую можно измерить подходящими методами. Константа пропорциональности представляет собой простое кратное константе Больцмана. Если молекулы, атомы или электроны [10] [11] испускаются из материала и измеряются их скорости, спектр их скоростей часто почти подчиняется теоретическому закону, называемому распределением Максвелла-Больцмана , который дает хорошо обоснованное измерение температуры, для которых действует закон. [12] Пока еще не было успешных экспериментов такого рода, которые напрямую использовали бы распределение Ферми-Дирака для термометрии, но, возможно, это будет достигнуто в будущем. [13]
Скорость звука в газе теоретически можно рассчитать, исходя из молекулярного характера газа, его температуры и давления, а также значения постоянной Больцмана. Для газа с известным молекулярным характером и давлением это обеспечивает связь между температурой и постоянной Больцмана. Эти величины могут быть известны или измерены более точно, чем термодинамические переменные, определяющие состояние образца воды в его тройной точке. Следовательно, принимая значение постоянной Больцмана в качестве первоначально определенного эталона точно определенного значения, измерение скорости звука может обеспечить более точное измерение температуры газа. [14]
Измерение спектра электромагнитного излучения идеального трехмерного черного тела может обеспечить точное измерение температуры, поскольку частота максимальной спектральной яркости излучения черного тела прямо пропорциональна температуре черного тела; это известно как закон смещения Вина и имеет теоретическое объяснение в законе Планка и законе Бозе-Эйнштейна .
Измерение спектра мощности шума, создаваемого электрическим резистором, также может обеспечить точное измерение температуры. Резистор имеет две клеммы и по сути представляет собой одномерное тело. Закон Бозе-Эйнштейна для этого случая показывает, что мощность шума прямо пропорциональна температуре резистора, значению его сопротивления и ширине полосы шума. В данной полосе частот мощность шума имеет равные вклады от каждой частоты и называется шумом Джонсона . Если известно значение сопротивления, то можно найти температуру. [15] [16]
Исторически сложилось так, что до мая 2019 года определение шкалы Кельвина было изобретенным Кельвином и основанным на соотношении количеств энергии в процессах в идеальном двигателе Карно, полностью с точки зрения макроскопической термодинамики. [ нужна цитата ] Этот двигатель Карно должен был работать между двумя температурами: температурой тела, температуру которого нужно было измерить, и эталонной температурой тела с температурой тройной точки воды. Затем эталонная температура тройной точки была определена как точно равная273,16 К. С мая 2019 года это значение не зафиксировано по определению, но должно измеряться с помощью микроскопических явлений, включающих константу Больцмана, как описано выше. Микроскопическое статистическое механическое определение не имеет эталонной температуры.
Материалом, на котором может быть основана макроскопически определенная температурная шкала, является идеальный газ . Давление, оказываемое фиксированным объемом и массой идеального газа, прямо пропорционально его температуре. Некоторые природные газы демонстрируют настолько почти идеальные свойства в подходящем диапазоне температур, что их можно использовать для термометрии; это было важно во время развития термодинамики и имеет практическое значение до сих пор. [17] [18] Однако идеальный газовый термометр теоретически не идеален для термодинамики. Это связано с тем, что энтропия идеального газа при абсолютном нуле температуры не является положительной полуопределенной величиной, что ставит газ в нарушение третьего закона термодинамики. В отличие от реальных материалов, идеальный газ не сжижается и не затвердевает, каким бы холодным он ни был. Альтернативное мышление, закон идеального газа, относится к пределу бесконечно высокой температуры и нулевого давления; эти условия гарантируют невзаимодействующие движения составляющих молекул. [19] [20] [21]
Величина кельвина теперь определяется с точки зрения кинетической теории, полученной из значения постоянной Больцмана .
Кинетическая теория обеспечивает микроскопическое объяснение температуры некоторых тел материала, особенно газов, на основе того, что макроскопические системы состоят из множества микроскопических частиц, таких как молекулы и ионы различных видов, причем все частицы одного вида одинаковы. Он объясняет макроскопические явления посредством классической механики микроскопических частиц. Теорема о равнораспределении кинетической теории утверждает, что каждая классическая степень свободы свободно движущейся частицы имеет среднюю кинетическую энергию k B T /2 , где k B обозначает постоянную Больцмана . [ нужна цитата ] Поступательное движение частицы имеет три степени свободы, так что, за исключением очень низких температур, когда преобладают квантовые эффекты, средняя поступательная кинетическая энергия свободно движущейся частицы в системе с температурой T будет равна 3 k B. Т /2 .
Молекулы, такие как кислород (O 2 ), имеют больше степеней свободы , чем отдельные сферические атомы: они совершают вращательные и колебательные движения, а также поступательные движения. Нагревание приводит к повышению температуры из-за увеличения средней поступательной кинетической энергии молекул. Нагревание также приведет к увеличению энергии, связанной с колебательными и вращательными режимами, за счет равнораспределения . Таким образом, двухатомному газу потребуется больше затрат энергии для повышения его температуры на определенную величину, т. е. он будет иметь большую теплоемкость , чем одноатомный газ.
Как отмечалось выше, скорость звука в газе можно рассчитать, исходя из молекулярного характера газа, его температуры и давления, а также значения постоянной Больцмана. Принимая значение постоянной Больцмана в качестве первоначально определенного эталона точно определенного значения, измерение скорости звука может обеспечить более точное измерение температуры газа. [14]
Можно измерить среднюю кинетическую энергию составляющих микроскопических частиц, если им позволить выйти из объема системы через небольшое отверстие в содержащей стенке. Необходимо измерить спектр скоростей и на его основе рассчитать среднее значение. Это не обязательно тот случай, когда частицы, которые улетают и измеряются, имеют такое же распределение скоростей, как и частицы, которые остаются в объеме системы, но иногда возможен хороший образец.
Температура — одна из основных величин в изучении термодинамики . Раньше величина Кельвина определялась в терминах термодинамики, но в настоящее время, как упоминалось выше, она определяется в терминах кинетической теории.
Термодинамическую температуру называют абсолютной по двум причинам. Во-первых, его формальный характер не зависит от свойств конкретных материалов. Другая причина заключается в том, что его ноль в некотором смысле является абсолютным, поскольку он указывает на отсутствие микроскопического классического движения составляющих частиц материи, так что они имеют предельную нулевую удельную теплоемкость при нулевой температуре в соответствии с третьим законом. термодинамики. Тем не менее термодинамическая температура действительно имеет определенное числовое значение, произвольно выбранное по традиции и зависящее от свойств конкретных материалов; это просто менее произвольно, чем относительные шкалы «градусов», такие как Цельсия и Фаренгейта . Поскольку это абсолютная шкала с одной фиксированной точкой (нулем), для произвольного выбора остается только одна степень свободы, а не две, как в относительных шкалах. Для шкалы Кельвина с мая 2019 года международной конвенцией был сделан выбор в пользу использования знаний о режимах работы различных термометрических устройств, опирающихся на микроскопические кинетические теории молекулярного движения. Числовая шкала определяется традиционным определением значения постоянной Больцмана , которая связывает макроскопическую температуру со средней микроскопической кинетической энергией частиц, таких как молекулы. Его числовое значение произвольно, и существует альтернативная, менее широко используемая шкала абсолютных температур, называемая шкалой Ренкина , которая согласована со шкалой Фаренгейта, как Кельвин со шкалой Цельсия.
Термодинамическое определение температуры принадлежит Кельвину. Он создан в виде идеализированного устройства, называемого двигателем Карно , который, как предполагается, работает в воображаемом непрерывном цикле последовательных процессов , которые пересекают цикл состояний его рабочего тела. Двигатель забирает некоторое количество тепла Q 1 из горячего резервуара и отдает меньшее количество отходящего тепла Q 2 < 0 в холодный резервуар. Чистая тепловая энергия, поглощенная рабочим телом, передается в виде термодинамической работы в рабочий резервуар и считается мощностью двигателя. Предполагается, что цикл протекает настолько медленно, что в каждой точке цикла рабочее тело находится в состоянии термодинамического равновесия. Таким образом, предполагается, что последовательные процессы цикла протекают обратимо, без производства энтропии . Тогда количество энтропии, поступившей из горячего резервуара при нагреве рабочего тела, будет равно количеству энтропии, переданной в холодный резервуар при охлаждении рабочего тела. Затем определяются абсолютные или термодинамические температуры резервуаров T 1 и T 2 так, что [22]
Нулевой закон термодинамики позволяет использовать это определение для измерения абсолютной или термодинамической температуры произвольного интересующего тела, заставляя другой резервуар тепла иметь ту же температуру, что и интересующее тело.
Оригинальная работа Кельвина, постулирующая абсолютную температуру, была опубликована в 1848 году. Она была основана на работе Карно до формулировки первого закона термодинамики. У Карно не было ни четкого понимания тепла, ни конкретного понятия энтропии. Он написал о «калориях» и сказал, что все теплоты, прошедшие из горячего резервуара, перешли в холодный резервуар. Кельвин писал в своей статье 1848 года, что его шкала была абсолютной в том смысле, что она определялась «независимо от свойств какого-либо конкретного вида материи». Его окончательная публикация, в которой изложено только что изложенное определение, была напечатана в 1853 году, а статья прочитана в 1851 году. [23] [24] [25] [26]
Численные детали раньше определялись путем создания одного из резервуаров тепла в виде ячейки в тройной точке воды, абсолютная температура которой была определена как 273,16 К. [27] В настоящее время числовое значение вместо этого получается путем измерения с помощью микроскопического статистического метода. механическое международное определение, как указано выше.
С термодинамической точки зрения температура является интенсивной переменной , поскольку она равна дифференциальному коэффициенту одной экстенсивной переменной по отношению к другой для данного тела. Таким образом , он имеет размеры отношения двух экстенсивных переменных. В термодинамике два тела часто рассматривают как соединенные контактом с общей стенкой, обладающей некоторыми специфическими проницаемыми свойствами. Такую удельную проницаемость можно отнести к определенной интенсивной переменной. Примером может служить диатермическая стена, проницаемая только для тепла; интенсивной переменной в этом случае является температура. Когда два тела были соединены через специально проницаемую стенку в течение очень долгого времени и достигли постоянного устойчивого состояния, соответствующие интенсивные переменные равны в двух телах; для диатермической стенки это утверждение иногда называют нулевым законом термодинамики. [28] [29] [30]
В частности, когда тело описывается путем указания его внутренней энергии U , экстенсивной переменной, как функции его энтропии S , также экстенсивной переменной, и других переменных состояния V , N , с U = U ( S , V , N ), то температура равна частной производной внутренней энергии по энтропии: [29] [30] [31]
Аналогично, когда тело описывается путем указания его энтропии S как функции его внутренней энергии U и других переменных состояния V , N с S = S ( U , V , N ) , тогда обратная величина температуры равна частная производная энтропии по внутренней энергии: [29] [31] [32]
Приведенное выше определение абсолютной температуры, уравнение (1), дано Кельвину. Оно относится к системам, закрытым для переноса вещества, и уделяет особое внимание непосредственно экспериментальным процедурам. Изложение термодинамики Гиббсом начинается на более абстрактном уровне и касается систем, открытых для переноса материи; в этом развитии термодинамики приведенные выше уравнения (2) и (3) фактически являются альтернативными определениями температуры. [33]
Реальные тела часто не находятся в термодинамическом равновесии и не однородны. Для исследования методами классической необратимой термодинамики тело обычно концептуально разделяют в пространстве и времени на «ячейки» небольшого размера. Если в такой «ячейке» с хорошим приближением выполняются классические условия термодинамического равновесия вещества, то она однородна и для нее существует температура. Если это так для каждой «клетки» тела, то говорят, что локальное термодинамическое равновесие преобладает во всем теле. [34] [35] [36] [37] [38]
Имеет смысл, например, сказать об экстенсивной переменной U или об экстенсивной переменной S , что она имеет плотность на единицу объема или количество на единицу массы системы, но бессмысленно говорить об экстенсивной переменной S . плотность температуры на единицу объема или количество температуры на единицу массы системы. С другой стороны, нет смысла говорить о внутренней энергии в точке, а при преобладании локального термодинамического равновесия имеет смысл говорить о температуре в точке. Следовательно, температура может меняться от точки к точке в среде, не находящейся в глобальном термодинамическом равновесии, но в которой существует локальное термодинамическое равновесие.
Таким образом, когда в теле преобладает локальное термодинамическое равновесие, температуру можно рассматривать как пространственно изменяющееся локальное свойство этого тела, поскольку температура является интенсивной переменной.
Температура является мерой качества состояния материала. [39] Качество можно рассматривать как более абстрактную сущность, чем любая конкретная температурная шкала, которая его измеряет, и некоторые авторы называют его жаром . [40] [41] [42] Качество жары относится к состоянию материала только в определенной местности, и вообще, за исключением тел, находящихся в устойчивом состоянии термодинамического равновесия, жара варьируется от места к месту. Это не обязательно тот случай, когда материал в определенном месте находится в устойчивом и почти однородном состоянии, позволяющем ему иметь четко определенную температуру или температуру. Теплоту можно абстрактно представить как одномерное многообразие . Каждая действующая температурная шкала имеет свою собственную карту в многообразии температуры. [43] [44]
Когда две системы, находящиеся в тепловом контакте, имеют одинаковую температуру, теплообмен между ними отсутствует. Когда существует разница температур, тепло самопроизвольно перетекает от более теплой системы к более холодной, пока они не придут в тепловое равновесие . Такая передача тепла происходит за счет проводимости или теплового излучения. [45] [46] [47] [ 48] [49] [50] [51] [52]
Физики-экспериментаторы, например Галилей и Ньютон , [53] обнаружили, что существует бесконечно много эмпирических температурных шкал . Тем не менее, нулевой закон термодинамики гласит, что все они измеряют одно и то же качество. Это значит, что для тела, находящегося в состоянии внутреннего термодинамического равновесия, всякий правильно откалиброванный термометр любого типа, измеряющий температуру тела, регистрирует одну и ту же температуру. Для тела, не находящегося в собственном состоянии внутреннего термодинамического равновесия, разные термометры могут регистрировать разные температуры в зависимости соответственно от механизмов действия термометров.
Для экспериментальной физики тепло означает, что при сравнении любых двух данных тел в их соответствующих отдельных термодинамических состояниях любые два эмпирических термометра с показаниями числовой шкалы согласуются относительно того, какое из двух данных тел более горячее, или что они имеют та же температура. [54] Это не требует, чтобы два термометра имели линейную зависимость между показаниями их числовых шкал, но требует, чтобы связь между их числовыми показаниями была строго монотонной . [55] [56] Определенное ощущение большей температуры можно получить, независимо от калориметрии , термодинамики и свойств конкретных материалов, из закона смещения Вина теплового излучения : температура ванны теплового излучения пропорциональна универсальная константа, равная частоте максимума ее частотного спектра ; эта частота всегда положительна, но может иметь значения, стремящиеся к нулю . Тепловое излучение первоначально определяется для полости, находящейся в термодинамическом равновесии. Эти физические факты оправдывают математическое утверждение о том, что тепло существует в упорядоченном одномерном многообразии . Это фундаментальный признак температуры и термометров для тел, находящихся в собственном термодинамическом равновесии. [8] [43] [44] [57] [58]
За исключением системы, претерпевающей фазовый переход первого порядка , такой как таяние льда, поскольку замкнутая система получает тепло, без изменения ее объема и без изменения действующих на нее внешних силовых полей ее температура повышается. Для системы, претерпевающей такой фазовый переход настолько медленно, что отклонением от термодинамического равновесия можно пренебречь, ее температура остается постоянной, поскольку в систему поступает скрытое тепло . И наоборот, потеря тепла из закрытой системы без фазового перехода, без изменения объема и без изменения внешних силовых полей, действующих на нее, снижает ее температуру. [59]
В то время как для тел, находящихся в их собственных состояниях термодинамического равновесия, понятие температуры требует, чтобы все эмпирические термометры соглашались относительно того, какое из двух тел горячее или что они имеют одинаковую температуру, это требование небезопасно для тел, находящихся в устойчивом состоянии. состояния, хотя и не находящиеся в термодинамическом равновесии. Тогда вполне может быть, что разные эмпирические термометры расходятся во мнениях относительно того, какой из них горячее, и если это так, то по крайней мере одно из тел не имеет четко определенной абсолютной термодинамической температуры. Тем не менее, любое данное тело и любой подходящий эмпирический термометр все же могут поддерживать понятия эмпирической, неабсолютной теплоты и температуры для подходящего диапазона процессов. Это предмет изучения неравновесной термодинамики . [ нужна цитата ]
Когда тело не находится в устойчивом состоянии, понятие температуры становится еще менее безопасным, чем для тела, находящегося в устойчивом состоянии и не находящегося в термодинамическом равновесии. Это также является предметом изучения неравновесной термодинамики .
Для аксиоматической трактовки термодинамического равновесия с 1930-х годов стало принято ссылаться на нулевой закон термодинамики . Обычно формулируемая минималистская версия такого закона постулирует только то, что все тела, которые при термическом соединении находились бы в тепловом равновесии, должны иметь одинаковую температуру по определению, но сама по себе не устанавливает температуру как величину, выраженную как действительная величина. число на шкале. Более физически информативная версия такого закона рассматривает эмпирическую температуру как диаграмму на многообразии температуры. [43] [58] [60] В то время как нулевой закон допускает определения многих различных эмпирических шкал температуры, второй закон термодинамики выбирает определение одной предпочтительной абсолютной температуры , уникальной с точностью до произвольного масштабного коэффициента, откуда она называется термодинамическая температура . [8] [43] [61] [62] [63] [64] Если внутреннюю энергию рассматривать как функцию объема и энтропии однородной системы, находящейся в термодинамическом равновесии, термодинамическая абсолютная температура появляется как частная производная внутренней энергии. относительно энтропии при постоянном объеме. Его естественным, внутренним источником или нулевой точкой является абсолютный ноль , при котором энтропия любой системы минимальна. Хотя это самая низкая абсолютная температура, описываемая моделью, третий закон термодинамики постулирует, что абсолютный ноль не может быть достигнут ни одной физической системой.
Когда передача энергии к телу или от него осуществляется только в виде тепла, состояние тела меняется. В зависимости от окружающей среды и стен, отделяющих их от тела, в организме возможны различные изменения. Они включают химические реакции, повышение давления, повышение температуры и фазовый переход. Для каждого вида изменения при определенных условиях теплоемкость представляет собой отношение количества переданного тепла к величине изменения. [65]
Например, если изменение представляет собой повышение температуры при постоянном объеме, без фазового перехода и химического изменения, то температура тела повышается и его давление увеличивается. Количество переданного тепла Δ Q , разделенное на наблюдаемое изменение температуры Δ T , представляет собой теплоемкость тела при постоянном объеме:
Если теплоемкость измеряется для четко определенного количества вещества , удельная теплота является мерой тепла, необходимого для увеличения температуры такой единицы количества на одну единицу температуры. Например, для повышения температуры воды на один кельвин (равный одному градусу Цельсия) требуется 4186 джоулей на килограмм (Дж/кг).

Измерение температуры с использованием современных научных термометров и температурных шкал восходит, по крайней мере, к началу 18 века, когда Даниэль Габриэль Фаренгейт адаптировал термометр (переход на ртуть ) и шкалу, разработанные Оле Кристенсеном Рёмером . Шкала Фаренгейта до сих пор используется в США в ненаучных целях.
Температуру измеряют термометрами , которые можно калибровать по различным температурным шкалам . В большинстве стран мира (за исключением Белиза , Мьянмы , Либерии и США ) шкала Цельсия используется для большинства целей измерения температуры. Большинство ученых измеряют температуру по шкале Цельсия, а термодинамическую температуру - по шкале Кельвина , которая представляет собой смещение шкалы Цельсия так, что ее нулевая точка равна0 К =−273,15 °C , или абсолютный ноль . Многие инженерные области в США, особенно высокие технологии и федеральные спецификации США (гражданские и военные), также используют шкалы Кельвина и Цельсия. Другие инженерные области в США также полагаются на шкалу Рэнкина (сдвинутая шкала Фаренгейта) при работе в термодинамических дисциплинах, таких как горение .
Основной единицей температуры в Международной системе единиц (СИ) является кельвин . Имеет символ К.
Для повседневных применений часто удобно использовать шкалу Цельсия, в которой0 °C очень близко соответствует температуре замерзания воды и100 °C — это температура кипения на уровне моря. Поскольку капли жидкости обычно существуют в облаках при минусовых температурах,0 °C лучше определить как точку плавления льда. В этой шкале разница температур в 1 градус Цельсия равна приращению в 1 Кельвин , но масштаб компенсируется температурой, при которой тает лед (273,15 К ).
По международному соглашению [66] до мая 2019 года шкалы Кельвина и Цельсия определялись двумя точками фиксации: абсолютным нулем и тройной точкой Венского стандарта средней океанской воды , которая представляет собой воду, специально приготовленную с определенной смесью изотопов водорода и кислорода. . Абсолютный ноль определялся как точно0 К и−273,15 °С . Это температура, при которой все классические поступательные движения частиц, составляющих материю, прекращаются и они находятся в полном покое в классической модели. Однако с квантовой точки зрения движение нулевой точки сохраняется и имеет связанную с ней энергию, энергию нулевой точки . Материя находится в своем основном состоянии [67] и не содержит тепловой энергии . Температура273,16 К и0,01 °C были определены как значения тройной точки воды. Это определение преследовало следующие цели: оно фиксировало величину кельвина как равную ровно 1 части из 273,16 частей разницы между абсолютным нулем и тройной точкой воды; установило, что один кельвин имеет точно такую же величину, как один градус по шкале Цельсия; и установило, что разница между нулевыми точками этих шкал равна273,15 К (0 К =−273,15 °С и273,16 К =0,01 °С ). С 2019 года появилось новое определение, основанное на постоянной Больцмана [68] , но масштабы практически не изменились.
В США наиболее широко используется шкала Фаренгейта. В этом масштабе температура замерзания воды соответствует32 °F и точка кипения до212 °Ф . Шкала Ренкина, до сих пор используемая в области химического машиностроения в США, представляет собой абсолютную шкалу, основанную на приращении по Фаренгейту.
Следующие температурные шкалы используются или исторически использовались для измерения температуры:
Область физики плазмы занимается явлениями электромагнитной природы, связанными с очень высокими температурами. Принято выражать температуру как энергию в единицах, связанных с электронвольтом или килоэлектронвольтом ( эВ / кВ или кэВ/ кВ ) . Соответствующая энергия, которая по размерам отличается от температуры, затем рассчитывается как произведение постоянной Больцмана и температуры . Тогда 1 эВ/ к B будет 11 605 К . При изучении вещества КХД обычно встречаются температуры порядка нескольких сотен МэВ/ кВ , что эквивалентно примерно10 12 К .
Когда измеряют изменение температуры в определенной области пространства или времени, оказываются ли измерения температуры непрерывными или дискретными? Существует широко распространенное заблуждение, что такие измерения температуры всегда должны быть непрерывными. [69] Это заблуждение частично происходит из исторической точки зрения, связанной с непрерывностью классических физических величин , которая утверждает, что физические величины должны принимать каждое промежуточное значение между начальным значением и конечным значением. [69] [70] Однако классическая картина верна только в тех случаях, когда температура измеряется в системе, находящейся в равновесии , то есть вне этих условий температура не может быть непрерывной. [69] Для систем, находящихся вне равновесия, например, на границах раздела материалов (например, граница раздела металл/неметалл или граница раздела жидкость-пар), измерения температуры могут показывать резкие разрывы во времени и пространстве. [69] Например, Фанг и Уорд были одними из первых авторов, которые успешно сообщили о скачках температуры до 7,8 К на поверхности испаряющихся капель воды. [71] Об этом сообщалось в межмолекулярных масштабах или в масштабе длины свободного пробега молекул, которая обычно составляет порядка нескольких микрометров в газах [72] при комнатной температуре. Вообще говоря, в случаях межфазной теплопередачи скачки температуры считаются нормой, а не исключением. [73] Это происходит из-за резкого изменения вибрационных или тепловых свойств материалов на таких границах раздела, которые предотвращают мгновенную передачу тепла и установление теплового равновесия (предпосылка для наличия однородной равновесной температуры на границе раздела). [74] [75] Кроме того, измерения температуры в макромасштабе (типичный масштаб наблюдений) могут быть слишком грубыми, поскольку они усредняют микроскопическую тепловую информацию на основе масштаба репрезентативного объема выборки системы управления и, таким образом, вполне вероятно, что при таких средних значениях температурные скачки на микромасштабе могут быть упущены из виду. [69] Такое усреднение может даже давать неправильные или вводящие в заблуждение результаты во многих случаях измерения температуры, даже на макромасштабе, и поэтому разумно тщательно изучить микрофизическую информацию, прежде чем усреднять или сглаживать любые потенциальные температурные скачки. в системе как таковой такие разрывы не всегда могут быть усреднены или сглажены. [69] [76]Температурные неравномерности, а не просто аномалии, на самом деле существенно улучшили наше понимание и возможности прогнозирования, касающиеся теплопередачи в малых масштабах. [69] [73] [74] [75] [76]
Исторически сложилось так, что существует несколько научных подходов к объяснению температуры: классическое термодинамическое описание, основанное на макроскопических эмпирических переменных, которые можно измерить в лаборатории; кинетическая теория газов , связывающая макроскопическое описание с вероятностным распределением энергии движения частиц газа; и микроскопическое объяснение, основанное на статистической физике и квантовой механике . Кроме того, строгие и чисто математические подходы обеспечили аксиоматический подход к классической термодинамике и температуре. [77] Статистическая физика обеспечивает более глубокое понимание, описывая атомное поведение материи и выводит макроскопические свойства из статистических средних микроскопических состояний, включая как классические, так и квантовые состояния. В фундаментальном физическом описании температура может быть измерена непосредственно в единицах энергии. Однако в практических системах измерения науки, техники и торговли, таких как современная метрическая система единиц, макроскопические и микроскопические описания взаимосвязаны константой Больцмана , коэффициентом пропорциональности, который масштабирует температуру до микроскопической средней кинетической энергии. .
Микроскопическое описание в статистической механике основано на модели, которая анализирует систему на ее фундаментальные частицы материи или на набор классических или квантово-механических осцилляторов и рассматривает систему как статистический ансамбль микросостояний . Как совокупность классических материальных частиц, температура является мерой средней энергии движения, называемой поступательной кинетической энергией частиц, будь то в твердых телах, жидкостях, газах или плазме. Кинетическая энергия, концепция классической механики , равна половине массы частицы, умноженной на квадрат ее скорости . В этой механической интерпретации теплового движения кинетическая энергия материальных частиц может заключаться в скорости частиц их поступательного или колебательного движения или в инерции их вращательных мод. В одноатомных совершенных газах и, примерно, в большинстве газов и в простых металлах, температура является мерой средней поступательной кинетической энергии частицы, 3/2 k B T . Он также определяет функцию распределения вероятностей энергии. В конденсированном состоянии, и особенно в твердых телах, это чисто механическое описание часто менее полезно, и модель осциллятора обеспечивает лучшее описание для объяснения квантово-механических явлений. Температура определяет статистическую заселенность микросостояний ансамбля. Микроскопическое определение температуры имеет смысл только в термодинамическом пределе , то есть для больших ансамблей состояний или частиц, чтобы соответствовать требованиям статистической модели.
Кинетическая энергия также рассматривается как составная часть тепловой энергии . Тепловую энергию можно разделить на независимые компоненты, связанные со степенями свободы частиц или режимами осцилляторов в термодинамической системе . Вообще число этих степеней свободы, доступных для экраспределения энергии , зависит от температуры, т. е. от энергетической области рассматриваемых взаимодействий. Для твердых тел тепловая энергия связана прежде всего с колебаниями его атомов или молекул около положения равновесия. В идеальном одноатомном газе кинетическая энергия обнаруживается исключительно в чисто поступательном движении частиц. В других системах вибрационные и вращательные движения также вносят степени свободы.
Максвелл и Больцман разработали кинетическую теорию , которая дает фундаментальное понимание температуры в газах. [78] Эта теория также объясняет закон идеального газа и наблюдаемую теплоемкость одноатомных (или «благородных» ) газов. [79] [80] [81]
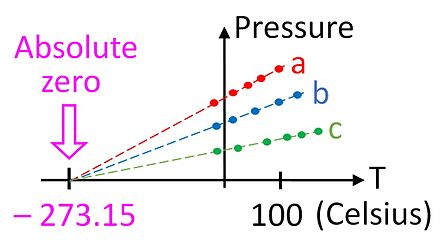
Закон идеального газа основан на наблюдаемых эмпирических отношениях между давлением ( p ), объемом ( V ) и температурой ( T ) и был признан задолго до того, как была разработана кинетическая теория газов (см. законы Бойля и Чарльза ). Закон идеального газа гласит: [82]
где n — количество молей газа, а R = 8,314 462 618 ... Дж⋅моль −1 ⋅K −1 [83] — газовая постоянная .
Это соотношение дает нам первый намек на то, что на шкале температур существует абсолютный ноль , потому что он справедлив только в том случае, если температура измеряется по абсолютной шкале, такой как шкала Кельвина. Закон идеального газа позволяет измерять температуру в этой абсолютной шкале с помощью газового термометра . Температуру в кельвинах можно определить как давление в паскалях одного моля газа в сосуде объемом один кубический метр, разделенное на газовую постоянную.
Хотя это не особенно удобное устройство, газовый термометр обеспечивает важную теоретическую основу, с помощью которой можно калибровать все термометры. На практике невозможно использовать газовый термометр для измерения абсолютной нулевой температуры, поскольку газы конденсируются в жидкость задолго до того, как температура достигнет нуля. Однако можно экстраполировать до абсолютного нуля, используя закон идеального газа, как показано на рисунке.
Кинетическая теория предполагает, что давление вызвано силой, связанной с ударами отдельных атомов о стенки, и что вся энергия представляет собой поступательную кинетическую энергию . Используя сложный аргумент симметрии, [84] Больцман вывел то, что сейчас называется функцией распределения вероятностей Максвелла-Больцмана для скорости частиц в идеальном газе. Из этой функции распределения вероятностей средняя кинетическая энергия (на частицу) одноатомного идеального газа равна [80] [85]
где постоянная Больцмана k B — постоянная идеального газа, деленная на число Авогадро , и — среднеквадратическая скорость . [86] Эта прямая пропорциональность между температурой и средней молекулярной кинетической энергией является частным случаем теоремы о равнораспределении и справедлива только в классическом пределе идеального газа . Это не справедливо для большинства веществ.
Когда два иначе изолированных тела соединены вместе жестким физическим путем, непроницаемым для материи, происходит спонтанная передача энергии в виде тепла от более горячего к более холодному из них. В конце концов, они достигают состояния взаимного теплового равновесия , в котором теплопередача прекращается, а соответствующие переменные состояния тел становятся неизменными. [87] [88] [89]
Одно из утверждений нулевого закона термодинамики заключается в том, что если каждая из двух систем находится в тепловом равновесии с третьей системой, то они также находятся в тепловом равновесии друг с другом. [90] [91] [92]
Это утверждение помогает определить температуру, но само по себе оно не завершает определение. Эмпирическая температура — это числовая шкала температуры термодинамической системы. Такую теплоту можно определить как существующую в одномерном многообразии , простирающемся между горячим и холодным. Иногда утверждается, что нулевой закон включает существование уникального универсального многообразия температуры и числовых шкал на нем, чтобы обеспечить полное определение эмпирической температуры. [60] Чтобы быть пригодным для эмпирической термометрии, материал должен иметь монотонную связь между теплотой и некоторой легко измеряемой переменной состояния, такой как давление или объем, когда все другие соответствующие координаты фиксированы. Исключительно подходящей системой является идеальный газ , который может обеспечить шкалу температур, соответствующую абсолютной шкале Кельвина. Шкала Кельвина определяется на основе второго закона термодинамики.
В качестве альтернативы рассмотрению или определению нулевого закона термодинамики историческим развитием термодинамики было определение температуры в терминах второго закона термодинамики , который касается энтропии . [ нужна цитата ] Второй закон гласит, что любой процесс приведет либо к отсутствию изменений, либо к чистому увеличению энтропии Вселенной. Это можно понять с точки зрения вероятности.
Например, в серии подбрасываний монеты идеально упорядоченной системой будет та, в которой либо при каждом подбрасывании выпадает орел, либо при каждом подбрасывании выпадает решка. Это означает, что результат всегда на 100% один и тот же. Напротив, возможны многие смешанные ( неупорядоченные ) исходы, и их количество увеличивается с каждым броском. В конце концов, комбинации ~50% орла и ~50% решки доминируют, и получение результата, значительно отличающегося от 50/50, становится все более маловероятным. Таким образом, система естественным образом переходит в состояние максимального беспорядка или энтропии.
Поскольку температура управляет передачей тепла между двумя системами, а Вселенная стремится к максимуму энтропии, ожидается, что существует некоторая связь между температурой и энтропией. Тепловая машина – это устройство для преобразования тепловой энергии в механическую, в результате чего совершается работа. Анализ тепловой машины Карно дает необходимые соотношения. Согласно закону сохранения энергии, поскольку энергия является функцией состояния , которая не изменяется в течение полного цикла, работа тепловой машины за полный цикл равна чистой теплоте, т. е. сумме тепла, переданной в систему при высокой температуре, q H > 0, а отходящее тепло, выделяемое при низкой температуре, q C < 0. [93]
КПД равен работе, деленной на погонную теплоту:
где w cy — работа, совершаемая за цикл. Эффективность зависит только от | q C |/ q ЧАС . Поскольку q C и q H соответствуют теплообмену при температурах TC и TH соответственно , | q C |/ q H должно быть некоторой функцией этих температур:
Теорема Карно утверждает, что все обратимые двигатели, работающие с одними и теми же тепловыми резервуарами, одинаково эффективны. [ нужна цитата ] Таким образом, тепловой двигатель, работающий между T 1 и T 3 , должен иметь тот же КПД, что и двигатель, состоящий из двух циклов, один между T 1 и T 2 , а второй между T 2 и T 3 . Это может быть только в том случае, если
что подразумевает
Поскольку первая функция не зависит от T 2 , эта температура должна сокращаться в правой части, что означает, что f ( T 1 , T 3 ) имеет форму g ( T 1 )/ g ( T 3 ) (т.е. f ( T 1 , T 3 ) Т 3 ) знак равно ж ( Т 1 , Т 2 ) ж ( Т 2 , Т 3 ) знак равно г ( Т 1 ) / г ( Т 2 ) · г ( Т 2 ) / г ( Т 3 ) знак равно г ( Т 1 ) / g ( T 3 )) , где g — функция одной температуры. Теперь можно выбрать температурную шкалу с учетом того свойства, что
Подстановка (6) обратно в (4) дает зависимость эффективности от температуры:
Для TC = 0 К эффективность составляет 100 %, и эта эффективность становится больше 100 % ниже 0 К. Поскольку эффективность, превышающая 100 %, нарушает первый закон термодинамики, это означает, что 0 К — это минимально возможная температура. Фактически, самая низкая температура, когда-либо полученная в макроскопической системе , составила 20 нК и была достигнута в 1995 году в НИСТ. Вычитание правой части (5) из средней части и перестановка дает [22] [93]
где отрицательный знак указывает на тепло, выделяемое из системы. Это соотношение предполагает существование функции состояния S , изменение которой обычно исчезает для полного цикла, если она определяется формулой
где нижний индекс указывает на обратимый процесс. Эта функция соответствует энтропии системы, которая была описана ранее. Перестановка (8) дает формулу для температуры через фиктивные бесконечно малые квазиобратимые элементы энтропии и тепла:
Для системы постоянного объема, где энтропия S ( E ) является функцией ее энергии E , d E = d q rev и (9) дает
т.е. обратная температура - это скорость увеличения энтропии по отношению к энергии при постоянном объеме.
Статистическая механика определяет температуру на основе фундаментальных степеней свободы системы. Уравнение (10) является определяющим соотношением температуры, где энтропия определяется (с точностью до константы) логарифмом числа микросостояний системы в данном макросостоянии (как указано в микроканоническом ансамбле ):
где – постоянная Больцмана, W – число микросостояний с энергией E системы (вырождение).
Когда две системы с разными температурами соединяются чисто термически, тепло перетекает от системы с более высокой температурой к системе с более низкой температурой; термодинамически это понимается под вторым законом термодинамики: общее изменение энтропии после передачи энергии от системы 1 к системе 2 равно:
и поэтому положителен, если
С точки зрения статистической механики общее число микросостояний в объединенной системе 1 + система 2 равно , логарифм которого (умноженный на константу Больцмана) есть сумма их энтропий; таким образом, поток тепла от высокой температуры к низкой, приводящий к увеличению общей энтропии, более вероятен, чем любой другой сценарий (обычно он гораздо более вероятен), поскольку в результирующем макросостоянии больше микросостояний.
Определение температуры можно распространить даже на системы из нескольких частиц, например, на квантовую точку . Обобщенная температура получается путем рассмотрения временных ансамблей вместо ансамблей конфигурационного пространства, заданных в статистической механике, в случае теплового обмена и обмена частицами между небольшой системой фермионов ( N даже менее 10) с одно-/двухзаселенной системой. Конечный квантовый большой канонический ансамбль [94] , полученный в рамках гипотезы эргодичности и ортодичности, [95] позволяет выразить обобщенную температуру из отношения среднего времени пребывания и системы одиночного/двойного заполнения: [96]
где E F — энергия Ферми . Эта обобщенная температура стремится к обычной температуре, когда N стремится к бесконечности.
В эмпирических температурных шкалах, не привязанных к абсолютному нулю, отрицательная температура — это температура ниже нулевой точки используемой шкалы. Например, сухой лед имеет температуру сублимации−78,5 °C , что эквивалентно−109,3 ° F. [97] По абсолютной шкале Кельвина эта температура равна194,6 К. Ни одно тело не может быть доведено точно до0 К (температура идеально самого холодного тела) в результате любого конечного практически осуществимого процесса; это следствие третьего закона термодинамики . [98] [99] [100]
Согласно международной кинетической теории температура тела не может принимать отрицательные значения. Однако термодинамическая температурная шкала не так ограничена.
Для тела материи иногда можно концептуально определить, с точки зрения микроскопических степеней свободы, а именно спины частиц, подсистему с температурой, отличной от температуры всего тела. Когда тело находится в состоянии внутреннего термодинамического равновесия, температуры всего тела и подсистемы должны быть одинаковыми. Две температуры могут различаться, когда посредством работы через внешние силовые поля энергия может передаваться в подсистему и обратно отдельно от остальной части тела; тогда все тело не находится в состоянии внутреннего термодинамического равновесия. Существует верхний предел энергии, которого может достичь такая спиновая подсистема.
Считая подсистему находящейся во временном состоянии виртуального термодинамического равновесия, можно получить отрицательную температуру по термодинамической шкале. Термодинамическая температура является обратной производной энтропии подсистемы по ее внутренней энергии. По мере увеличения внутренней энергии подсистемы энтропия увеличивается в некотором диапазоне, но в конечном итоге достигает максимального значения, а затем начинает уменьшаться по мере того, как начинают заполняться состояния с наивысшей энергией. В точке максимума энтропии температурная функция демонстрирует поведение сингулярности , поскольку наклон энтропии как функции энергии уменьшается до нуля, а затем становится отрицательным. Когда энтропия подсистемы достигает максимума, ее термодинамическая температура достигает положительной бесконечности, переходя на отрицательную бесконечность, когда наклон становится отрицательным. Такие отрицательные температуры жарче, чем любая положительная температура. Со временем, когда подсистема подвергается воздействию остальной части тела, имеющей положительную температуру, энергия передается в виде тепла от подсистемы с отрицательной температурой к системе с положительной температурой. [101] Для таких подсистем температура кинетической теории не определена.
.jpg/440px-A_Guide_to_Cosmic_Temperatures_(SVS14374_-_Cosmic_Temperatures_Infographic_Final_Full).jpg)
уравнение(64).
Следовательно, мы определяем температуру как движущую силу, которая вызывает передачу так называемого тепла.
уравнения (39), (40) и (65).