В химии димеризация — это процесс соединения двух идентичных или подобных молекулярных объектов связями . Получающиеся связи могут быть как сильными, так и слабыми. Многие симметричные химические виды описываются как димеры , даже если мономер неизвестен или крайне нестабилен. [1]
Термин гомодимер используется, когда две субъединицы идентичны (например, A–A), и гетеродимер , когда они не идентичны (например, A–B). Обратную димеризацию часто называют диссоциацией . Когда два противоположно заряженных иона объединяются в димеры, их называют парами Бьеррума [ 2] в честь датского химика Нильса Бьеррума .

Безводные карбоновые кислоты образуют димеры путем водородной связи кислотного водорода и карбонильного кислорода. Например, уксусная кислота образует димер в газовой фазе, где мономерные единицы удерживаются вместе водородными связями . [3] Многие молекулы, содержащие ОН, образуют димеры, например, димер воды .
Эксимеры и эксиплексы — это возбужденные структуры с коротким временем жизни. Например, благородные газы не образуют стабильных димеров, но они образуют эксимеры Ar 2 *, Kr 2 * и Xe 2 * под высоким давлением и электрической стимуляцией. [4]
Молекулярные димеры часто образуются в результате реакции двух идентичных соединений, например: 2A → A−A . В этом примере говорят, что мономер «A» димеризуется, давая димер « A−A ».
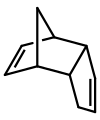
Дициклопентадиен — это асимметричный димер двух молекул циклопентадиена , которые прореагировали в реакции Дильса-Альдера, дав продукт. При нагревании он «трескается» (претерпевает ретрореакцию Дильса-Альдера), давая идентичные мономеры:
Многие неметаллические элементы встречаются в виде димеров: водород , азот , кислород и галогены фтор , хлор , бром и йод . Некоторые металлы образуют часть димеров в своей паровой фазе: дилитий ( Li2 ) , динатрий ( Na2 ), дикалий ( K2 ) , дирубидий ( Rb2 ) и дицезий ( Cs2 ). Такие элементарные димеры являются гомоядерными двухатомными молекулами .
В контексте полимеров «димер» также относится к степени полимеризации 2, независимо от стехиометрии или реакций конденсации .
Один из случаев, когда это применимо, — дисахариды . Например, целлобиоза — это димер глюкозы , хотя в результате реакции образования образуется вода :
При этом образующийся димер имеет стехиометрию, отличную от исходной пары мономеров.
Дисахариды не обязательно должны состоять из тех же моносахаридов , чтобы считаться димерами. Примером является сахароза , димер фруктозы и глюкозы, который следует тому же уравнению реакции, что и представлено выше.
Аминокислоты также могут образовывать димеры, которые называются дипептидами . Примером является глицилглицин , состоящий из двух молекул глицина, соединенных пептидной связью . Другие примеры включают аспартам и карнозин .
Многие молекулы и ионы описываются как димеры, даже если мономер неуловим.

Диборан (B 2 H 6 ) — димер борана , который неуловим и редко наблюдается. Почти все соединения типа R2BH существуют в виде димеров. [5]
Триалкилалюминиевые соединения могут существовать как мономеры или димеры, в зависимости от стерической массы присоединенных групп. Например, триметилалюминий существует как димер, но тримезитилалюминий принимает мономерную структуру. [6]
Димер циклопентадиенилхромтрикарбонила существует в измеримых равновесных количествах с монометаллическим радикалом ( C5H5 ) Cr ( CO) 3 . [7]
Пиримидиновые димеры (также известные как тиминовые димеры) образуются в результате фотохимической реакции из пиримидиновых оснований ДНК при воздействии ультрафиолетового света. [6] Это сшивание вызывает мутации ДНК , которые могут быть канцерогенными , вызывая рак кожи . [6] Когда присутствуют пиримидиновые димеры , они могут блокировать полимеразы , снижая функциональность ДНК до тех пор, пока она не будет восстановлена. [6]

Димеры белков возникают в результате взаимодействия двух белков , которые могут взаимодействовать дальше, образуя более крупные и сложные олигомеры . [8] Например, тубулин образуется путем димеризации α-тубулина и β-тубулина , и этот димер затем может полимеризоваться дальше, образуя микротрубочки . [9] Для симметричных белков более крупный белковый комплекс может быть разбит на более мелкие идентичные белковые субъединицы , которые затем димеризуются, уменьшая генетический код, необходимый для создания функционального белка. [8]
Как крупнейшее и наиболее разнообразное семейство рецепторов в геноме человека, рецепторы, сопряженные с G-белком (GPCR), были тщательно изучены, и недавние исследования подтвердили их способность образовывать димеры. [10] Димеры GPCR включают как гомодимеры, так и гетеродимеры, образованные из родственных членов семейства GPCR. [11] Хотя не все, некоторые GPCR требуют димеризации для функционирования, например, рецептор GABA B , что подчеркивает важность димеров в биологических системах. [12]

Подобно рецепторам, связанным с G-белком, димеризация необходима для рецепторных тирозинкиназ (RTK) для выполнения их функции в передаче сигнала , влияя на множество различных клеточных процессов. [13] RTK обычно существуют в виде мономеров, но претерпевают конформационные изменения при связывании лиганда , что позволяет им димеризоваться с близлежащими RTK. [14] [15] Димеризация активирует цитоплазматические домены киназы , которые отвечают за дальнейшую передачу сигнала . [13]