Аденозиндифосфат ( АДФ ), также известный как аденозинпирофосфат ( АПП ), является важным органическим соединением в метаболизме и необходим для потока энергии в живых клетках . АДФ состоит из трех важных структурных компонентов: сахарного остова, прикрепленного к аденину , и двух фосфатных групп, связанных с 5-м атомом углерода рибозы . Дифосфатная группа АДФ прикреплена к 5'-углероду сахарного остова, в то время как аденин прикреплен к 1'-углероду. [1]
АДФ может быть взаимопревращен в аденозинтрифосфат (АТФ) и аденозинмонофосфат (АМФ). АТФ содержит на одну фосфатную группу больше, чем АДФ, в то время как АМФ содержит на одну фосфатную группу меньше. Передача энергии, используемая всеми живыми существами, является результатом дефосфорилирования АТФ ферментами, известными как АТФазы . Расщепление фосфатной группы от АТФ приводит к связыванию энергии с метаболическими реакциями и побочным продуктом АДФ. [1] АТФ непрерывно реформируется из низкоэнергетических видов АДФ и АМФ. Биосинтез АТФ достигается посредством таких процессов, как фосфорилирование на уровне субстрата , окислительное фосфорилирование и фотофосфорилирование , каждый из которых облегчает добавление фосфатной группы к АДФ.
Цикл АДФ обеспечивает энергию, необходимую для выполнения работы в биологической системе, термодинамический процесс передачи энергии от одного источника к другому. Существует два типа энергии: потенциальная энергия и кинетическая энергия . Потенциальную энергию можно рассматривать как запасенную энергию или полезную энергию, которая доступна для выполнения работы. Кинетическая энергия — это энергия объекта в результате его движения. Значение АТФ заключается в его способности хранить потенциальную энергию в фосфатных связях. Энергия, запасенная между этими связями, затем может быть передана для выполнения работы. Например, передача энергии от АТФ к белку миозину вызывает конформационное изменение при соединении с актином во время сокращения мышцы . [1]
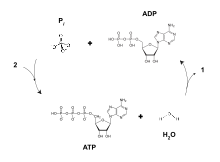
Для эффективного производства одного мышечного сокращения требуется несколько реакций между миозином и актином, и, следовательно, для производства каждого мышечного сокращения требуется наличие большого количества АТФ. По этой причине биологические процессы эволюционировали, чтобы производить эффективные способы пополнения потенциальной энергии АТФ из АДФ. [2]
Разрыв одной из фосфорных связей АТФ генерирует приблизительно 30,5 килоджоулей на моль АТФ (7,3 ккал ). [3] АДФ может быть преобразован или преобразован обратно в АТФ посредством процесса высвобождения химической энергии, содержащейся в пище; у людей это постоянно происходит посредством аэробного дыхания в митохондриях . [2] Растения используют фотосинтетические пути для преобразования и хранения энергии солнечного света, а также преобразования АДФ в АТФ. [3] Животные используют энергию, высвобождаемую при расщеплении глюкозы и других молекул, для преобразования АДФ в АТФ, которая затем может использоваться для обеспечения необходимого роста и поддержания клеток. [2]
Десятишаговый катаболический путь гликолиза является начальной фазой высвобождения свободной энергии при расщеплении глюкозы и может быть разделен на две фазы: подготовительную фазу и фазу выплаты. АДФ и фосфат необходимы в качестве предшественников для синтеза АТФ в реакциях выплаты цикла трикарбоновых кислот и механизма окислительного фосфорилирования . [4] Во время фазы выплаты гликолиза ферменты фосфоглицераткиназа и пируваткиназа облегчают добавление фосфатной группы к АДФ путем фосфорилирования на уровне субстрата . [5]
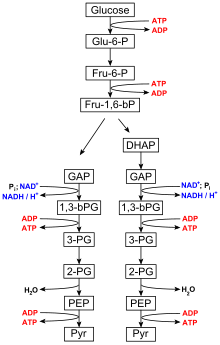
Гликолиз осуществляется всеми живыми организмами и состоит из 10 этапов. Чистая реакция для всего процесса гликолиза : [6]
Шаги 1 и 3 требуют ввода энергии, полученной в результате гидролиза АТФ до АДФ и Pi ( неорганического фосфата), тогда как шаги 7 и 10 требуют ввода АДФ, каждый из которых дает АТФ. [7] Ферменты , необходимые для расщепления глюкозы, находятся в цитоплазме , вязкой жидкости, которая заполняет живые клетки, где происходят гликолитические реакции. [1]
Цикл лимонной кислоты , также известный как цикл Кребса или цикл TCA (трикарбоновых кислот), представляет собой 8-шаговый процесс, в котором пируват, образующийся в результате гликолиза, преобразуется в 4 НАДН, ФАДН2 и ГТФ, которые затем преобразуются в АТФ. [8] Только на 5-м этапе, где ГТФ генерируется сукцинил-КоА-синтетазой, а затем преобразуется в АТФ, используется АДФ (ГТФ + АДФ → ГДФ + АТФ). [9]
Окислительное фосфорилирование производит 26 из 30 эквивалентов АТФ, образующихся при клеточном дыхании путем переноса электронов от НАДН или ФАДН2 к О2 через переносчики электронов. [10] Энергия, высвобождаемая при переносе электронов от НАДН или ФАДН2 с более высокой энергией к О2 с более низкой энергией, необходима для фосфорилирования АДФ и повторного образования АТФ. [11] Именно это энергетическое соединение и фосфорилирование АДФ до АТФ дает цепи переноса электронов название окислительное фосфорилирование. [1]
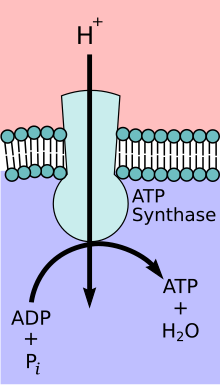
Во время начальных фаз гликолиза и цикла TCA такие кофакторы , как NAD+, отдают и принимают электроны [12] , что способствует способности цепи переноса электронов создавать градиент протонов через внутреннюю мембрану митохондрий. [13] Комплекс АТФ-синтазы существует внутри мембраны митохондрий (часть F O ) и выступает в матрикс (часть F 1 ). Энергия, полученная в результате химического градиента, затем используется для синтеза АТФ путем сопряжения реакции неорганического фосфата с АДФ в активном центре фермента АТФ-синтазы ; уравнение для этого можно записать как АДФ + P i → АТФ. [ необходима цитата ]
В нормальных условиях небольшие дискообразные тромбоциты циркулируют в крови свободно и не взаимодействуя друг с другом. АДФ хранится в плотных телах внутри тромбоцитов и высвобождается при активации тромбоцитов. АДФ взаимодействует с семейством рецепторов АДФ, обнаруженных на тромбоцитах (P2Y1, P2Y12 и P2X1), что приводит к активации тромбоцитов. [14]
АДФ в крови преобразуется в аденозин под действием экто-АДФаз , ингибируя дальнейшую активацию тромбоцитов через аденозиновые рецепторы . [ необходима ссылка ]