.JPG/440px-Old_drawing_of_a_Chlorine-Caustic_Soda_Plant_(Edgewood,_Maryland).JPG)
Хлорно -щелочной процесс (также хлорщелочной и хлорщелочной ) — промышленный процесс электролиза растворов хлорида натрия ( NaCl). Это технология, используемая для производства хлора и гидроксида натрия (каустической соды) [1] , которые являются товарными химическими веществами, необходимыми для промышленности. В 1987 году с помощью этого процесса было получено тридцать пять миллионов тонн хлора. [2] Хлор и гидроксид натрия, полученные по этому процессу, широко используются в химической промышленности.
Обычно процесс проводят в рассоле (водном растворе NaCl), в этом случае в результате образуются гидроксид натрия (NaOH), водород и хлор. При использовании хлорида кальция или хлорида калия продукты содержат кальций или калий вместо натрия. Известны родственные процессы, в которых используется расплавленный NaCl для получения хлора и металлического натрия или конденсированный хлористый водород для получения водорода и хлора.
Этот процесс требует высокого энергопотребления, например, около 2500 кВтч (9000 МДж) электроэнергии на тонну произведенного гидроксида натрия. Поскольку в результате процесса получаются эквивалентные количества хлора и гидроксида натрия (два моля гидроксида натрия на моль хлора), необходимо найти применение этим продуктам в одинаковой пропорции. На каждый моль произведенного хлора производится один моль водорода. Большая часть этого водорода используется для производства соляной кислоты , аммиака , перекиси водорода или сжигается для производства электроэнергии и/или пара. [3]
Хлорно-щелочной процесс используется с 19 века и является основной отраслью промышленности в США , Западной Европе и Японии . [4] [5] В 20 веке он стал основным источником хлора. [6] Процесс с диафрагменным элементом и процесс с ртутным элементом используются уже более 100 лет, но они являются экологически вредными из-за использования асбеста и ртути соответственно. Мембранный клеточный процесс, который был разработан только за последние 60 лет, является превосходным методом благодаря повышенной энергоэффективности и отсутствию вредных химикатов. [5]
Хотя первое образование хлора путем электролиза рассола приписывают химику Уильяму Крукшенку в 1800 году, только 90 лет спустя электролитический метод был успешно использован в промышленных масштабах. Промышленное производство началось в 1892 году. [7] В 1833 году Фарадей сформулировал законы, регулирующие электролиз водных растворов, а патенты были выданы Куку и Ватту в 1851 году и Стэнли в 1853 году на электролитическое производство хлора из рассола. [7]

Используются три метода производства. Хотя метод с использованием ртутных элементов производит гидроксид натрия, не содержащий хлора, использование нескольких тонн ртути приводит к серьезным экологическим проблемам. При нормальном производственном цикле в год выбрасывается несколько сотен фунтов ртути, которая накапливается в окружающей среде. Кроме того, хлор и гидроксид натрия, полученные в результате хлорщелочного процесса с использованием ртутных элементов, сами загрязнены следами ртути. Мембранно-диафрагменный метод не использует ртуть, но гидроксид натрия содержит хлор, который необходимо удалить.
Наиболее распространенный хлорщелочной процесс включает электролиз водного раствора хлорида натрия ( рассола ) в мембранной ячейке . Мембрана, например, изготовленная из Нафиона , Флемиона или Ациплекса, используется для предотвращения реакции между ионами хлора и гидроксида.
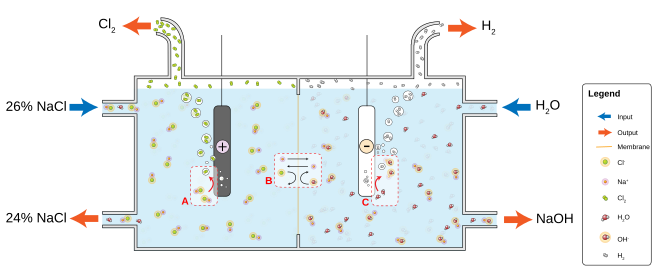
Насыщенный рассол подается в первую камеру ячейки, где ионы хлорида окисляются на аноде , теряя электроны и превращаясь в газообразный хлор ( A на рисунке):
На катоде положительные ионы водорода , вытянутые из молекул воды, восстанавливаются электронами, подаваемыми электролитическим током, до газообразного водорода, высвобождая ионы гидроксида в раствор ( C на рисунке):
Ионопроницаемая ионообменная мембрана в центре ячейки позволяет ионам натрия (Na + ) проходить во вторую камеру, где они вступают в реакцию с ионами гидроксида с образованием каустической соды (NaOH) ( B на рисунке). [1] Таким образом, общая реакция электролиза рассола такова:
В процессе диафрагменной ячейки имеются два отсека, разделенные проницаемой диафрагмой, часто изготовленной из асбестовых волокон . Рассол вводится в анодное отделение и перетекает в катодное отделение. Подобно мембранному элементу, ионы хлорида окисляются на аноде с образованием хлора, а на катоде вода расщепляется на каустическую соду и водород. Диафрагма предотвращает реакцию каустической соды с хлором. Разбавленный каустический рассол покидает камеру. Каустическая сода обычно должна быть сконцентрирована до 50% и удалена соль. Это делается с помощью испарительного процесса с использованием примерно трех тонн пара на тонну каустической соды. Соль, отделенную от каустического рассола, можно использовать для насыщения разбавленного рассола. Хлор содержит кислород, и его часто приходится очищать путем сжижения и испарения.

В процессе ртутного элемента, также известном как процесс Кастнера-Келлнера , насыщенный соляной раствор плавает поверх тонкого слоя ртути. Ртуть является катодом, где образуется натрий, образующий амальгаму с ртутью. Амальгама непрерывно вытягивается из ячейки и вступает в реакцию с водой, которая разлагает амальгаму на гидроксид натрия, водород и ртуть. Ртуть возвращается в электролизер. Хлор образуется на аноде и пузырьками выходит из ячейки. Ртутные элементы выводятся из обращения из-за опасений по поводу отравления ртутью в результате загрязнения ртутными элементами, например, которое произошло в Канаде (см. Болезнь Минамата Онтарио ) и Японии (см. Болезнь Минамата ).
В результате первоначальной общей реакции образуется гидроксид, а также газообразные водород и хлор: [8]
Без мембраны ионы OH - , образующиеся на катоде, могут свободно диффундировать по электролиту. По мере того, как электролит становится более основным из-за образования OH - , из раствора выходит меньше Cl 2 , поскольку он начинает диспропорционироваться с образованием ионов хлорида и гипохлорита на аноде:
Чем больше возможностей у Cl 2 взаимодействовать с NaOH в растворе, тем меньше Cl 2 выходит на поверхность раствора и тем быстрее прогрессирует образование гипохлорита. Это зависит от таких факторов, как температура раствора, время, в течение которого молекула Cl 2 находится в контакте с раствором, и концентрация NaOH.
Аналогично по мере увеличения концентрации гипохлоритов из них образуются хлораты:
Эта реакция ускоряется при температуре выше примерно 60 °C. Происходят и другие реакции, такие как самоионизация воды и разложение гипохлорита на катоде, скорость последней зависит от таких факторов, как диффузия и площадь поверхности катода, контактирующая с электролитом. [9]
Если ток прервется, когда катод погружен в воду, катоды, подвергшиеся воздействию гипохлоритов, например, изготовленных из нержавеющей стали, растворятся в неразделенных ячейках.
Если производство водорода и кислородных газов не является приоритетом, добавление в электролит 0,18% хромата натрия или калия повысит эффективность производства остальных продуктов. [9]
Из-за коррозионного характера производства хлора анод (где образуется хлор) должен быть инерционным и изготавливаться из таких материалов, как металлическая платина , [10] графит (во времена Фарадея его называли плюмбаго), [10] или платинированный титан . [11] Титановый анод, плакированный смешанными оксидами металлов (также называемый анодом со стабильными размерами), сегодня является промышленным стандартом. Исторически в качестве анодов также использовались платина, магнетит , диоксид свинца , [12] диоксид марганца и ферросилиций (13–15% кремния [13] ). [14] Платина, легированная иридием , более устойчива к коррозии от хлора, чем чистая платина. [14] [15] Неплакированный титан нельзя использовать в качестве анода, поскольку он анодирует , образуя непроводящий оксид и пассивирует . Графит будет медленно распадаться из-за внутреннего образования электролитического газа из-за пористой природы материала и образования углекислого газа в результате окисления углерода, в результате чего мелкие частицы графита будут взвешены в электролите, который можно удалить фильтрацией. Катод (где образуется гидроксид) может быть изготовлен из нелегированного титана, графита или более легко окисляемого металла, такого как нержавеющая сталь или никель .
Интересы производителей хлорщелочной продукции представляют на региональном, национальном и международном уровнях такие ассоциации, как Euro Chlor и Всемирный совет по хлору .