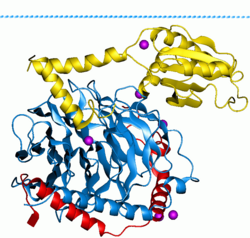
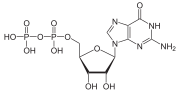

G-белки , также известные как белки, связывающие гуаниновые нуклеотиды , представляют собой семейство белков , которые действуют как молекулярные переключатели внутри клеток и участвуют в передаче сигналов от различных стимулов снаружи клетки внутрь. Их активность регулируется факторами, которые контролируют их способность связываться и гидролизовать гуанозинтрифосфат (ГТФ) до гуанозиндифосфата (ГДФ). Когда они привязаны к GTP, они «включены», а когда они привязаны к ВВП, они «выключены». G-белки принадлежат к более крупной группе ферментов , называемых GTPases .
Существует два класса G-белков. Первые функционируют как мономерные малые ГТФазы (маленькие G-белки), а вторые — как гетеротримерные комплексы G-белков . Последний класс комплексов состоит из альфа (Gα ) , бета (Gβ ) и гамма ( Gγ ) субъединиц . [1] Кроме того, бета- и гамма-субъединицы могут образовывать стабильный димерный комплекс , называемый бета-гамма-комплексом . [2]
Гетеротримерные G-белки, расположенные внутри клетки, активируются рецепторами, связанными с G-белками (GPCR), которые охватывают клеточную мембрану . [3] Сигнальные молекулы связываются с доменом GPCR, расположенным вне клетки, а внутриклеточный домен GPCR затем, в свою очередь, активирует определенный G-белок. Также было показано, что некоторые GPCR в активном состоянии «предварительно связаны» с G-белками, тогда как в других случаях считается, что имеет место механизм коллизионного сцепления. [4] [5] [6] Белок G запускает каскад дальнейших сигнальных событий , которые в конечном итоге приводят к изменению функции клетки. Рецепторы, связанные с G-белком, и G-белки, работая вместе, передают сигналы от многих гормонов , нейротрансмиттеров и других сигнальных факторов. [7] G-белки регулируют метаболические ферменты , ионные каналы , белки-переносчики и другие части клеточного механизма, контролируя транскрипцию , подвижность , сократимость и секрецию , которые, в свою очередь, регулируют различные системные функции, такие как эмбриональное развитие , обучение и память, а также гомеостаз . [8]
Белки G были открыты в 1980 году, когда Альфред Гилман и Мартин Родбелл исследовали стимуляцию клеток адреналином . Они обнаружили, что когда адреналин связывается с рецептором, рецептор не стимулирует ферменты (внутри клетки) напрямую. Вместо этого рецептор стимулирует белок G, который затем стимулирует фермент. Примером является аденилатциклаза , которая производит второй мессенджер циклический АМФ . [9] За это открытие они получили Нобелевскую премию по физиологии и медицине 1994 года . [10]
Нобелевские премии были присуждены за многие аспекты передачи сигналов G-белками и GPCR. К ним относятся антагонисты рецепторов , нейромедиаторы , обратный захват нейромедиаторов , рецепторы, связанные с G-белком , G-белки, вторичные мессенджеры , ферменты, которые запускают фосфорилирование белков в ответ на цАМФ и последующие метаболические процессы, такие как гликогенолиз .
Яркие примеры включают (в хронологическом порядке награждения):
G-белки являются важными молекулами , передающими сигналы в клетках. «Нарушение сигнальных путей GPCR [рецептора, связанного с G-белком] участвует во многих заболеваниях, таких как диабет , слепота, аллергия, депрессия, сердечно-сосудистые дефекты и некоторые формы рака . По оценкам, около 30% современных лекарств» клеточные мишени — это GPCR». [15] Геном человека кодирует около 800 [16] рецепторов, связанных с G-белком , которые обнаруживают фотоны света, гормоны, факторы роста, лекарства и другие эндогенные лиганды . Примерно 150 GPCR, обнаруженных в геноме человека, до сих пор имеют неизвестные функции.
В то время как G-белки активируются рецепторами, связанными с G-белком , они инактивируются белками RGS (что означает «регулятор передачи сигналов G-белка»). Рецепторы стимулируют связывание GTP (включение G-белка). Белки RGS стимулируют гидролиз GTP (создавая GDP и тем самым отключая G-белок).
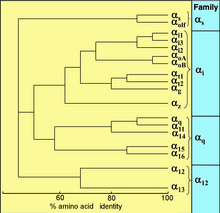
Все эукариоты используют G-белки для передачи сигналов и развили большое разнообразие G-белков. Например, люди кодируют 18 различных белков Gα , 5 белков Gβ и 12 белков Gγ . [17]
G-белок может относиться к двум различным семействам белков. Гетеротримерные G-белки , иногда называемые «большими» G-белками, активируются рецепторами, связанными с G-белками , и состоят из субъединиц альфа (α), бета (β) и гамма (γ) . «Маленькие» G-белки (20-25 кДа) принадлежат к суперсемейству малых ГТФаз Ras . Эти белки гомологичны субъединице альфа (α), обнаруженной в гетеротримерах, но на самом деле являются мономерными и состоят только из одной единицы. Однако, как и их более крупные родственники, они также связывают GTP и GDP и участвуют в передаче сигнала .
Различные типы гетеротримерных G-белков имеют общий механизм. Они активируются в ответ на конформационные изменения в GPCR, обменивая GDP на GTP и диссоциируя, чтобы активировать другие белки на определенном пути передачи сигнала . [18] Однако конкретные механизмы различаются в зависимости от типа белка.

Активируемые рецептором G-белки связаны с внутренней поверхностью клеточной мембраны . Они состоят из субъединиц Gα и тесно связанных с ними субъединиц Gβγ . Существует четыре основных семейства субъединиц Gα : Gαs ( G-стимулирующие), Gαi ( G-ингибирующие), Gαq /11 и Gα12 /13 . [20] [21] Они ведут себя по-разному при распознавании эффекторной молекулы, но имеют схожий механизм активации.
Когда лиганд активирует рецептор, связанный с G-белком , он вызывает конформационные изменения в рецепторе, которые позволяют рецептору функционировать как фактор обмена гуаниновых нуклеотидов (GEF), который обменивает GDP на GTP. GTP (или GDP) связан с субъединицей Gα в традиционном представлении об активации гетеротримерного GPCR. Этот обмен запускает диссоциацию субъединицы Gα ( которая связана с GTP) от димера Gβγ и рецептора в целом. Однако начинают приниматься модели, предполагающие молекулярную перегруппировку, реорганизацию и предварительное комплексообразование эффекторных молекул. [4] [22] [23] И Gα - GTP, и Gβγ могут затем активировать различные сигнальные каскады (или пути вторичного мессенджера ) и эффекторные белки, в то время как рецептор способен активировать следующий G-белок. [24]
Субъединица Gα в конечном итоге гидролизует присоединенный GTP до GDP за счет присущей ему ферментативной активности , что позволяет ему повторно ассоциироваться с Gβγ и начинать новый цикл. Группа белков, называемая регулятором передачи сигналов G-белка (RGS), действует как белки, активирующие GTPase (GAP), и специфична для субъединиц G α . Эти белки ускоряют гидролиз GTP до GDP, тем самым прекращая передачу сигнала. В некоторых случаях сам эффектор может обладать внутренней активностью GAP, которая затем может помочь деактивировать этот путь. Это справедливо в случае фосфолипазы С -бета, которая обладает активностью GAP в своей С-концевой области. Это альтернативная форма регуляции субъединицы Gα . Такие GαGAP не имеют каталитических остатков (специфических аминокислотных последовательностей) для активации белка Gα . Вместо этого они работают, снижая энергию активации, необходимую для протекания реакции. [25]
Gαs активирует цАМФ-зависимый путь , стимулируя выработку циклического АМФ (цАМФ) из АТФ . Это достигается путем прямой стимуляции мембраносвязанного фермента аденилатциклазы . Затем цАМФ может действовать как второй мессенджер, который затем взаимодействует с протеинкиназой А (ПКА) и активирует ее. PKA может фосфорилировать множество нижестоящих мишеней.
цАМФ -зависимый путь используется в качестве пути передачи сигнала для многих гормонов, включая:
Gαi ингибирует выработку цАМФ из АТФ. например соматостатин, простагландины
G αq/11 стимулирует мембраносвязанную фосфолипазу C бета, которая затем расщепляет фосфатидилинозитол-4,5-бисфосфат (PIP 2 ) на два вторичных мессенджера, инозитолтрифосфат (IP 3 ) и диацилглицерин (DAG). IP 3 индуцирует высвобождение кальция из эндоплазматического ретикулума . DAG активирует протеинкиназу C. Инозитол-фосфолипид-зависимый путь используется в качестве пути передачи сигнала для многих гормонов, включая:
Малые ГТФазы, также известные как малые G-белки, аналогичным образом связывают ГТФ и ВВП и участвуют в передаче сигнала . Эти белки гомологичны альфа-(α)-субъединице, присутствующей в гетеротримерах, но существуют в виде мономеров. Это небольшие (от 20 до 25 кДа) белки , которые связываются с гуанозинтрифосфатом ( GTP ). Это семейство белков гомологично Ras GTPases и также называется GTPases суперсемейства Ras .
Чтобы связаться с внутренним листком плазматической мембраны, многие G-белки и небольшие ГТФазы липидируются [ нужна цитация ] , то есть ковалентно модифицируются с помощью липидных удлинений. Они могут быть миристоилированными , пальмитоилированными или пренилированными .
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка )