
В координационной химии лиганд [а] — это ион или молекула с функциональной группой , которая связывается с центральным атомом металла с образованием координационного комплекса . Соединение с металлом обычно предполагает формальную передачу одной или нескольких электронных пар лиганда , часто через основания Льюиса . [1] Характер связи металл-лиганд может варьироваться от ковалентной до ионной . При этом порядок связи металл-лиганд может варьироваться от одного до трех. Лиганды рассматриваются как основания Льюиса, хотя известно, что в редких случаях используются кислотные «лиганды Льюиса ». [2] [3]
Металлы и металлоиды связаны с лигандами почти во всех случаях, хотя газообразные «голые» ионы металлов могут генерироваться в высоком вакууме. Лиганды в комплексе определяют реакционную способность центрального атома, включая скорость замещения лигандов, реакционную способность самих лигандов и окислительно-восстановительный потенциал . Выбор лиганда требует критического рассмотрения во многих практических областях, включая бионеорганическую и медицинскую химию , гомогенный катализ и химию окружающей среды .
Лиганды классифицируются по-разному, в том числе по заряду, размеру (объему), идентичности координирующего атома (атомов) и количеству электронов, отданных металлу ( дентатность или гаптичность ). Размер лиганда определяется углом его конуса .
Состав координационных комплексов известен с начала 1800-х годов, таких как берлинская лазурь и медный купорос . Ключевой прорыв произошел, когда Альфред Вернер согласовал формулы и изомеры . Он показал, среди прочего, что формулы многих соединений кобальта (III) и хрома (III) можно понять, если металл имеет шесть лигандов в октаэдрической геометрии . Первыми, кто использовал термин «лиганд», были Альфред Вернер и Карл Сомиски применительно к химии кремния. Теория позволяет понять разницу между координированным и ионным хлоридом в хлоридах аммиака кобальта и объяснить многие ранее необъяснимые изомеры. Он разделил первый координационный комплекс, названный гексолом, на оптические изомеры, опровергнув теорию о том, что хиральность обязательно связана с соединениями углерода. [4] [5]
В общем, лиганды рассматриваются как доноры электронов, а металлы как акцепторы электронов, т.е. соответственно основания Льюиса и кислоты Льюиса . Это описание было полуколичественным во многих отношениях, например, в модели ECW . Связь часто описывается с использованием формализмов теории молекулярных орбиталей. [6] [7]
Лиганды и ионы металлов можно упорядочить разными способами; одна система ранжирования фокусируется на «твердости» лиганда (см. также теорию твердой/мягкой кислоты/основания ). Ионы металлов преимущественно связывают определенные лиганды. В общем, ионы «жестких» металлов предпочитают лиганды слабого поля, тогда как ионы «мягких» металлов предпочитают лиганды сильного поля. Согласно теории молекулярных орбиталей, ВЗМО (высшая занятая молекулярная орбиталь) лиганда должна иметь энергию, которая перекрывается с НСМО (самая низкая незанятая молекулярная орбиталь) предпочтительного металла. Ионы металлов, связанные с лигандами сильного поля, подчиняются принципу Ауфбау , тогда как комплексы, связанные с лигандами слабого поля, следуют правилу Хунда .
Связывание металла с лигандами приводит к образованию набора молекулярных орбиталей, где металл можно идентифицировать с новыми ВЗМО и НСМО (орбитали, определяющие свойства и реакционную способность образующегося комплекса) и определенному упорядочению 5 d-орбиталей. (который может быть заполнен или частично заполнен электронами). В октаэдрической среде пять вырожденных d-орбиталей разделяются на наборы по 3 и 2 орбитали (более подробное объяснение см. в теории кристаллического поля ):
Разница в энергии между этими двумя наборами d-орбиталей называется параметром расщепления Δ o . Величина Δ o определяется напряженностью поля лиганда: лиганды сильного поля по определению увеличивают Δ o больше, чем лиганды слабого поля. Лиганды теперь можно сортировать по величине Δ o (см. таблицу ниже). Такое упорядочение лигандов почти неизменно для всех ионов металлов и называется спектрохимическим рядом .
Для комплексов с тетраэдрическим окружением d-орбитали снова распадаются на два набора, но на этот раз в обратном порядке:
Разница в энергии между этими двумя наборами d-орбиталей теперь называется Δt . Величина Δt меньше , чем для Δo , поскольку в тетраэдрическом комплексе на d-орбитали влияют только 4 лиганда, тогда как в октаэдрическом комплексе на d-орбитали влияют 6 лигандов. Когда координационное число не является ни октаэдрическим, ни тетраэдрическим, расщепление становится соответственно более сложным. Однако для целей ранжирования лигандов первоочередной интерес представляли свойства октаэдрических комплексов и образующаяся в результате Δo .
Расположение d-орбиталей на центральном атоме (определяемое «силой» лиганда) оказывает сильное влияние практически на все свойства образующихся комплексов. Например, разница в энергии d-орбиталей оказывает сильное влияние на спектры оптического поглощения металлокомплексов. Оказывается, что валентные электроны, занимающие орбитали со значительным 3d-орбитальным характером, поглощают в области спектра 400–800 нм ( УФ–видимый диапазон). Поглощение света (то, что мы воспринимаем как цвет ) этими электронами (то есть возбуждение электронов с одной орбитали на другую орбиталь под воздействием света) можно соотнести с основным состоянием металлокомплекса, которое отражает связывающие свойства лигандов. Относительное изменение (относительной) энергии d-орбиталей в зависимости от напряженности поля лигандов описывается диаграммами Танабе – Сугано .
В тех случаях, когда лиганд имеет низкую энергию НСМО, такие орбитали также участвуют в связывании. Связь металл-лиганд может быть дополнительно стабилизирована за счет формальной передачи электронной плотности обратно лиганду в процессе, известном как обратная связь . В этом случае заполненная орбиталь на основе центрального атома передает плотность НСМО (координированного) лиганда. Оксид углерода является ярким примером лиганда, который связывает металлы посредством обратного донорства. Дополнительно пи-донором могут служить лиганды с низкоэнергетическими заполненными орбиталями пи-симметрии.

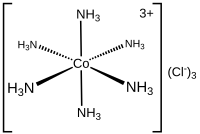
Лиганды классифицируются по количеству электронов, которые они «отдают» металлу. Лиганды L представляют собой основания Льюиса . Лиганды L представлены аминами , фосфинами , CO , N 2 и алкенами . Примеры лигандов L включают диводород и углеводороды, которые взаимодействуют посредством агостических взаимодействий . Лиганды X представляют собой галогениды и псевдогалогениды . Лиганды X обычно происходят из анионных предшественников, таких как хлорид, но включают лиганды, в которых соли аниона на самом деле не существуют, такие как гидрид и алкил. [8] [9]
В частности, в области металлоорганической химии лиганды классифицируются в соответствии с «методом CBC» для классификации ковалентных связей, популяризированным МЛХ Грином и «основанным на представлении о том, что существует три основных типа [лигандов]... представленных символы L, X и Z, которые соответствуют соответственно 2-электронным, 1-электронным и 0-электронным нейтральным лигандам». [10] [11]
Многие лиганды способны связывать ионы металлов через несколько сайтов, обычно потому, что лиганды имеют неподеленные пары более чем на одном атоме. Такие лиганды полидентатны. [12] Лиганды, которые связываются более чем одним атомом, часто называют хелатирующими . Лиганд, который связывается через два сайта, классифицируется как бидентатный , а три сайта — как тридентатный . « Угол прикуса » относится к углу между двумя связями бидентатного хелата. Хелатирующие лиганды обычно образуются путем связывания донорных групп посредством органических линкеров. Классическим бидентатным лигандом является этилендиамин , который получается путем связывания двух аммиачных групп этиленовым (-CH 2 CH 2 -) линкером. Классическим примером полидентатного лиганда является гексадентатный хелатирующий агент ЭДТА , который способен связываться через шесть участков, полностью окружая некоторые металлы. Количество раз, когда полидентатный лиганд связывается с металлическим центром, обозначается буквой « κ n », где n указывает количество мест, с помощью которых лиганд прикрепляется к металлу. ЭДТА 4- , когда она гексидентатная, связывается как κ 6 -лиганд, амины и атомы кислорода карбоксилата не соприкасаются. На практике значение n лиганда не указывается явно, а скорее предполагается. Сродство связывания хелатной системы зависит от угла хелатирования или угла прикуса .
Дентичность (обозначенная κ ) — это номенклатура, описывающая количество несмежных атомов лиганда, связанных с металлом. Этот дескриптор часто опускается, поскольку дентальность лиганда часто очевидна. Комплекс трис(этилендиамин)кобальта(III) можно описать как [Co(κ 2 -en) 3 ] 3+ .
Комплексы полидентатных лигандов называются хелатными комплексами. Они имеют тенденцию быть более стабильными, чем комплексы, полученные из монодентатных лигандов. Эта повышенная стабильность, называемая хелатным эффектом , обычно объясняется эффектами энтропии , которая способствует смещению многих лигандов одним полидентатным лигандом.
С хелатным эффектом связан макроциклический эффект . Макроциклический лиганд — это любой крупный лиганд, который хотя бы частично окружает центральный атом и связывается с ним, оставляя центральный атом в центре большого кольца. Чем жестче и выше его дентатность, тем более инертным будет макроциклический комплекс. Гем является примером, в котором атом железа находится в центре порфиринового макроцикла , связанного с четырьмя атомами азота тетрапиррольного макроцикла. Очень стабильный диметилглиоксиматный комплекс никеля представляет собой синтетический макроцикл, полученный из диметилглиоксима .
Гаптичность (обозначенная греческой буквой η ) относится к числу смежных атомов, которые составляют донорный участок и прикрепляются к металлическому центру. Обозначение η применяется, когда координировано несколько атомов. Например, η 2 представляет собой лиганд, который координирует свои действия через два смежных атома. Бутадиен образует комплексы как η 2 , так и η 4 в зависимости от числа атомов углерода, связанных с металлом. [13] [14] [15]
Транс-связывающие лиганды представляют собой бидентатные лиганды, которые могут занимать координационные позиции на противоположных сторонах координационного комплекса. [16]
В отличие от полидентатных лигандов амбидентатные лиганды могут прикрепляться к центральному атому в любом из двух (или более) мест, но не в обоих. Примером является тиоцианат SCN- , который может присоединяться либо к атому серы, либо к атому азота. Такие соединения вызывают изомерию сцепления .
Таким образом, полидентат и амбидентат представляют собой два разных типа полифункциональных лигандов (лиганды с более чем одной функциональной группой ), которые могут связываться с металлическим центром через разные атомы лиганда с образованием различных изомеров. Полидентатные лиганды могут связываться через один атом И другой (или несколько других) одновременно, тогда как амбидентатные лиганды могут связываться через один атом ИЛИ другой. Белки представляют собой сложные примеры полифункциональных лигандов, обычно полидентатных.
Мостиковый лиганд связывает два или более металлоцентра. Практически все неорганические твердые вещества с простыми формулами представляют собой координационные полимеры , состоящие из центров ионов металлов, связанных мостиковыми лигандами. В эту группу материалов входят все безводные бинарные галогениды и псевдогалогениды металлов. Мостиковые лиганды также сохраняются в растворе. Многоатомные лиганды, такие как карбонат, являются амбидентатными и поэтому часто связываются с двумя или тремя металлами одновременно. Атомы, соединяющие металлы, иногда обозначаются префиксом « μ ». Большинство неорганических твердых веществ являются полимерами благодаря наличию множества мостиковых лигандов. Мостиковые лиганды, способные координировать несколько ионов металлов, привлекают значительный интерес из-за их потенциального использования в качестве строительных блоков для изготовления функциональных мультиметаллических ансамблей. [17]
Биядерные лиганды связывают два иона металлов. [18] Обычно бинуклеирующие лиганды содержат мостиковые лиганды, такие как феноксид, пиразолат или пиразин, а также другие донорные группы, которые связываются только с одним из двух ионов металлов.
Некоторые лиганды могут связываться с металлическим центром через один и тот же атом, но с разным числом неподеленных пар . Порядок связи металл-лиганд можно частично определить по углу связи металл-лиганд (M-X-R). Этот валентный угол часто называют линейным или изогнутым, с дальнейшим обсуждением степени, в которой угол изогнут. Например, имидо-лиганд в ионной форме имеет три неподеленные пары. Одна неподеленная пара используется в качестве донора сигма-X, две другие неподеленные пары доступны в качестве доноров pi L-типа. Если обе неподеленные пары используются в пи-связях, то геометрия M-N-R является линейной. Однако, если одна или обе эти неподеленные пары не являются связующими, то связь M-N-R искривляется, и степень изгиба говорит о том, насколько сильной может быть пи-связь. η 1 -Оксид азота может координироваться с металлическим центром линейным или изогнутым образом.
Лиганд-спектатор — это сильно координирующийся полидентатный лиганд, который не участвует в химических реакциях, но удаляет активные центры на металле. Лиганды-спектаторы влияют на реакционную способность металлоцентра, с которым они связаны.
Объемные лиганды используются для управления стерическими свойствами металлоцентра. Они используются по многим причинам, как практическим, так и академическим. С практической стороны они влияют на селективность металлических катализаторов, например, при гидроформилировании . Представляет академический интерес объемистые лиганды, которые стабилизируют необычные координационные центры, например, реакционноспособные колиганды или низкие координационные числа. Часто объемистые лиганды используются для моделирования стерической защиты, обеспечиваемой белками металлосодержащим активным центрам. Конечно, чрезмерная стерическая масса может препятствовать координации определенных лигандов.
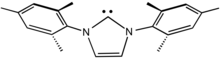
Хиральные лиганды полезны для индукции асимметрии внутри координационной сферы. Часто лиганд используют в виде оптически чистой группы. В некоторых случаях, например, в случае вторичных аминов, асимметрия возникает при координации. Хиральные лиганды используются в гомогенном катализе , например асимметричном гидрировании .
Гемилабильные лиганды содержат по крайней мере две электронно различные координационные группы и образуют комплексы, в которых одна из них легко вытесняется из металлического центра, а другая остается прочно связанной. Было обнаружено, что такое поведение увеличивает реакционную способность катализаторов по сравнению с использованием более традиционные лиганды.
Неиннокентные лиганды связываются с металлами таким образом, что распределение электронной плотности между металлическим центром и лигандом неясно. Описание связывания невинных лигандов часто включает в себя описание нескольких резонансных форм , которые вносят частичный вклад в общее состояние.
Практически каждая молекула и каждый ион могут служить лигандом (или «координировать») металлов. К монодентатным лигандам относятся практически все анионы и все простые основания Льюиса. Таким образом, галогениды и псевдогалогениды являются важными анионными лигандами, тогда как аммиак , окись углерода и вода являются особенно распространенными лигандами с нейтральным зарядом. Простые органические соединения также очень распространены, будь то анионные ( RO − и RCO−
2) или нейтральный ( R 2 O , R 2 S , R 3− x NH x и R 3 P ). Стерические свойства некоторых лигандов оценивают по углам их конусов .
Помимо классических оснований и анионов Льюиса, все ненасыщенные молекулы также являются лигандами, используя свои пи-электроны для образования координатной связи. Кроме того, металлы могут связываться с σ-связями, например , в силанах , углеводородах и диводороде (см. Также: Агостическое взаимодействие ).
В комплексах неиннокентных лигандов лиганд связан с металлами обычными связями, но лиганд также обладает окислительно-восстановительной активностью.
В следующей таблице лиганды отсортированы по напряженности поля [ нужна ссылка ] (сначала лиганды слабого поля):
Записи в таблице отсортированы по напряженности поля, связыванию через указанный атом (т.е. как концевой лиганд). «Сила» лиганда меняется, когда лиганд связывается альтернативным способом связывания (например, когда он образует мостик между металлами) или когда конформация лиганда искажается (например, линейный лиганд, который в результате стерических взаимодействий вынужден связываться в нелинейная мода).
В этой таблице другие распространенные лиганды перечислены в алфавитном порядке.
Лигандный обмен (также называемый заменой лиганда ) — это химическая реакция , в которой лиганд в соединении заменяется другим. Признаны два общих механизма: ассоциативное замещение или диссоциативное замещение .

Ассоциативное замещение очень похоже на механизм S N 2 в органической химии. Обычно меньший лиганд может присоединиться к ненасыщенному комплексу с последующей потерей другого лиганда. Обычно скорость замещения имеет первый порядок при входе в лиганд L и ненасыщенный комплекс. [19]

Диссоциативное замещение характерно для октаэдрических комплексов. Этот путь очень похож на механизм S N 1 в органической химии. Идентичность входящего лиганда не влияет на скорость. [19]
BioLiP [20] представляет собой обширную базу данных по взаимодействиям лиганд-белок, в которой трехмерная структура взаимодействий лиганд-белок взята из банка данных белков . MANORAA — веб-сервер для анализа консервативного и дифференциального молекулярного взаимодействия лиганда в комплексе с гомологами белковой структуры из Банка данных белков. Он обеспечивает связь с белками-мишенями, такими как его расположение в биохимических путях, SNP и базовая экспрессия белка/РНК в органе-мишени. [21]