
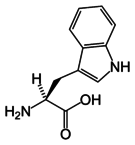

Ароматическая аминокислота – это аминокислота , включающая ароматическое кольцо.

Среди 20 стандартных аминокислот к ароматическим относят гистидин , фенилаланин , триптофан , тирозин .
Ароматические аминокислоты, за исключением гистидина , поглощают ультрафиолетовый свет с длиной волны выше 250 нм и флуоресцируют в этих условиях. Эта характеристика используется в количественном анализе, в частности при определении концентрации этих аминокислот в растворе. [1] [2] Большинство белков поглощают длину волны 280 нм из-за присутствия тирозина и триптофана . Из ароматических аминокислот наибольший коэффициент угасания имеет триптофан ; максимум его поглощения приходится на длину волны 280 нм. Максимум поглощения тирозина приходится на длину волны 274 нм. [3]
Ароматические аминокислоты стабилизируют складчатую структуру многих белков. [4] [5] Ароматические остатки обнаруживаются преимущественно в ядрах глобулярных белков , хотя часто составляют ключевые части интерфейсов взаимодействия белок-белок или белок- лиганд на поверхности белка.
Ароматические аминокислоты часто служат предшественниками важных биохимических веществ.
У растений шикиматный путь сначала приводит к образованию хоризмата , который является предшественником фенилаланина, тирозина и триптофана. Эти ароматические аминокислоты являются предшественниками многих вторичных метаболитов , необходимых для биологических функций растения, таких как гормоны салицилат и ауксин . Этот путь содержит ферменты, которые можно регулировать с помощью ингибиторов, которые могут остановить выработку хоризмата и, в конечном итоге, биологические функции организма. Гербициды и антибиотики действуют путем ингибирования этих ферментов, участвующих в биосинтезе ароматических аминокислот, тем самым делая их токсичными для растений. [7] Глифосат , тип гербицида, используется для контроля накопления лишней зелени. Помимо уничтожения зелени, глифосат может легко влиять на поддержание микробиоты кишечника в организмах-хозяевах, специфически ингибируя 5-енолпирувилшикимат-3-фосфатсинтазу, которая предотвращает биосинтез незаменимых ароматических аминокислот. Ингибирование этого фермента приводит к таким расстройствам, как желудочно-кишечные заболевания и метаболические заболевания. [8]
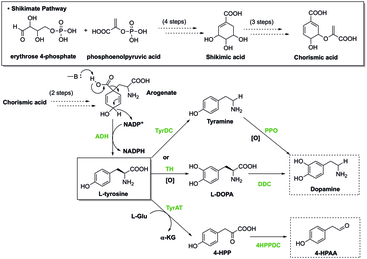
Животные получают ароматические аминокислоты из своего рациона, но почти [а] все растения и некоторые микроорганизмы должны синтезировать ароматические аминокислоты метаболически затратным путем шикимата , чтобы их производить. Гистидин , фенилаланин , триптофан — незаменимые аминокислоты для животных. Поскольку они не синтезируются в организме человека, их необходимо получать с пищей. Тирозин является полунезаменимым; следовательно, он может синтезироваться животным, но только из фенилаланина. Фенилкетонурия , генетическое заболевание, возникающее в результате неспособности расщеплять фенилаланин, возникает из-за отсутствия фермента фенилаланингидроксилазы . Недостаток триптофана в рационе может вызвать задержку развития скелета. [9] Чрезмерное потребление ароматических аминокислот, значительно превышающее уровни, получаемые при обычном потреблении белка, может привести к гипертонии , [10] что может долгое время оставаться незамеченным у здоровых людей. Это может быть вызвано и другими факторами, такими как употребление различных трав и продуктов, таких как шоколад, которые в разной степени ингибируют ферменты моноаминоксидазы , а также некоторых лекарств. Ароматические следовые амины, такие как тирамин, могут вытеснять норадреналин из периферических моноаминовых везикул , а у людей, принимающих ингибиторы моноаминоксидазы (ИМАО), это происходит настолько, что становится опасным для жизни. Синдром голубого подгузника — аутосомно-рецессивное заболевание , вызванное плохим усвоением триптофана в организме.