Аскорбиновая кислота — органическое соединение формулы С.
6ЧАС
8О
6, первоначально называвшаяся гексуроновой кислотой . Это белое твердое вещество, но нечистые образцы могут иметь желтоватый оттенок. Он свободно растворяется в воде, образуя слабокислые растворы. Это мягкий восстановитель .
Аскорбиновая кислота существует в виде двух энантиомеров (зеркальных изомеров ), обычно обозначаемых « l » (от «лево») и « d » (от «декстро»). L - изомер встречается чаще всего: он встречается в природе во многих продуктах питания и представляет собой одну из форм (« витамер ») витамина С , необходимого питательного вещества для человека и многих животных. Дефицит витамина С вызывает цингу , которая раньше была основной болезнью моряков в длительных морских путешествиях. Он используется в качестве пищевой добавки и диетической добавки из-за своих антиоксидантных свойств. Форма « d » может быть получена путем химического синтеза , но не имеет существенной биологической роли.
Противоцинготные свойства некоторых продуктов были продемонстрированы в 18 веке Джеймсом Линдом . В 1907 году Аксель Хольст и Теодор Фрёлих обнаружили, что противоцинготный фактор представляет собой водорастворимое химическое вещество, отличное от того, которое предотвращает авитаминоз . Между 1928 и 1932 годами Альберт Сент-Дьердьи выделил кандидата на это вещество, которое он назвал «гексуроновой кислотой», сначала из растений, а затем из надпочечников животных. В 1932 году Чарльз Глен Кинг подтвердил, что это действительно противоцинготный фактор.
В 1933 году химик-сахар Уолтер Норман Хауорт , работая с образцами «гексуроновой кислоты», которые Сент-Дьёрдьи выделил из паприки и прислал ему в предыдущем году, установил правильную структуру и оптико-изомерную природу соединения, а в 1934 году сообщил о его первый синтез. [2] [3] Что касается противоцинготных свойств соединения, Хаворт и Сент-Дьёрдьи предложили переименовать его в «а-скорбиновую кислоту», а позже конкретно в l -аскорбиновую кислоту. [4] За их работу в 1937 году две Нобелевские премии : по химии и физиологии и медицине были присуждены Хаворту и Сент-Дьёрдьи соответственно.
Независимо аскорбиновая кислота была синтезирована в 1933 году Тадеушем Райхштейном (лауреатом Нобелевской премии по физиологии и медицине 1950 года). [5]
Аскорбиновая кислота представляет собой лактон 2-кетоглюконовой кислоты на основе фурана . Он содержит соседний эндиол, соседний с карбонилом . Эта структурная картина -C(OH)=C(OH)-C(=O)- характерна для редуктонов и увеличивает кислотность одной из енольных гидроксильных групп . Депротонированное сопряженное основание представляет собой аскорбат- анион, который стабилизируется за счет делокализации электронов, возникающей в результате резонанса между двумя формами:
По этой причине аскорбиновая кислота гораздо более кислая, чем можно было бы ожидать, если бы соединение содержало только изолированные гидроксильные группы.
Аскорбат-анион образует соли , такие как аскорбат натрия , аскорбат кальция и аскорбат калия .
Аскорбиновая кислота также может реагировать с органическими кислотами в виде спиртов , образуя сложные эфиры, такие как аскорбилпальмитат и аскорбилстеарат .
Нуклеофильная атака аскорбиновой кислоты на протон приводит к образованию 1,3-дикетона:
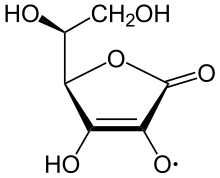
Ион аскорбата является преобладающим видом при типичных биологических значениях pH. Это мягкий восстановитель и антиоксидант . Он окисляется с потерей одного электрона с образованием катион -радикала , а затем с потерей второго электрона с образованием дегидроаскорбиновой кислоты . Обычно он реагирует с окислителями активных форм кислорода , такими как гидроксильный радикал .
Аскорбиновая кислота особенная, поскольку она может переносить один электрон благодаря резонансно-стабилизированной природе ее собственного ион-радикала , называемого полудегидроаскорбатом . Чистая реакция:
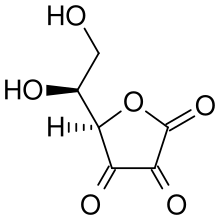
Под воздействием кислорода аскорбиновая кислота подвергается дальнейшему окислительному разложению с образованием различных продуктов, включая дикетогулоновую кислоту, ксилоновую кислоту , треоновую кислоту и щавелевую кислоту . [7]
Активные формы кислорода наносят вред животным и растениям на молекулярном уровне из-за их возможного взаимодействия с нуклеиновыми кислотами , белками и липидами. Иногда эти радикалы инициируют цепные реакции. Аскорбат может прекратить эти цепные радикальные реакции путем переноса электрона . Окисленные формы аскорбата относительно нереактивны и не вызывают повреждения клеток.
Однако, будучи хорошим донором электронов, избыток аскорбата в присутствии свободных ионов металлов может не только стимулировать, но и инициировать свободнорадикальные реакции, что делает его потенциально опасным прооксидантным соединением в определенных метаболических контекстах.
Аскорбиновая кислота и ее натриевые, калиевые и кальциевые соли широко используются в качестве антиоксидантных пищевых добавок . Эти соединения водорастворимы и, следовательно, не могут защитить жиры от окисления: с этой целью в качестве антиоксидантных пищевых добавок можно использовать жирорастворимые эфиры аскорбиновой кислоты с длинноцепочечными жирными кислотами (аскорбилпальмитат или аскорбилстеарат).
Он создает летучие соединения при смешивании с глюкозой и аминокислотами при 90 °C. [8]
Это кофактор окисления тирозина . [9]
Основное применение l -аскорбиновой кислоты и ее солей — в качестве пищевых добавок, главным образом для борьбы с окислением. Он одобрен для этой цели в ЕС под номером E E300, [10] в США, [11] в Австралии и Новой Зеландии. [12]
Еще одно важное применение l- аскорбиновой кислоты – это пищевая добавка . Он включен в Список основных лекарственных средств Всемирной организации здравоохранения . [13]
Естественный биосинтез витамина С происходит во многих растениях и животных посредством множества процессов.
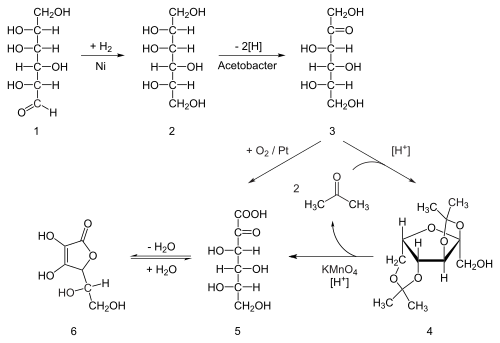
Семьдесят процентов мировых поставок аскорбиновой кислоты производится в Китае. [21] Аскорбиновую кислоту получают в промышленности из глюкозы методом, основанным на историческом процессе Райхштейна . На первом из пяти стадий процесса глюкоза каталитически гидрируется до сорбита , который затем окисляется микроорганизмом Acetobacter suboxydans до сорбозы . В результате этой ферментативной реакции окисляется только одна из шести гидроксильных групп. С этого момента доступны два маршрута. Обработка продукта ацетоном в присутствии кислотного катализатора превращает четыре из оставшихся гидроксильных групп в ацетали . Незащищенная гидроксильная группа окисляется до карбоновой кислоты в результате реакции с каталитическим окислителем ТЕМПО (регенерированным гипохлоритом натрия – отбеливающим раствором). Исторически сложилось так, что при промышленном приготовлении по процессу Райхштейна в качестве отбеливающего раствора использовался перманганат калия . Кислотно-катализируемый гидролиз этого продукта выполняет двойную функцию: удаление двух ацетальных групп и лактонизацию замыкания кольца . На этом этапе получается аскорбиновая кислота. Каждый из пяти этапов имеет доходность более 90%. [22]
Более биотехнологический процесс, впервые разработанный в Китае в 1960-х годах, но получивший дальнейшее развитие в 1990-х годах, обходится без использования защитных групп ацетона. Второй генетически модифицированный вид микробов, такой как мутант Erwinia , среди прочих, окисляет сорбозу в 2-кетоглюконовую кислоту (2-KGA), которая затем может подвергаться лактонизации с замыканием цикла посредством дегидратации. Этот метод используется в основном процессе производства аскорбиновой кислоты в Китае, который поставляет 70% мировой аскорбиновой кислоты. [21] Исследователи изучают способы одноэтапной ферментации. [23] [24]
Традиционным способом анализа содержания аскорбиновой кислоты является процесс титрования окислителем , разработано несколько методик.
Популярный метод йодометрии использует йод в присутствии индикатора крахмала . Йод восстанавливается аскорбиновой кислотой, и, когда вся аскорбиновая кислота прореагировала, йод оказывается в избытке, образуя сине-черный комплекс с индикатором крахмалом. Это указывает на конечную точку титрования.
В качестве альтернативы аскорбиновую кислоту можно обработать избытком йода с последующим обратным титрованием тиосульфатом натрия, используя в качестве индикатора крахмал. [25]
Этот йодометрический метод был переработан для использования реакции аскорбиновой кислоты с йодатом и йодидом в растворе кислоты . При электролизе раствора йодида калия образуется йод, который реагирует с аскорбиновой кислотой. Окончание процесса определяют потенциометрическим титрованием аналогично титрованию по Карлу Фишеру . Количество аскорбиновой кислоты можно рассчитать по закону Фарадея .
Другая альтернатива использует N -бромсукцинимид (NBS) в качестве окислителя в присутствии йодида калия и крахмала. NBS сначала окисляет аскорбиновую кислоту; когда последний исчерпывается, НБС высвобождает йод из йодида калия, который затем образует сине-черный комплекс с крахмалом.