Ниобий — химический элемент ; он имеет символ Nb (ранее колумбий , Cb ) и атомный номер 41. Это светло-серый, кристаллический и пластичный переходный металл . Чистый ниобий имеет твердость по шкале Мооса , аналогичную чистому титану [4] , а пластичность аналогична железу . Ниобий окисляется в атмосфере Земли очень медленно, поэтому его применяют в ювелирных изделиях в качестве гипоаллергенной альтернативы никелю . Ниобий часто встречается в минералах пирохлоре и колумбите , отсюда и прежнее название «колумбий». Ее название происходит из греческой мифологии : Ниоба , дочь Тантала , тезки тантала . Название отражает большое сходство между двумя элементами в их физических и химических свойствах, что затрудняет их различие. [5]
Английский химик Чарльз Хэтчетт сообщил о новом элементе, похожем на тантал, в 1801 году и назвал его колумбием. В 1809 году английский химик Уильям Хайд Волластон ошибочно пришел к выводу, что тантал и колумбий идентичны. Немецкий химик Генрих Розе в 1846 году определил, что танталовые руды содержат второй элемент, который он назвал ниобием. В 1864 и 1865 годах ряд научных открытий выявил, что ниобий и колумбий были одним и тем же элементом (в отличие от тантала), и в течение столетия оба названия использовались как синонимы. Ниобий был официально принят в качестве названия элемента в 1949 году, но название колумбий до сих пор используется в металлургии США.
Лишь в начале 20 века ниобий впервые был использован в коммерческих целях. Ниобий является важной добавкой к высокопрочным низколегированным сталям. Бразилия является ведущим производителем ниобия и феррониобия , сплава 60–70% ниобия с железом. Ниобий используется в основном в сплавах, большая часть которого содержится в специальной стали , например, используемой в газопроводах . Хотя эти сплавы содержат максимум 0,1%, небольшой процент ниобия повышает прочность стали за счет удаления карбидов и нитридов . Температурная стабильность ниобийсодержащих суперсплавов важна для их использования в реактивных и ракетных двигателях .
Ниобий используется в различных сверхпроводящих материалах. Эти сплавы , также содержащие титан и олово , широко используются в сверхпроводящих магнитах МРТ -сканеров . Другие области применения ниобия включают сварку, атомную промышленность, электронику, оптику, нумизматику и ювелирные изделия. В последних двух применениях очень желательными свойствами являются низкая токсичность и радужное свечение, вызванное анодированием . Ниобий считается технологически важным элементом .
.jpg/440px-Charles_Hatchett._Soft-ground_etching_by_F._C._Lewis_after_T_Wellcome_V0002614_(cropped).jpg)
_-_n._2990_-_Niobe_madre_-_Firenze.jpg/440px-Sommer,_Giorgio_(1834-1914)_-_n._2990_-_Niobe_madre_-_Firenze.jpg)
Ниобий был идентифицирован английским химиком Чарльзом Хэтчеттом в 1801 году. [6] [7] [8] Он обнаружил новый элемент в образце минерала, который был отправлен в Англию из Коннектикута , США, в 1734 году Джоном Уинтропом (внуком Джона Уинтроп Младший ) и назвал минерал колумбит и новый элемент колумбий в честь Колумбии , поэтического названия Соединенных Штатов. [9] [10] [11] Колумбий , открытый Хэтчеттом, вероятно, представлял собой смесь нового элемента с танталом. [9]
Впоследствии возникла значительная путаница [12] по поводу разницы между колумбием (ниобием) и близкородственным танталом. В 1809 году английский химик Уильям Хайд Волластон сравнил оксиды, полученные как из колумбия — колумбита, с плотностью 5,918 г/см 3 , так и из тантала — танталита , с плотностью более 8 г/см 3 , и пришел к выводу, что два оксида, несмотря на значительная разница в плотности была идентична; таким образом, он сохранил название тантал. [12] Этот вывод был оспорен в 1846 году немецким химиком Генрихом Розе , который утверждал, что в образце танталита было два разных элемента, и назвал их в честь детей Тантала : ниобий ( от Ниобы ) и пелопий (от Пелопса ). [13] [14] Эта путаница возникла из-за минимальных наблюдаемых различий между танталом и ниобием. Заявленные новые элементы пелопий , ильмений и дианий [15] на самом деле были идентичны ниобию или смесям ниобия и тантала. [16]
Различия между танталом и ниобием были однозначно продемонстрированы в 1864 году Кристианом Вильгельмом Бломстрандом [16] и Анри Этьеном Сент-Клер Девилем , а также Луи Дж. Тростом , определившим формулы некоторых соединений в 1865 году [16] [17 ] ] и, наконец, швейцарским химиком Жаном Шарлем Галиссаром де Мариньяком [18] в 1866 году, которые доказали, что существует только два элемента. Статьи об ильмениуме продолжали появляться до 1871 года. [19]
Де Мариньяк был первым, кто получил металл в 1864 году, когда он восстановил хлорид ниобия, нагревая его в атмосфере водорода . [20] Хотя де Мариньяк смог производить ниобий, не содержащий тантала, в более крупных масштабах к 1866 году, только в начале 20 века ниобий стал использоваться в нитях накаливания , что стало первым коммерческим применением. [17] Это использование быстро устарело из-за замены ниобия вольфрамом , который имеет более высокую температуру плавления. Тот факт, что ниобий повышает прочность стали, был впервые обнаружен в 1920-х годах, и это применение остается его основным применением. [17] В 1961 году американский физик Юджин Канцлер и его коллеги из Bell Labs обнаружили, что ниобий-олово продолжает проявлять сверхпроводимость в присутствии сильных электрических токов и магнитных полей, [21] что сделало его первым материалом, поддерживающим высокие токи и поля, необходимые для полезных мощных магнитов и электроэнергетического оборудования . Это открытие позволило — два десятилетия спустя — производить длинные многожильные кабели, намотанные в катушки, для создания больших и мощных электромагнитов для вращающихся механизмов, ускорителей частиц и детекторов частиц. [22] [23]
Колумбий (символ Cb) [24] — это название, первоначально данное Хэтчеттом после открытия металла в 1801 году. [7] Название отражало то, что типовой образец руды был доставлен из Соединенных Штатов Америки ( Колумбия ). [25] Это название до сих пор используется в американских журналах — последняя статья, опубликованная Американским химическим обществом с колумбием в названии, датируется 1953 годом [26] — в то время как ниобий использовался в Европе. Чтобы положить конец этой путанице, название ниобий было выбрано для элемента 41 на 15-й конференции Союза химии в Амстердаме в 1949 году. [27] Год спустя это название было официально принято Международным союзом теоретической и прикладной химии (IUPAC). после 100 лет споров, несмотря на хронологический приоритет названия «Колумбий» . [27] Это был своего рода компромисс; [27] ИЮПАК принял вольфрам вместо вольфрама из уважения к использованию в Северной Америке; и ниобий вместо колумбия из уважения к европейскому использованию. Хотя многие химические общества и правительственные организации США обычно используют официальное название IUPAC, некоторые металлурги и общества металлов до сих пор используют оригинальное американское название « колумбий » . [28] [29] [30] [31]
Ниобий — блестящий , серый, пластичный , парамагнитный металл 5-й группы таблицы Менделеева ( см. таблицу) с электронной конфигурацией в крайних оболочках , нетипичной для 5-й группы. Аналогичные нетипичные конфигурации встречаются в окрестностях рутения (44), родия. (45) и палладий (46).
Хотя считается, что он имеет объемно-центрированную кубическую кристаллическую структуру от абсолютного нуля до точки плавления, измерения теплового расширения с высоким разрешением вдоль трех кристаллографических осей обнаруживают анизотропию, несовместимую с кубической структурой. [32] Поэтому ожидаются дальнейшие исследования и открытия в этой области.
Ниобий становится сверхпроводником при криогенных температурах. При атмосферном давлении он имеет самую высокую критическую температуру среди элементарных сверхпроводников — 9,2 К. [33] Ниобий имеет наибольшую глубину магнитного проникновения среди всех элементов. [33] Кроме того, это один из трех элементарных сверхпроводников типа II , наряду с ванадием и технецием . Сверхпроводящие свойства сильно зависят от чистоты металлического ниобия. [34]
В очень чистом виде он сравнительно мягкий и пластичный, но примеси делают его более твердым. [35]
Металл имеет низкое сечение захвата тепловых нейтронов ; [36] таким образом, он используется в ядерной промышленности, где желательны структуры, прозрачные для нейтронов. [37]
Металл приобретает синеватый оттенок при длительном воздействии воздуха при комнатной температуре. [38] Несмотря на высокую температуру плавления в элементарной форме (2468 °C), он менее плотен, чем другие тугоплавкие металлы . Кроме того, он устойчив к коррозии, обладает свойствами сверхпроводимости и образует диэлектрические оксидные слои.
Ниобий немного менее электроположителен и более компактен, чем его предшественник в периодической таблице, цирконий , тогда как он практически идентичен по размеру более тяжелым атомам тантала в результате сжатия лантаноидов . [35] В результате химические свойства ниобия очень похожи на свойства тантала, который в периодической таблице располагается сразу после ниобия . [17] Хотя его коррозионная стойкость не такая выдающаяся, как у тантала, более низкая цена и большая доступность делают ниобий привлекательным для менее требовательных применений, таких как футеровка чанов на химических заводах. [35]
Ниобий в земной коре состоит из одного стабильного изотопа 93 Nb . [39] К 2003 году было синтезировано как минимум 32 радиоизотопа с атомной массой от 81 до 113. Наиболее стабильным является 92 Nb с периодом полураспада 34,7 миллиона лет. Одним из наименее стабильных является 113 Nb; расчетный период полураспада 30 миллисекунд. Изотопы, более легкие, чем стабильный 93 Nb, имеют тенденцию к β + -распаду , а более тяжелые — к β - распаду, за некоторыми исключениями. 81 Nb, 82 Nb и 84 Nb имеют незначительные пути распада β + -задержанной эмиссии протонов , 91 Nb распадается за счет захвата электронов и эмиссии позитронов , а 92 Nb распадается как за счет β +, так и β - распада. [39]
Описано не менее 25 ядерных изомеров с атомной массой от 84 до 104. В этом диапазоне только 96 Nb, 101 Nb и 103 Nb не имеют изомеров. Наиболее стабильным изомеров ниобия является 93m Nb с периодом полураспада 16,13 года. Наименее стабильным изомером является 84m Nb с периодом полураспада 103 нс. Все изомеры ниобия распадаются путем изомерного перехода или бета-распада, за исключением 92m1 Nb, который имеет незначительную ветвь электронного захвата. [39]
Ниобий, по оценкам, является 34-м по распространенности элементом в земной коре с содержанием 20 частей на миллион . [40] Некоторые полагают, что его распространенность на Земле намного больше, и что высокая плотность элемента сконцентрировала его в ядре Земли. [29] Свободный элемент не встречается в природе, но ниобий встречается в сочетании с другими элементами в минералах. [35] Минералы, содержащие ниобий, часто также содержат тантал. Примеры включают колумбит ( (Fe,Mn)Nb 2 O 6 ) и колумбит-танталит (или колтан , (Fe,Mn)(Ta,Nb) 2 O 6 ). [41] Минералы колумбит-танталит (наиболее распространенными видами являются колумбит-(Fe) и танталит-(Fe), где «-(Fe)» - это суффикс Левинсона, указывающий на преобладание железа над другими элементами, такими как марганец [42] [43] [44] [45] ), которые чаще всего встречаются в качестве акцессорных минералов в пегматитовых интрузиях и в щелочных интрузивных породах . Реже встречаются ниобаты кальция , урана , тория и редкоземельных элементов . Примерами таких ниобатов являются пирохлор ( (Na,Ca) 2 Nb 2 O 6 (OH,F) ) (ныне название группы, относительно распространенным примером является, например, фторкальциопирохлор [44] [45] [46] [47] ] [48] ) и эвксенит (правильно названный эвксенит-(Y) [44] [45] [49] ) ( (Y,Ca,Ce,U,Th)(Nb,Ta,Ti) 2 O 6 ). Эти крупные месторождения ниобия обнаружены в связи с карбонатитами (карбонатно - силикатными магматическими породами ) и в составе пирохлора. [50]
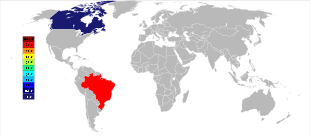
Три крупнейших в настоящее время разрабатываемых месторождения пирохлора, два в Бразилии и одно в Канаде, были обнаружены в 1950-х годах и до сих пор являются основными производителями ниобиевых минеральных концентратов. [17] Крупнейшее месторождение расположено в пределах карбонатитовой интрузии в Араше , штат Минас-Жерайс , Бразилия, принадлежащей компании CBMM ( Companhia Brasileira de Metalurgia e Mineração ); Другое действующее месторождение в Бразилии расположено недалеко от Каталана , штат Гояс , и принадлежит China Molybdenum , также расположено в пределах карбонатитовой интрузии. [51] Вместе эти две шахты производят около 88% мировых поставок. [52] Бразилия также имеет большое, но еще неразработанное месторождение недалеко от Сан-Габриэль-да-Кашуэйра , штат Амазонас , а также несколько более мелких месторождений, особенно в штате Рорайма . [52] [53]
Третьим по величине производителем ниобия является карбонатитовый рудник Ниобек в Сент-Оноре , недалеко от Чикутими , Квебек , Канада, принадлежащий Magris Resources. [54] Он производит от 7% до 10% мировых поставок. [51] [52]
После отделения от остальных минералов получают смешанные оксиды тантала Ta 2 O 5 и ниобия Nb 2 O 5 . Первым этапом обработки является реакция оксидов с плавиковой кислотой : [41]
Первое разделение в промышленном масштабе, разработанное швейцарским химиком де Мариньяком , использует различную растворимость сложных фторидов ниобия и тантала , моногидрата оксипентафторниобата дикалия ( K 2 [NbOF 5 ]·H 2 O ) и гептафторотанталата дикалия ( K 2 [TaF 7 ]). ) в воде. Более новые процессы используют жидкостную экстракцию фторидов из водного раствора органическими растворителями , такими как циклогексанон . [41] Комплексные фториды ниобия и тантала экстрагируются отдельно из органического растворителя водой и либо осаждаются добавлением фторида калия с образованием комплекса фторида калия, либо осаждаются аммиаком в виде пятиокиси: [55]
С последующим:
Для восстановления до металлического ниобия используется несколько методов . Электролиз расплавленной смеси K 2 [ NbOF 5 ] и хлорида натрия является одним из них ; другой — восстановление фторида натрием . С помощью этого метода можно получить ниобий относительно высокой чистоты. В крупномасштабном производстве Nb 2 O 5 восстанавливают водородом или углеродом. [55] В алюминотермической реакции смесь оксидов железа и оксидов ниобия реагирует с алюминием :
Для усиления реакции добавляются небольшие количества окислителей, таких как нитрат натрия . В результате получаются оксид алюминия и феррониобий — сплав железа и ниобия, используемый в производстве стали. [56] [57] Феррониобий содержит от 60 до 70% ниобия. [51] Без оксида железа для производства ниобия используется алюминотермический процесс. Дальнейшая очистка необходима для достижения класса сверхпроводящих сплавов. Электронно-лучевая плавка в вакууме — это метод, используемый двумя основными поставщиками ниобия. [58] [59]
По состоянию на 2013 год компания CBMM[обновлять] из Бразилии контролировала 85 процентов мирового производства ниобия. [60] По оценкам Геологической службы США , добыча увеличилась с 38 700 тонн в 2005 году до 44 500 тонн в 2006 году. [61] [62] Мировые ресурсы оцениваются в 4,4 миллиона тонн. [62] За десятилетний период с 1995 по 2005 год производство увеличилось более чем вдвое, начиная с 17 800 тонн в 1995 году . [63] В период с 2009 по 2011 год производство оставалось стабильным на уровне 63 000 тонн в год, [64] с небольшим снижение в 2012 году до всего лишь 50 000 тонн в год. [65]
Меньшие количества обнаружены на месторождении Каньика в Малави ( рудник Каньика ).
Во многом ниобий похож на тантал и цирконий . Он реагирует с большинством неметаллов при высоких температурах; с фтором при комнатной температуре; с хлором при 150°С и водородом при 200° С ; и с азотом при 400 °C, с продуктами, которые часто являются межузельными и нестехиометрическими. [35] Металл начинает окисляться на воздухе при температуре 200° С . [55] Он устойчив к коррозии под действием кислот, включая царскую водку , соляную , серную , азотную и фосфорную кислоты . [35] Ниобий подвергается воздействию горячей концентрированной серной кислоты, плавиковой кислоты и смесей плавиковой/азотной кислот. Он также подвергается воздействию горячих насыщенных растворов гидроксидов щелочных металлов.
Хотя ниобий проявляет все формальные степени окисления от +5 до –1, в наиболее распространенных соединениях ниобий находится в состоянии +5. [35] Характерно, что соединения в степени окисления менее 5+ демонстрируют связь Nb – Nb. В водных растворах ниобий проявляет только степень окисления +5. Он также легко склонен к гидролизу и плохо растворим в разбавленных растворах соляной , серной , азотной и фосфорной кислот из-за осаждения водного оксида Nb. [58] Nb(V) также мало растворим в щелочных средах из-за образования растворимых полиоксониобатов. [69] [70]
Ниобий образует оксиды в степенях окисления +5 ( Nb 2 O 5 ), [71] +4 ( NbO 2 ) и более редкой степени окисления +2 ( NbO ). [72] Наиболее распространенным является пятиокись, предшественник почти всех соединений и сплавов ниобия. [55] [73] Ниобаты образуются путем растворения пентоксида в основных растворах гидроксидов или плавления его в оксидах щелочных металлов. Примерами являются ниобат лития ( LiNbO 3 ) и ниобат лантана ( LaNbO 4 ). Ниобат лития представляет собой тригонально искаженную перовскитоподобную структуру, тогда как ниобат лантана содержит одиночный NbO. 3−
4ионы. [55] Известен также слоистый сульфид ниобия ( NbS 2 ). [35]
Материалы могут быть покрыты тонкой пленкой оксида ниобия (V) химическим осаждением из паровой фазы или процессами осаждения атомного слоя , полученными путем термического разложения этоксида ниобия (V) при температуре выше 350 ° C. [74] [75]


Ниобий образует галогениды в степенях окисления +5 и +4, а также разнообразные субстехиометрические соединения . [55] [58] Пентагалогениды ( NbX
5) имеют октаэдрические центры Nb. Пентафторид ниобия ( NbF 5 ) представляет собой белое твердое вещество с температурой плавления 79,0 °C, а пентахлорид ниобия ( NbCl 5 ) желтого цвета (см. изображение справа) с температурой плавления 203,4 °C. Оба гидролизуются с образованием оксидов и оксигалогенидов, таких как NbOCl 3 . Пентахлорид представляет собой универсальный реагент, используемый для получения металлоорганических соединений, таких как дихлорид ниобоцена ( (C
5ЧАС
5)
2NbCl
2). [76] Тетрагалогениды ( NbX
4) — полимеры темного цвета со связями Nb-Nb; например, черный гигроскопичный тетрафторид ниобия ( NbF 4 ) и коричневый тетрахлорид ниобия ( NbCl 4 ).
Анионные галогениды ниобия хорошо известны, отчасти благодаря кислотности Льюиса пентагалогенидов. Наиболее важным является [NbF 7 ] 2- , промежуточный продукт при выделении Nb и Та из руд. [41] Этот гептафторид имеет тенденцию образовывать оксопентафторид легче, чем соединение тантала. Другие галогенидные комплексы включают октаэдрический [ NbCl 6 ] - :
Как и в случае с другими металлами с низкими атомными номерами, известно множество восстановленных галогенидных кластерных ионов, ярким примером которых является [ Nb 6 Cl 18 ] 4- . [77]
Другие бинарные соединения ниобия включают нитрид ниобия (NbN), который становится сверхпроводником при низких температурах и используется в детекторах инфракрасного света. [78] Основным карбидом ниобия является NbC , чрезвычайно твердый , тугоплавкий керамический материал, коммерчески используемый в насадках для режущих инструментов .

Из 44 500 тонн ниобия, добытого в 2006 году, около 90% было использовано в производстве высококачественной конструкционной стали. Второе по величине применение — суперсплавы . [79] Сверхпроводники и электронные компоненты из ниобиевых сплавов составляют очень небольшую долю мирового производства. [79]
Ниобий является эффективным микролегирующим элементом стали, в составе которого образуется карбид и нитрид ниобия . [29] Эти соединения улучшают измельчение зерна и замедляют рекристаллизацию и дисперсионное твердение . Эти эффекты, в свою очередь, повышают ударную вязкость , прочность , формуемость и свариваемость . [29] В микролегированных нержавеющих сталях содержание ниобия является небольшим (менее 0,1%) [80], но важным дополнением к высокопрочным низколегированным сталям , которые широко используются в конструкции современных автомобилей. [29] Ниобий иногда используется в значительно больших количествах для изготовления высокоизносостойких деталей машин и ножей, вплоть до 3% в нержавеющей стали Crucible CPM S110V. [81]
Эти же ниобиевые сплавы часто используются при строительстве трубопроводов. [82] [83]

Количество ниобия используется в суперсплавах на основе никеля, кобальта и железа в пропорциях до 6,5% [80] для таких применений, как детали реактивных двигателей , газовые турбины , узлы ракет, системы турбонаддува, жаростойкость и сгорание. оборудование. Ниобий выделяет упрочняющую γ''-фазу в зеренной структуре суперсплава. [84]
Одним из примеров суперсплава является Inconel 718 , состоящий примерно из 50% никеля , 18,6% хрома , 18,5% железа , 5% ниобия, 3,1% молибдена , 0,9% титана и 0,4% алюминия . [85] [86]
Эти суперсплавы использовались, например, в перспективных системах планера программы Gemini . Другой ниобиевый сплав [ необходимы разъяснения ] использовался для сопла сервисного модуля Apollo . Поскольку ниобий окисляется при температуре выше 400 °C, для этих применений необходимо защитное покрытие, чтобы предотвратить хрупкость сплава . [87]
Сплав C-103 был разработан в начале 1960-х годов совместно Wah Chang Corporation и Boeing Co. DuPont , Union Carbide Corp., General Electric Co. и несколькими другими компаниями одновременно разрабатывали сплавы на основе Nb , во многом вызванные холодной войной и Космическая гонка . Он состоит из 89% ниобия, 10% гафния и 1% титана и используется для сопел жидкостных ракетных двигателей , таких как главный двигатель лунных модулей Аполлона . [87]
Реакционная способность ниобия с кислородом требует работы с ним в вакууме или инертной атмосфере , что значительно увеличивает стоимость и сложность производства. Вакуумно-дуговой переплав (ВДП) и электронно-лучевая плавка (ЭЛП), новые для того времени процессы, позволили разработать ниобий и другие химически активные металлы. Проект, в результате которого был получен C-103, начался в 1959 году с 256 экспериментальных ниобиевых сплавов «серии C» ( C , возможно, возникший из колумбия ), которые можно было плавить в виде пуговиц и скатывать в листы . Корпорация Wah Chang имела запасы гафния , очищенного из циркониевых сплавов ядерного качества , которые она хотела использовать в коммерческих целях. Наилучшим сочетанием формуемости и жаропрочных свойств обладал 103-й экспериментальный состав сплавов серии С – Nb-10Hf-1Ti. Ва Чанг изготовил первую 500-фунтовую плавку C-103 в 1961 году, от слитка до листа, используя EBM и VAR. Предполагаемые области применения включали газотурбинные двигатели и жидкометаллические теплообменники . Конкурирующие ниобиевые сплавы той эпохи включали FS85 (Nb-10W-28Ta-1Zr) от Fansteel Metallurgical Corp. , Cb129Y (Nb-10W-10Hf-0,2Y) от Wah Chang и Boeing, Cb752 (Nb-10W-2,5Zr) от Wah Chang и Boeing, Cb752 (Nb-10W-2,5Zr) от Wah Chang. Union Carbide и Nb1Zr от Superior Tube Co. [87]

Сопло двигателей серии Merlin Vacuum , разработанных SpaceX для верхней ступени ракеты Falcon 9, изготовлено из ниобиевого сплава [ нужны разъяснения ] . [88]

Ниобий-германий ( Nb
3Ge ), ниобий–олово ( Nb
3Sn ), а также ниобий-титановые сплавы используются в качестве сверхпроводящего провода II рода для сверхпроводящих магнитов . [89] [90] Эти сверхпроводящие магниты используются в приборах магнитно-резонансной томографии и ядерного магнитного резонанса, а также в ускорителях частиц . [91] Например, Большой адронный коллайдер использует 600 тонн сверхпроводящих нитей, а Международный термоядерный экспериментальный реактор использует примерно 600 тонн нитей Nb 3 Sn и 250 тонн нитей NbTi. [92] Только в 1992 году было построено клинических систем магнитно-резонансной томографии на сумму более 1 миллиарда долларов США с использованием ниобий-титановой проволоки. [22]

Сверхпроводящие радиочастотные (SRF) резонаторы, используемые в лазерах на свободных электронах FLASH (результат отмененного проекта линейного ускорителя TESLA) и XFEL , изготовлены из чистого ниобия. [93] Команда криомодулей в Фермилабе использовала ту же технологию SRF, что и в проекте FLASH, для разработки девятиэлементных SRF-резонаторов с частотой 1,3 ГГц, изготовленных из чистого ниобия. Полости будут использоваться в 30-километровом (19 милях) линейном ускорителе частиц Международного линейного коллайдера . [94] Та же технология будет использоваться в LCLS-II в Национальной ускорительной лаборатории SLAC и в PIP-II в Фермилаб. [95]
Высокая чувствительность сверхпроводящих болометров из нитрида ниобия делает их идеальным детектором электромагнитного излучения в ТГц диапазоне частот. Эти детекторы были протестированы на Субмиллиметровом телескопе , Южнополярном телескопе , Лабораторном телескопе-приемнике и на APEX , и теперь используются в приборе HIFI на борту Космической обсерватории Гершель . [96]
Ниобат лития , который является сегнетоэлектриком , широко используется в мобильных телефонах и оптических модуляторах , а также для производства устройств на поверхностных акустических волнах . Он принадлежит к сегнетоэлектрикам структуры ABO 3 , таким как танталат лития и титанат бария . [97] Ниобиевые конденсаторы доступны в качестве альтернативы танталовым конденсаторам , [98] но танталовые конденсаторы по-прежнему преобладают. Ниобий добавляется в стекло для получения более высокого показателя преломления , что позволяет сделать корректирующие стекла тоньше и легче .
Ниобий и некоторые ниобиевые сплавы физиологически инертны и гипоаллергенны . По этой причине ниобий используется в протезах и имплантатах, таких как кардиостимуляторы. [99] Ниобий, обработанный гидроксидом натрия, образует пористый слой, который способствует остеоинтеграции . [100]
Подобно титану, танталу и алюминию, ниобий можно нагревать и анодировать («реактивное анодирование металлов ») для получения широкого спектра переливающихся цветов для ювелирных изделий, [101] [102] где его гипоаллергенные свойства весьма желательны. [103]
Ниобий используется в качестве драгоценного металла в памятных монетах, часто с серебром или золотом. Например, начиная с 2003 года в Австрии производилась серия серебряных ниобиевых монет евро ; Цвет этих монет создается за счет дифракции света тонким слоем анодированного оксида. [104] В 2012 году доступны десять монет с изображением самых разных цветов в центре монеты: синего, зеленого, коричневого, фиолетового, фиолетового или желтого. Еще двумя примерами являются австрийская памятная монета номиналом 25 евро в честь 150-летия Земмерингской альпийской железной дороги 2004 года и австрийская памятная монета стоимостью 25 евро в 2006 году для Европейской спутниковой навигации . [106] Австрийский монетный двор выпустил для Латвии аналогичную серию монет, начиная с 2004 года, [107] и еще одну в 2007 году. [108] В 2011 году Королевский монетный двор Канады начал производство монеты из серебра и ниобия стоимостью 5 долларов под названием « Луна охотника». [109] , в котором ниобий избирательно окислялся, создавая таким образом уникальную отделку, в которой не бывает двух одинаковых монет.
Уплотнения дугогасительной трубки натриевых ламп высокого давления изготавливаются из ниобия, иногда легированного 1% циркония ; ниобий имеет очень похожий коэффициент теплового расширения, соответствующий керамике дуговой трубки из спеченного оксида алюминия , полупрозрачному материалу, который устойчив к химическому воздействию или восстановлению под действием горячего жидкого натрия и паров натрия, содержащихся внутри операционной лампы. [110] [111] [112]
Ниобий используется в стержнях для дуговой сварки некоторых стабилизированных марок нержавеющей стали [113] и в анодах систем катодной защиты некоторых резервуаров для воды, которые затем обычно покрываются платиной. [114] [115]
Ниобий используется для изготовления высоковольтного провода модуля рецептора частиц солнечной короны солнечного зонда Parker . [116]
Были проведены исследования, позволяющие использовать катализаторы на основе ниобия для переработки полиэтилентерефталата (ПЭТ). [117] [118]
Ниобий не имеет известной биологической роли. Хотя ниобиевая пыль раздражает глаза и кожу и представляет потенциальную опасность возгорания, элементарный ниобий в более широком масштабе физиологически инертен (и, следовательно, гипоаллергенен) и безвреден. Он часто используется в ювелирных изделиях и был протестирован для использования в некоторых медицинских имплантатах. [119] [120]
Кратковременное и долговременное воздействие ниобатов и хлорида ниобия, двух водорастворимых химических веществ, было протестировано на крысах. У крыс, получавших однократную инъекцию пентахлорида ниобия или ниобатов, средняя летальная доза (LD 50 ) составляет от 10 до 100 мг/кг. [121] [122] [123] При пероральном введении токсичность ниже; исследование на крысах показало LD 50 после семи дней приема 940 мг/кг. [121]
{{cite book}}: |journal=игнорируется ( помощь ){{cite book}}: |journal=игнорируется ( помощь ){{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка ){{cite book}}: |journal=игнорируется ( помощь ){{cite book}}: |journal=игнорируется ( помощь )