Нобелий — синтетический химический элемент ; у него есть символ No и атомный номер 102. Он назван в честь Альфреда Нобеля , изобретателя динамита и благотворителя науки. Радиоактивный металл , это десятый трансурановый элемент и предпоследний член ряда актинидов . Как и все элементы с атомным номером более 100, нобелий можно производить только в ускорителях частиц путем бомбардировки более легких элементов заряженными частицами. Известно, что всего существует двенадцать изотопов нобелия ; наиболее стабильным является 259 No с периодом полураспада 58 минут, но более короткоживущий 255 No (период полураспада 3,1 минуты) чаще всего используется в химии, поскольку его можно производить в больших масштабах.
Химические эксперименты подтвердили, что нобелий ведет себя как более тяжелый гомолог иттербия в таблице Менделеева . Химические свойства нобелия до конца не известны: в основном они известны только в водном растворе . До открытия нобелия было предсказано, что он будет демонстрировать стабильную степень окисления +2 , а также состояние +3, характерное для других актинидов; эти предсказания позже подтвердились, поскольку состояние +2 гораздо более стабильно, чем состояние +3 в водном растворе , и нобелий трудно удерживать в состоянии +3.
В 1950-х и 1960-х годах многие заявления об открытии нобелия поступали из лабораторий Швеции , Советского Союза и США . Хотя шведские учёные вскоре отказались от своих претензий, приоритет открытия и, следовательно, наименование элемента оспаривались между советскими и американскими учёными. Лишь в 1997 году Международный союз теоретической и прикладной химии (IUPAC) приписал советской команде открытие. Несмотря на это, нобелий, шведское предложение, было сохранено в качестве названия элемента из-за его давнего использования в литературе.

Сверхтяжелое [b] атомное ядро создается в результате ядерной реакции, объединяющей два других ядра неравного размера [c] в одно; грубо говоря, чем более неравны два ядра по массе, тем больше вероятность того, что они вступят в реакцию. [11] Материал, состоящий из более тяжелых ядер, превращается в мишень, которая затем бомбардируется пучком более легких ядер. Два ядра могут слиться в одно только в том случае, если они приблизятся друг к другу достаточно близко; Обычно ядра (все положительно заряженные) отталкивают друг друга из-за электростатического отталкивания . Сильное взаимодействие может преодолеть это отталкивание, но только на очень небольшом расстоянии от ядра; Таким образом, ядра пучка сильно ускоряются , чтобы сделать такое отталкивание незначительным по сравнению со скоростью ядра пучка. [12] Энергия, приложенная к ядрам пучка для их ускорения, может заставить их достичь скорости, составляющей одну десятую скорости света . Однако если приложить слишком много энергии, ядро пучка может развалиться. [12]
Одного сближения недостаточно для слияния двух ядер: когда два ядра сближаются друг с другом, они обычно остаются вместе примерно 10–20 секунд , а затем расходятся (не обязательно в том же составе, что и до реакции), а не образуют одно ядро. [12] [13] Это происходит потому, что во время попытки образования одного ядра электростатическое отталкивание разрывает образующееся ядро. [12] Каждая пара мишени и пучка характеризуется своим поперечным сечением — вероятностью того, что синтез произойдет, если два ядра сблизятся друг с другом, выраженной через поперечную площадь, на которую должна попасть падающая частица, чтобы произошел синтез. . [d] Этот синтез может произойти в результате квантового эффекта, при котором ядра могут туннелировать за счет электростатического отталкивания. Если два ядра смогут оставаться рядом после этой фазы, множественные ядерные взаимодействия приведут к перераспределению энергии и энергетическому равновесию. [12]
В результате слияния возникает возбужденное состояние [16] , называемое составным ядром , и поэтому оно очень нестабильно. [12] Чтобы достичь более стабильного состояния, временное слияние может делиться без образования более стабильного ядра. [17] Альтернативно, составное ядро может выбросить несколько нейтронов , которые унесут энергию возбуждения; если последнего недостаточно для выброса нейтронов, слияние приведет к образованию гамма-излучения . Это происходит примерно через 10–16 секунд после первоначального ядерного столкновения и приводит к созданию более стабильного ядра. [17] В определении Объединенной рабочей группы IUPAC/IUPAP (JWP) говорится, что химический элемент может быть признан открытым только в том случае, если его ядро не распалось в течение 10–14 секунд . Это значение было выбрано в качестве оценки того, сколько времени требуется ядру, чтобы приобрести внешние электроны и, таким образом, проявить свои химические свойства. [18] [э]
Пучок проходит через мишень и достигает следующей камеры — сепаратора; если образуется новое ядро, оно уносится этим лучом. [20] В сепараторе вновь образовавшееся ядро отделяется от других нуклидов (из исходного пучка и любых других продуктов реакции) [f] и передается в детектор с поверхностным барьером , который останавливает ядро. Отмечается точное место предстоящего воздействия на детекторе; также отмечена его энергия и время прибытия. [20] Передача занимает около 10-6 секунд ; Чтобы быть обнаруженным, ядро должно выжить так долго. [23] Ядро записывается снова, как только регистрируется его распад, и измеряются местоположение, энергия и время распада. [20]
Стабильность ядра обеспечивается сильным взаимодействием. Однако его радиус действия очень короток; по мере увеличения размеров ядра его влияние на самые внешние нуклоны ( протоны и нейтроны) ослабевает. При этом ядро разрывается за счет электростатического отталкивания между протонами, и его радиус действия не ограничен. [24] Полная энергия связи , обеспечиваемая сильным взаимодействием, линейно возрастает с числом нуклонов, тогда как электростатическое отталкивание увеличивается пропорционально квадрату атомного номера, т.е. последнее растет быстрее и становится все более важным для тяжелых и сверхтяжелых ядер. [25] [26] Таким образом, теоретически предсказаны сверхтяжелые ядра [27] и до сих пор наблюдалось [28] преимущественное распад через моды распада, которые вызваны таким отталкиванием: альфа-распад и спонтанное деление . [g] Почти все альфа-излучатели имеют более 210 нуклонов, [30] а самый легкий нуклид, в первую очередь подвергающийся спонтанному делению, имеет 238. [31] В обоих режимах распада ядра сдерживаются соответствующими энергетическими барьерами для каждого режима, но они могут быть проложен через туннель. [25] [26]

Альфа-частицы обычно образуются в результате радиоактивного распада, поскольку масса альфа-частицы на нуклон достаточно мала, чтобы оставить некоторую энергию, которую альфа-частица может использовать в качестве кинетической энергии для выхода из ядра. [33] Спонтанное деление вызвано электростатическим отталкиванием, разрывающим ядро на части и производящим различные ядра в разных случаях деления одинаковых ядер. [26] По мере увеличения атомного номера спонтанное деление быстро становится более важным: частичные периоды полураспада спонтанного деления уменьшаются на 23 порядка величины от урана (элемент 92) до нобелия (элемент 102), [34] и на 30 порядков величины. от тория (90-й элемент) до фермия (100-й элемент). [35] Таким образом, более ранняя модель жидкой капли предполагала, что спонтанное деление будет происходить почти мгновенно из-за исчезновения барьера деления для ядер с числом около 280 нуклонов. [26] [36] Более поздняя модель ядерной оболочки предположила, что ядра, содержащие около 300 нуклонов, образуют остров стабильности , в котором ядра будут более устойчивы к спонтанному делению и в первую очередь будут подвергаться альфа-распаду с более длительным периодом полураспада. [26] [36] Последующие открытия показали, что предсказанный остров может находиться дальше, чем первоначально предполагалось; они также показали, что ядра, промежуточные между долгоживущими актинидами и предсказанным островом, деформируются и приобретают дополнительную стабильность за счет оболочечных эффектов. [37] Эксперименты с более легкими сверхтяжелыми ядрами, [38] , а также с ядрами, расположенными ближе к ожидаемому острову, [34] показали большую, чем предполагалось ранее, устойчивость к спонтанному делению, показывая важность оболочечных эффектов на ядрах. [час]
Альфа-распад регистрируется по испускаемым альфа-частицам, а продукты распада легко определить еще до фактического распада; если в результате такого распада или серии последовательных распадов образуется известное ядро, можно легко определить исходный продукт реакции. [i] (То, что все распады внутри цепочки распада действительно были связаны друг с другом, устанавливается по расположению этих распадов, которое должно находиться в одном и том же месте.) [20] Известное ядро можно распознать по специфическим характеристикам распада. он подвергается воздействию энергии распада (или, точнее, кинетической энергии испускаемой частицы). [j] Однако в результате спонтанного деления в качестве продуктов образуются различные ядра, поэтому исходный нуклид невозможно определить по его дочерним элементам. [к]
Таким образом, информация, доступная физикам, стремящимся синтезировать сверхтяжелый элемент, — это информация, собранная на детекторах: местоположение, энергия и время прибытия частицы в детектор, а также время ее распада. Физики анализируют эти данные и стремятся прийти к выводу, что это действительно было вызвано новым элементом и не могло быть вызвано другим нуклидом, чем заявленный. Часто предоставленных данных недостаточно для вывода о том, что новый элемент определенно был создан, и нет другого объяснения наблюдаемым эффектам; допущены ошибки в интерпретации данных. [л]
Открытие элемента 102 было сложным процессом, о нем заявили группы из Швеции , США и Советского Союза . Первое полное и неопровержимое сообщение о его обнаружении поступило только в 1966 году из Объединенного института ядерных исследований в Дубне (тогда в Советском Союзе). [49]
Первое заявление об открытии элемента 102 было сделано физиками Нобелевского института в Швеции в 1957 году. Команда сообщила, что они бомбардировали мишень кюрия ионами углерода-13 в течение двадцати пяти часов с получасовыми интервалами. Между бомбардировками на мишени проводили ионообменную химию. Двенадцать из пятидесяти бомбардировок содержали образцы, испускающие альфа-частицы с энергией (8,5 ± 0,1) МэВ , которые находились в каплях, элюированных раньше, чем фермий (атомный номер Z = 100) и калифорний ( Z = 98). Сообщаемый период полураспада составлял 10 минут и был присвоен либо 251 102, либо 253 102, хотя вероятность того, что наблюдаемые альфа-частицы произошли от предположительно короткоживущего изотопа менделевия ( Z = 101), созданного в результате электронного захвата элемента 102, была не исключено. [49] Группа предложила новому элементу название нобелий (Нет), [50] [51] которое было немедленно одобрено ИЮПАК, [52] решение, которое группа из Дубны охарактеризовала в 1968 году как поспешное. [53]
В 1958 году ученые Национальной лаборатории Лоуренса Беркли повторили эксперимент. Команда Беркли, состоящая из Альберта Гиорсо , Гленна Т. Сиборга , Джона Р. Уолтона и Торбьёрна Сиккеланда , использовала новый линейный ускоритель тяжелых ионов (HILAC) для бомбардировки мишени из кюрия (95% 244 См и 5% 246 См) Ионы 13 C и 12 C. Они не смогли подтвердить активность в 8,5 МэВ, о которой заявили шведы, но вместо этого смогли обнаружить распад фермия-250, предположительно дочернего элемента 254 102 (полученного из кюрия-246), который имел кажущийся период полураспада ~3 с. Вероятно, это определение также было ошибочным, поскольку более поздние работы в Дубне в 1963 году показали, что период полураспада 254 No значительно больше (около 50 с). Более вероятно, что наблюдаемые альфа-распады происходили не от элемента 102, а от 250m Фм. [49]
В 1959 году шведская группа попыталась объяснить неспособность команды из Беркли обнаружить элемент 102 в 1958 году, утверждая, что они его открыли. Однако более поздние работы показали, что не существует изотопов нобелия легче, чем 259 No (в шведских экспериментах не могло быть получено более тяжелых изотопов) с периодом полураспада более 3 минут, и что результаты шведской группы, скорее всего, получены из тория -225. , который имеет период полураспада 8 минут и быстро подвергается тройному альфа-распаду с образованием полония -213, энергия распада которого составляет 8,53612 МэВ. Этой гипотезе придает вес тот факт, что торий-225 можно легко получить в ходе используемой реакции и его нельзя выделить используемыми химическими методами. Более поздние работы с нобелием также показали, что двухвалентное состояние более стабильно, чем трехвалентное, и, следовательно, образцы, испускающие альфа-частицы, не могли содержать нобелий, поскольку двухвалентный нобелий не элюировался бы с другими трехвалентными актинидами. [49] Таким образом, шведская группа позже отказалась от своих претензий и связала эту деятельность с фоновыми эффектами. [52]
В 1959 году группа продолжила свои исследования и заявила, что им удалось произвести изотоп, который распадался преимущественно за счет испускания альфа-частицы с энергией 8,3 МэВ, с периодом полураспада 3 секунды и связанной с ней 30% ветвью спонтанного деления . Первоначально активность была присвоена номеру 254 102, но позже была изменена на 252 102. Однако они также отметили, что нет уверенности в том, что элемент 102 был произведен из-за сложных условий. [49] Команда Беркли решила принять для этого элемента предложенное шведской командой название «нобелий». [52]
Между тем в Дубне в 1958 и 1960 годах проводились эксперименты по синтезу и 102-го элемента. В первом эксперименте 1958 года плутоний-239 и -241 бомбардировали ионами кислорода-16 . Наблюдались некоторые альфа-распады с энергией чуть более 8,5 МэВ, и им было присвоено значение 251 252 253 102, хотя команда писала, что нельзя исключать образование изотопов из примесей свинца или висмута (которые не производят нобелий). Хотя более поздние эксперименты 1958 года показали, что новые изотопы могут быть получены из примесей ртути , таллия , свинца или висмута, ученые все еще придерживались своего вывода, что элемент 102 может быть получен в результате этой реакции, упомянув период полураспада менее 30 секунд и энергия распада (8,8 ± 0,5) МэВ. Позже эксперименты 1960 года доказали, что это были фоновые эффекты. Эксперименты 1967 года также снизили энергию распада до (8,6 ± 0,4) МэВ, но оба значения слишком высоки, чтобы соответствовать энергии распада 253 No или 254 No. [49] Позже в 1970 году, а затем в 1987 году группа из Дубны заявила, что эти результаты не убедительно. [49]
В 1961 году ученые Беркли заявили об открытии 103-го элемента в реакции калифорния с ионами бора и углерода. Они заявили о производстве изотопа 257 103, а также заявили, что синтезировали альфа-распадающийся изотоп элемента 102, который имел период полураспада 15 с и энергию альфа-распада 8,2 МэВ. Они присвоили это номеру 255 102, не указав причину назначения. Значения не согласуются с теми, которые сейчас известны для 255 No, хотя они согласуются с теми, которые сейчас известны для 257 No, и хотя этот изотоп, вероятно, сыграл роль в этом эксперименте, его открытие было безрезультатным. [49]
Работы над 102-м элементом продолжались и в Дубне, и в 1964 году там были проведены эксперименты по обнаружению дочерних альфа-распадов изотопов 102-го элемента путем синтеза 102-го элемента из реакции мишени из урана -238 с ионами неона . Продукты переносили по серебряной улавливающей фольге, подвергали химической очистке и обнаруживали изотопы 250 Fm и 252 Fm. Выход 252 Fm был интерпретирован как свидетельство того, что его родительский 256 102 также был синтезирован: поскольку было отмечено, что 252 Fm также может быть получен непосредственно в этой реакции путем одновременного испускания альфа-частицы с избыточными нейтронами, были предприняты шаги для обеспечить, чтобы 252 Фм не попадали прямо на улавливающую фольгу. Период полураспада, обнаруженный для 256 102, составил 8 с, что намного превышает более современное значение 1967 года (3,2 ± 0,2) с. [49] Дальнейшие эксперименты были проведены в 1966 году для 254 102 по реакциям 243 Am ( 15 N ,4n) 254 102 и 238 U( 22 Ne,6n) 254 102, установив период полураспада (50 ± 10) с. : в то время несоответствие между этим значением и более ранним значением Беркли не было понято, хотя более поздние работы доказали, что образование изомера 250m Fm было менее вероятным в экспериментах в Дубне, чем в экспериментах в Беркли. Оглядываясь назад, можно сказать, что результаты Дубны по 254 102, вероятно, были правильными и теперь могут считаться окончательным обнаружением элемента 102. [49]
Еще один очень убедительный эксперимент из Дубны был опубликован в 1966 году (хотя он был представлен в 1965 году), снова используя те же две реакции, в результате чего был сделан вывод, что 254 102 действительно имеет период полураспада, намного больший, чем 3 секунды, заявленные Беркли. [49] Более поздние работы, проведенные в 1967 году в Беркли и 1971 году в Национальной лаборатории Ок-Ридж, полностью подтвердили открытие элемента 102 и уточнили более ранние наблюдения. [52] В декабре 1966 года группа из Беркли повторила эксперименты в Дубне и полностью подтвердила их, а также использовала эти данные, чтобы окончательно правильно определить изотопы, которые они ранее синтезировали, но еще не могли идентифицировать в то время, и, таким образом, заявили, что обнаружили нобелий в 1958–1961 гг. [52]

В 1969 году группа из Дубны провела химические эксперименты с элементом 102 и пришла к выводу, что он ведет себя как более тяжелый гомолог иттербия . Российские учёные предложили название джолиотий (Jo) для нового элемента в честь недавно умершей Ирен Жолио-Кюри , создав споры по поводу названий элементов , которые не будут разрешены в течение нескольких десятилетий, при этом каждая группа будет использовать свои собственные предложенные имена. [52] [54]
В 1992 году рабочая группа IUPAC - IUPAP Transfermium (TWG) провела переоценку заявлений об открытии и пришла к выводу, что только работа в Дубне 1966 года правильно обнаружила и приписала распады ядрам с атомным номером 102 в то время. Таким образом, команда Дубны официально признана первооткрывателями нобелия, хотя не исключено, что он был обнаружен в Беркли в 1959 году . «бесполезная трата времени», а Дубна согласилась с решением ИЮПАК. [53]
В 1994 году в рамках попытки разрешения спора об именах элементов ИЮПАК ратифицировал названия элементов 101–109. Для элемента 102 было утверждено название « нобелий» («Нет») на том основании, что оно укоренилось в литературе в течение 30 лет и что память Альфреда Нобеля следует увековечивать таким образом. [55] Из-за протестов по поводу названий 1994 года, которые по большей части не уважали выбор первооткрывателей, последовал период комментариев, и в 1995 году ИЮПАК назвал элемент 102 флеровий (Fl) частью нового предложения в честь Георгия Флёрова или его одноименная Лаборатория ядерных реакций имени Флерова . [56] Это предложение также не было принято, и в 1997 году название нобелий было восстановлено. [55] Сегодня название флеровий с тем же символом относится к элементу 114 . [57]
В периодической таблице нобелий расположен справа от актинида менделевия , слева от актинида лоуренция и ниже лантаноида иттербия . Металлический нобелий еще не получен в больших количествах, и массовое получение в настоящее время невозможно. [59] Тем не менее, относительно его свойств был сделан ряд предсказаний и некоторые предварительные экспериментальные результаты. [59]
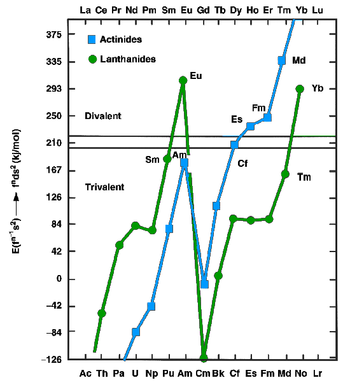
Лантаниды и актиниды в металлическом состоянии могут существовать как двухвалентные (например, европий и иттербий ), так и трехвалентные (большинство других лантаноидов) металлы. Первые имеют конфигурации f n s 2 , тогда как вторые имеют конфигурации f n −1 d 1 s 2 . В 1975 году Йоханссон и Розенгрен исследовали измеренные и предсказанные значения энергии когезии ( энтальпии кристаллизации) металлических лантаноидов и актинидов , как двухвалентных, так и трехвалентных металлов. [60] [61] Был сделан вывод, что увеличенной энергии связи конфигурации [Rn]5f 13 6d 1 7s 2 по сравнению с конфигурацией [Rn] 5f 14 7s 2 для нобелия недостаточно, чтобы компенсировать энергию, необходимую для продвижения одной 5f электрон на 6d, что верно и для очень поздних актинидов: таким образом, ожидалось, что эйнштейний , фермий , менделевий и нобелий будут двухвалентными металлами, хотя для нобелия это предсказание еще не подтвердилось. [60] Возрастающее преобладание двухвалентного состояния задолго до завершения актинидной серии объясняется релятивистской стабилизацией 5f-электронов, которая увеличивается с увеличением атомного номера: в результате этого нобелий является преимущественно двухвалентным, а не трехвалентным, в отличие от всех другие лантаноиды и актиниды. [62] В 1986 году было подсчитано, что металлический нобелий имеет энтальпию сублимации между 126 кДж/моль, значение, близкое к значениям для эйнштейния, фермия и менделевия и подтверждающее теорию о том, что нобелий образует двухвалентный металл. [59] Как и другие двухвалентные поздние актиниды (за исключением вновь трехвалентного лоуренсия), металлический нобелий должен иметь гранецентрированную кубическую кристаллическую структуру. [2] Металлический двухвалентный нобелий должен иметь металлический радиус около 197 мкм . [59] По прогнозам, температура плавления нобелия составит 800 ° C, то же значение, что и для соседнего элемента менделевия. [63] По прогнозам, его плотность составит около 9,9 ± 0,4 г/см 3 . [2]
Химия нобелия не полностью изучена и известна только в водном растворе, в котором он может принимать степени окисления +3 или +2 , причем последняя более стабильна. [50] До открытия нобелия в значительной степени ожидалось, что в растворе он будет вести себя так же, как и другие актиниды, с преобладанием трехвалентного состояния; однако Сиборг в 1949 году предсказал, что состояние +2 также будет относительно стабильным для нобелия, поскольку ион No 2+ будет иметь электронную конфигурацию основного состояния [Rn]5f 14 , включая стабильную заполненную оболочку 5f 14 . Прошло девятнадцать лет, прежде чем это предсказание подтвердилось. [64]
В 1967 году были проведены эксперименты по сравнению химического поведения нобелия с поведением тербия , калифорния и фермия . Все четыре элемента прореагировали с хлором , и образовавшиеся хлориды отложились вдоль трубки, по которой они переносились газом. Было обнаружено, что полученный хлорид нобелия сильно адсорбируется на твердых поверхностях, что доказывает, что он не очень летуч , как хлориды трех других исследованных элементов. Однако ожидалось, что и NoCl 2 , и NoCl 3 будут проявлять нелетучее поведение, и, следовательно, этот эксперимент не дал окончательных результатов относительно предпочтительной степени окисления нобелия. [64] Определение предпочтения нобелия к состоянию +2 пришлось отложить до следующего года, когда эксперименты по катионообменной хроматографии и соосаждению были проведены примерно на пятидесяти тысячах атомов 255 No, и было обнаружено, что он вел себя иначе, чем другие актиниды и многое другое. как двухвалентные щелочноземельные металлы . Это доказало, что в водном растворе нобелий наиболее устойчив в двухвалентном состоянии, когда отсутствуют сильные окислители . [64] Более поздние эксперименты в 1974 году показали, что нобелий элюируется щелочноземельными металлами, между Ca 2+ и Sr 2+ . [64] Нобелий — единственный известный элемент f-блока, для которого состояние +2 является наиболее распространенным и стабильным в водном растворе. Это происходит из-за большой энергетической щели между 5f- и 6d-орбиталями в конце актинидного ряда. [65]
Ожидается, что релятивистская стабилизация подоболочки 7s сильно дестабилизирует дигидрид нобелия NoH 2 , а релятивистская стабилизация спинора 7p 1/2 по спинору 6d 3/2 означает, что возбужденные состояния в атомах нобелия имеют вклады 7s и 7p вместо ожидаемый вклад 6d. Большие расстояния No–H в молекуле NoH 2 и значительный перенос заряда приводят к чрезвычайной ионности с дипольным моментом 5,94 Д для этой молекулы. Ожидается, что в этой молекуле нобелий будет проявлять поведение , подобное основной группе , в частности, действуя как щелочноземельный металл с конфигурацией валентной оболочки n s 2 и 5f-орбиталями, подобными ядру. [66]
Способность к комплексообразованию нобелия с хлорид -ионами наиболее близка к способности бария , который довольно слабо образует комплексы. [64] Его комплексообразующая способность с цитратом , оксалатом и ацетатом в водном растворе 0,5 М нитрата аммония находится между таковыми у кальция и стронция, хотя несколько ближе к таковой у стронция. [64]
Стандартный восстановительный потенциал пары E °(No 3+ → No 2+ ) оценивался в 1967 году в пределах от +1,4 до +1,5 В ; [64] Позже в 2009 году было обнаружено, что оно составляет всего около +0,75 В. [67] Положительное значение показывает, что № 2+ более стабилен, чем № 3+ , и что № 3+ является хорошим окислителем. Хотя указанные значения для E ° (No 2+ → No 0 ) и E ° (No 3+ → No 0 ) различаются в зависимости от источника, принятые стандартные оценки составляют -2,61 и -1,26 В. [64] Было предсказано что значение для пары E °(No 4+ → No 3+ ) будет +6,5 В. [64] Энергии Гиббса образования для No 3+ и No 2+ оцениваются в −342 и −480 кДж/ моль соответственно. [64]
Атом нобелия имеет 102 электрона. Ожидается, что они будут расположены в конфигурации [Rn]5f 14 7s 2 ( символ термина основного состояния 1 S 0 ), хотя экспериментальная проверка этой электронной конфигурации по состоянию на 2006 год еще не проводилась. Шестнадцать электронов в 5f и 7s подоболочки — валентные электроны . [59] При образовании соединений три валентных электрона могут быть потеряны, оставляя после себя ядро [Rn] 5f 13 : это соответствует тенденции, установленной другими актинидами с их электронными конфигурациями [Rn] 5f n в триположительном состоянии. Тем не менее, более вероятно, что теряются только два валентных электрона, оставляя после себя стабильное ядро [Rn]5f 14 с заполненной оболочкой 5f 14 . Первый потенциал ионизации нобелия был измерен в 1974 году и составил не более (6,65 ± 0,07) эВ на основании предположения, что электроны 7s будут ионизироваться раньше, чем электроны 5f; [68] это значение еще не уточнено из-за нехватки нобелия и высокой радиоактивности. [69] Ионный радиус гексакоордината и октакоордината № 3+ был предварительно оценен в 1978 году примерно в 90 и 102 пм соответственно; [64] экспериментально установлено, что ионный радиус No 2+ составляет от 100 пм до двух значащих цифр . [59] Энтальпия гидратации No 2+ рассчитана как 1486 кДж/моль. [64]
Известны четырнадцать изотопов нобелия с массовыми числами 248–260 и 262; все радиоактивны. [5] Кроме того, известны ядерные изомеры с массовыми числами 250, 251, 253 и 254. [70] [71] Из них самым долгоживущим изотопом является 259 No с периодом полураспада 58 минут, а самый длинный -живой изомер 251m No с периодом полураспада 1,7 секунды. [70] [71] Однако, согласно прогнозам, еще неоткрытый изотоп 261 No будет иметь еще более длительный период полураспада - 3 часа. [5] Кроме того, короткоживущий 255 No (период полураспада 3,1 минуты) чаще используется в химических экспериментах, поскольку его можно производить в больших количествах в результате облучения калифорния -249 ионами углерода-12 . [72] После 259 No и 255 No следующими наиболее стабильными изотопами нобелия являются 253 No (период полураспада 1,62 минуты), 254 No (51 секунда ), 257 No (25 секунд), 256 No (2,91 секунды) и 252. Нет (2,57 секунды). [72] [70] [71] Все остальные изотопы нобелия имеют период полураспада менее секунды, а самый короткоживущий известный изотоп нобелия ( 248 No) имеет период полураспада менее 2 микросекунд . [5] Изотоп 254 No особенно интересен теоретически, поскольку он находится в середине ряда вытянутых ядер от 231 Па до 279 Rg , а образование его ядерных изомеров (из которых известны два) контролируется протонными орбиталями , такими как как 2f 5/2 , которые располагаются чуть выше сферической оболочки протона; его можно синтезировать по реакции 208 Pb с 48 Ca. [73]
Периоды полураспада изотопов нобелия плавно возрастают от 250 No до 253 No. Однако при 254 No появляется провал , а за его пределами периоды полураспада четно-четных изотопов нобелия резко падают, поскольку доминирующим способом распада становится спонтанное деление. Например, период полураспада 256 No составляет почти три секунды, а у 258 No — всего 1,2 миллисекунды. [72] [70] [71] Это показывает, что в нобелии взаимное отталкивание протонов ограничивает область долгоживущих ядер в ряду актинидов . [74] Четно-нечетные изотопы нобелия в основном продолжают иметь более длительный период полураспада по мере увеличения их массового числа, с падением тенденции к 257 № [72] [70] [71]
Изотопы нобелия в основном производятся путем бомбардировки актинидных мишеней ( уран , плутоний , кюрий , калифорний или эйнштейний ), за исключением нобелия-262, который производится как дочерний элемент лоуренция-262. [72] Наиболее часто используемый изотоп, 255 No, может быть получен бомбардировкой кюрия -248 или калифорния-249 углеродом-12: последний метод более распространен. Облучение мишени из калифорния-249 массой 350 мкг / см -2 тремя триллионами (3 × 10 12 ) ионов углерода-12 с энергией 73 МэВ в секунду в течение десяти минут может привести к образованию около 1200 атомов нобелия-255. [72]
После получения нобелия-255 его можно выделить так же, как это используется для очистки соседнего актинида менделевия. Импульс отдачи образующихся атомов нобелия-255 используется для того, чтобы перенести их физически далеко от мишени, из которой они производятся, перенося их на тонкую металлическую фольгу (обычно бериллий , алюминий , платину или золото ) сразу за мишенью. в вакууме: обычно это сочетается с улавливанием атомов нобелия в газовой атмосфере (часто гелия ) и переносом их вместе с газовой струей из небольшого отверстия в реакционной камере. Используя длинную капиллярную трубку и добавляя аэрозоли хлорида калия в газообразный гелий, атомы нобелия можно транспортировать на десятки метров . [75] Тонкий слой нобелия, собранный на фольге, можно затем удалить разбавленной кислотой, не растворяя фольгу полностью. [75] Затем нобелий можно выделить, используя его склонность к образованию двухвалентного состояния, в отличие от других трехвалентных актинидов: в обычно используемых условиях элюирования (бис-(2-этилгексил)фосфорная кислота (ДЭГФ) в качестве неподвижной органической фазы и 0,05 М соляной кислоты в качестве подвижной водной фазы или использования 3 М соляной кислоты в качестве элюента из колонок с катионообменной смолой), нобелий будет проходить через колонку и элюироваться, в то время как другие трехвалентные актиниды остаются в колонке. [75] Однако, если используется прямая «ловушка» золотой фольги, процесс осложняется необходимостью отделять золото с помощью анионообменной хроматографии перед выделением нобелия путем элюирования из хроматографических экстракционных колонок с использованием HDEHP. [75]