Четырехокись осмия (также оксид осмия(VIII) ) представляет собой химическое соединение с формулой OsO 4 . Это соединение примечательно множеством применений, несмотря на его токсичность и редкость осмия . Он также обладает рядом необычных свойств, одно из которых заключается в том, что это твердое вещество летучее . Соединение бесцветно, но большинство образцов имеют желтый цвет. [5] Скорее всего, это связано с наличием примеси OsO 2 желто-коричневого цвета. [6] В биологии его свойство связываться с липидами сделало его широко используемым красителем в электронной микроскопии.
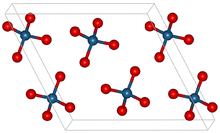
Оксид осмия(VIII) образует моноклинные кристаллы. [3] [7] Имеет характерный резкий запах, напоминающий хлор . Название элемента «осмий» происходит от слова «osme» , что по-гречески означает «запах» . OsO 4 летуч: он сублимирует при комнатной температуре . Он растворим в широком спектре органических растворителей. Умеренно растворим в воде, с которой обратимо реагирует с образованием осмиевой кислоты (см. ниже). [8] Чистый оксид осмия(VIII), вероятно, бесцветен; В [9] было высказано предположение, что его желтый оттенок обусловлен примесями диоксида осмия (OsO 2 ). [10] Молекула четырехокиси осмия тетраэдрическая и, следовательно, неполярная. Эта неполярность помогает OsO 4 проникать через заряженные клеточные мембраны. OsO 4 в 518 раз лучше растворяется в четыреххлористом углероде , чем в воде. [ нужна цитата ]
Осмий OsO 4 имеет степень окисления VIII; однако металл не обладает соответствующим зарядом 8+, поскольку связь в соединении носит в основном ковалентный характер ( энергия ионизации, необходимая для создания формального заряда 8+, также намного превышает энергии, доступные в обычных химических реакциях). Атом осмия имеет двойные связи с четырьмя оксидными лигандами , в результате чего образуется 16-электронный комплекс . Он изоэлектронен ионам перманганата и хромата .
OsO 4 образуется медленно, когда порошок осмия реагирует с O 2 при температуре окружающей среды. Реакция сыпучего вещества требует нагрева до 400 °С. [11]
Алкены присоединяются к OsO 4 с образованием диолатов , которые гидролизуются до цис -диолов. Конечный процесс называется дигидроксилированием. Это происходит посредством реакции циклоприсоединения [3 + 2] между OsO 4 и алкеном с образованием промежуточного сложного эфира осмата, который быстро гидролизуется с образованием вицинального диола . Поскольку атомы кислорода добавляются согласованно, в результате получается цис -стереохимия .
OsO 4 дорог и очень токсичен, что делает его непривлекательным реагентом для использования в стехиометрических количествах. Однако его реакции становятся каталитическими за счет добавления реоксидантов для повторного окисления побочного продукта Os (VI) обратно в Os (VIII). Типичные реагенты включают H 2 O 2 ( гидроксилирование по Миласу ), N-оксид N-метилморфолина ( дигидроксилирование по Апджону ) и K 3 Fe(CN) 6 /вода. Эти реоксиданты сами по себе не реагируют с алкенами. В качестве катализаторов можно использовать и другие соединения осмия, в том числе соли осмата(VI) ([OsO 2 (OH) 4 )] 2- и гидрат трихлорида осмия (OsCl 3 · x H 2 O). Эти виды окисляются до осмия (VIII) в присутствии таких окислителей. [12]
Основания Льюиса, такие как третичные амины и пиридины, увеличивают скорость дигидроксилирования. Это «лигандное ускорение» возникает за счет образования аддукта OsO 4 L, который быстрее присоединяется к алкену. Если амин хиральный, то дигидроксилирование может протекать с энантиоселективностью (см. Асимметричное дигидроксилирование по Шарплессу ). [13] OsO 4 не реагирует с большинством углеводов. [14]
Процесс можно расширить для получения двух альдегидов при окислении Лемье-Джонсона , в котором периодат используется для расщепления диола и регенерации каталитической загрузки OsO 4 . Этот процесс эквивалентен озонолизу .

OsO 4 представляет собой кислоту Льюиса и мягкий окислитель. Он реагирует с водным раствором щелочи с образованием перосмат-аниона OsO.
4(ОЙ)2−
2. [16] Этот вид легко восстанавливается до осмат- аниона OsO .
2(ОЙ)2−
4.
Когда основание Льюиса представляет собой амин , также образуются аддукты. Таким образом, OsO 4 может храниться в виде осмета , в котором OsO 4 находится в комплексе с уротропином . Осмет можно растворить в тетрагидрофуране (ТГФ) и разбавить водным буферным раствором , чтобы получить разбавленный (0,25%) рабочий раствор OsO 4 . [17]
С трет-BuNH 2 образуется имидопроизводное :
Аналогично с NH 3 получается нитридный комплекс :
Анион [Os(N)O 3 ] − изоэлектронен и изоструктурен OsO 4 .
OsO 4 хорошо растворим в трет-бутиловом спирте . В растворе он легко восстанавливается водородом до металлического осмия. Суспендированный металлический осмий можно использовать для катализа гидрирования широкого спектра органических химикатов, содержащих двойные или тройные связи.
OsO 4 подвергается «восстановительному карбонилированию» монооксидом углерода в метаноле при 400 К и 200 сбар с образованием треугольного кластера Os 3 (CO) 12 :
Осмий образует несколько оксофторидов, все из которых очень чувствительны к влаге. Фиолетовый цис -OsO 2 F 4 образуется при 77 К в безводном растворе HF : [18]
OsO 4 также реагирует с F 2 с образованием желтого OsO 3 F 2 : [19]
OsO 4 реагирует с одним эквивалентом [Me 4 N]F при 298 К и с 2 эквивалентами при 253 К: [11]
В органическом синтезе OsO 4 широко используется для окисления алкенов до вицинальных диолов путем присоединения двух гидроксильных групп с одной и той же стороны ( син-присоединение ). См. реакцию и механизм выше. Эту реакцию можно сделать как каталитической ( дигидроксилирование Апджона ), так и асимметричной ( асимметричное дигидроксилирование Шарплесса ).
Оксид осмия (VIII) также используется в каталитических количествах при оксиаминировании Шарплесса с получением вицинальных аминоспиртов.
В сочетании с периодатом натрия OsO 4 используется для окислительного расщепления алкенов ( окисление Лемье-Джонсона ), когда периодат служит как для расщепления диола, образующегося в результате дигидроксилирования, так и для повторного окисления OsO 3 обратно в OsO 4 . Чистая трансформация идентична трансформации, происходящей при озонолизе . Ниже приведен пример полного синтеза изостевиола. [20]
OsO 4 — широко используемый краситель , используемый в просвечивающей электронной микроскопии (ПЭМ) для обеспечения контрастности изображения. [21] Этот метод окрашивания также может быть известен в литературе как метод ОТО [22] [23] (осмий-тиокарбогидразид-осмий), метод пропитки осмием [24] или просто как окрашивание осмием. В качестве липидного пятна он также полезен в сканирующей электронной микроскопии (СЭМ) в качестве альтернативы напылению . Он внедряет тяжелый металл непосредственно в клеточные мембраны, создавая высокую скорость рассеяния электронов без необходимости покрытия мембраны слоем металла, который может скрыть детали клеточной мембраны. При окрашивании плазматической мембраны оксид осмия (VIII) связывает головные области фосфолипидов , создавая тем самым контраст с соседней протоплазмой (цитоплазмой). Кроме того, оксид осмия(VIII) также используется для фиксации биологических образцов в сочетании с HgCl 2 . Его способности к быстрому убийству используются для быстрого убийства живых особей, таких как простейшие. OsO 4 стабилизирует многие белки, превращая их в гели без разрушения структурных особенностей. Тканевые белки, стабилизированные OsO 4 , не коагулируются спиртами при дегидратации. [14] Оксид осмия (VIII) также используется в качестве красителя для липидов в оптической микроскопии. [25] OsO 4 также окрашивает роговицу человека (см. соображения безопасности).

Его также преимущественно используют для окрашивания сополимеров , наиболее известным примером являются блок-сополимеры, где можно окрасить одну фазу, чтобы показать микроструктуру материала . Например, блок-сополимеры стирола и бутадиена имеют центральную полибутадиеновую цепь с полистироловыми концевыми концами. При обработке OsO 4 бутадиеновая матрица реагирует преимущественно и таким образом поглощает оксид. Присутствия тяжелого металла достаточно, чтобы заблокировать электронный луч, поэтому домены полистирола ясно видны в тонких пленках в ПЭМ .
OsO 4 является промежуточным продуктом при извлечении осмия из руд. Осмийсодержащие остатки обрабатывают пероксидом натрия (Na 2 O 2 ) с образованием растворимого Na 2 [OsO 4 (OH) 2 ). При воздействии хлора эта соль дает OsO 4 . На заключительных стадиях переработки сырой OsO 4 растворяют в спиртовом NaOH с образованием Na 2 [OsO 2 (OH) 4 ), который при обработке NH 4 Cl дает (NH 4 ) 4 [OsO 2 Cl 2 ]. Эта соль восстанавливается под водородом с образованием осмия. [8]
OsO 4 позволил подтвердить модель футбольного мяча бакминстерфуллерена , 60-атомного аллотропа углерода . Аддуктом , образовавшимся из производного OsO 4 , стал C 60 (OsO 4 )(4 - трет - бутилпиридин ) 2 . Аддукт нарушил симметрию фуллерена, что позволило провести кристаллизацию и подтвердить структуру C 60 с помощью рентгеновской кристаллографии . [26]
Единственное известное клиническое применение тетраоксида осмия — для лечения артрита. [27] Отсутствие сообщений о долгосрочных побочных эффектах от местного применения тетроксида осмия (OsO 4 ) позволяет предположить, что осмий сам по себе может быть биосовместимым , хотя это зависит от вводимого соединения осмия.

OsO 4 необратимо окрашивает роговицу человека , что может привести к слепоте. Допустимый предел воздействия оксида осмия(VIII) (средневзвешенное по времени за 8 часов) составляет 2 мкг/м 3 . [7] Оксид осмия(VIII) может проникать через пластик и упаковку пищевых продуктов, поэтому его следует хранить в стеклянной упаковке в холодильнике. [14]