В химии периодические тенденции — это определенные закономерности, присутствующие в периодической таблице , которые иллюстрируют различные аспекты определенных элементов , сгруппированных по периодам и/или группам . Они были открыты русским химиком Дмитрием Менделеевым в 1863 году. Основные периодические тенденции включают атомный радиус , энергию ионизации , сродство к электрону , электроотрицательность , валентность и металлический характер . Эти тенденции существуют из-за схожих электронных конфигураций элементов внутри соответствующих групп или периодов; они отражают периодическую природу элементов. Эти тенденции дают качественную оценку свойств каждого элемента. [1] [2]
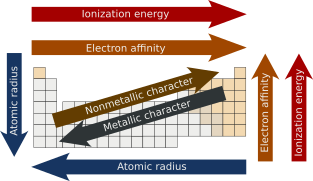
Атомный радиус — это расстояние от атомного ядра до крайней электронной орбитали в атоме . В общем, атомный радиус уменьшается по мере движения слева направо в периоде и увеличивается, когда мы спускаемся по группе. Это связано с тем, что в периоды валентные электроны находятся в одной и той же внешней оболочке. Атомный номер увеличивается за тот же период при движении слева направо, что, в свою очередь, увеличивает эффективный заряд ядра . Увеличение сил притяжения уменьшает атомный радиус элементов. Когда мы двигаемся вниз по группе, радиус атома увеличивается за счет добавления новой оболочки. [3] [4]
Энергия ионизации — это минимальное количество энергии, которое должен поглотить электрон в газообразном атоме или ионе, чтобы выйти из-под влияния притягивающей силы ядра. Его еще называют потенциалом ионизации. Первая энергия ионизации — это количество энергии, необходимое для отрыва первого электрона от нейтрального атома. Энергия, необходимая для отрыва второго электрона от нейтрального атома, называется второй энергией ионизации и так далее. [5]
В тренде, при движении слева направо по периоду современной таблицы Менделеева, энергия ионизации увеличивается по мере увеличения заряда ядра и уменьшения размера атома. Уменьшение размера атома приводит к более мощной силе притяжения между электронами и ядром. Однако предположим, что кто-то движется вниз в группе. В этом случае энергия ионизации уменьшается по мере увеличения размера атома из-за добавления валентной оболочки, тем самым уменьшая притяжение ядра к электронам. [6] [7]
Энергия, выделяющаяся при присоединении электрона к нейтральному газообразному атому с образованием аниона, называется сродством к электрону. [8] В соответствии с тенденцией, по мере продвижения слева направо в течение периода, сродство к электрону будет увеличиваться по мере увеличения заряда ядра и уменьшения размера атома, что приводит к более мощной силе притяжения ядра и добавленного электрона. Однако предположим, что кто-то движется вниз в группе. В этом случае сродство к электрону будет уменьшаться по мере увеличения размера атома из-за добавления валентной оболочки, тем самым уменьшая притяжение ядра к электронам. Хотя может показаться, что фтор должен иметь наибольшее сродство к электрону, его небольшой размер вызывает достаточное отталкивание между электронами, в результате чего хлор имеет самое высокое сродство к электрону в семействе галогенов . [9]
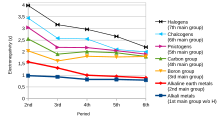
Склонность атома в молекуле притягивать к себе общую пару электронов называется электроотрицательностью. Это безразмерное свойство, поскольку это всего лишь тенденция. [10] Наиболее часто используемая шкала для измерения электроотрицательности была разработана Лайнусом Полингом . В его честь шкала была названа шкалой Полинга . Согласно этой шкале, фтор является наиболее электроотрицательным элементом, а цезий — наименее электроотрицательным элементом. [11]
В тренде, при движении слева направо по периоду современной таблицы Менделеева, электроотрицательность увеличивается по мере увеличения заряда ядра и уменьшения размера атома. Однако, если кто-то движется вниз в группе, электроотрицательность уменьшается по мере увеличения размера атома из-за добавления валентной оболочки, тем самым уменьшая притяжение атома к электронам. [12]
Однако в группе XIII ( семейство боров ) электроотрицательность сначала уменьшается от бора к алюминию , а затем увеличивается по группе. Это связано с тем, что размер атома увеличивается по мере продвижения вниз по группе, но в то же время эффективный заряд ядра увеличивается из-за плохой экранировки внутренних d- и f-электронов. В результате сила притяжения ядра для электронов увеличивается и, следовательно, электроотрицательность увеличивается от алюминия к таллию . [13] [14]
Валентность элемента — это количество электронов, которое атом должен потерять или приобрести, чтобы получить стабильную электронную конфигурацию . Проще говоря, это мера комбинационной способности элемента образовывать химические соединения . Электроны, находящиеся во внешней оболочке, обычно называются валентными электронами; количество валентных электронов определяет валентность атома. [15] [16]
По тренду при движении слева направо по периоду количество валентных электронов элементов увеличивается и варьируется от 1 до 8. Но валентность элементов сначала увеличивается от 1 до 4 , а затем уменьшается до нуля по мере достижения благородные газы . Однако по мере продвижения вниз по группе число валентных электронов обычно не меняется. Следовательно, во многих случаях элементы определенной группы имеют одинаковую валентность . Однако эта периодическая тенденция не всегда соблюдается для более тяжелых элементов, особенно для f-блока и переходных металлов . Эти элементы обладают переменной валентностью , поскольку у этих элементов есть d-орбиталь в качестве предпоследней орбитали и s-орбиталь в качестве самой внешней орбитали. Энергии этих (n-1)d и ns-орбиталей (например, 4d и 5s) относительно близки. [17] [18]
Металлические свойства обычно увеличиваются по группам, поскольку уменьшение притяжения между ядрами и внешними электронами приводит к тому, что эти электроны становятся более слабо связанными и, следовательно, способны проводить тепло и электричество. В течение каждого периода, слева направо, возрастающее притяжение между ядрами и внешними электронами приводит к уменьшению металлического характера . Напротив, неметаллический характер уменьшается по группам и увеличивается по периодам. [19] [20]