В материаловедении полиморфизм описывает явление, при котором соединение или элемент может кристаллизоваться в более чем одну кристаллическую структуру . Предыдущее определение развивалось на протяжении многих лет и все еще обсуждается сегодня. [1] [2] [3] Обсуждение определяющих характеристик полиморфизма включает в себя различие между типами переходов и структурных изменений, происходящих при полиморфизме, по сравнению с таковыми в других явлениях.
Полезно также отметить, что материалы с двумя полиморфными фазами можно назвать диморфными , с тремя полиморфными фазами — триморфными и т. д. [4]
Фазовые переходы (фазовые изменения), которые помогают описать полиморфизм, включают полиморфные переходы, а также переходы плавления и испарения. Согласно ИЮПАК , полиморфный переход — это «обратимый переход твердой кристаллической фазы при определенной температуре и давлении (точка инверсии) в другую фазу того же химического состава с другой кристаллической структурой». [5] Кроме того, Уолтер Маккроун описал фазы в полиморфном веществе как «разные по кристаллической структуре, но идентичные в жидком или парообразном состояниях». Маккроун также определяет полиморфную модификацию как «кристаллическую фазу данного соединения, возникающую в результате возможности по крайней мере двух различных расположений молекул этого соединения в твердом состоянии». [6] [7] Эти определяющие факты подразумевают, что полиморфизм включает изменения физических свойств, но не может включать химические изменения. Некоторые ранние определения не делают этого различия.
Устранение химических изменений из тех изменений, которые допустимы во время полиморфного перехода, определяет полиморфизм. Например, изомеризация часто может приводить к полиморфным переходам. Однако таутомерия (динамическая изомеризация) приводит к химическим изменениям, а не к полиморфизму. [1] Кроме того, аллотропия элементов и полиморфизм исторически связаны. Однако аллотропы элемента не всегда являются полиморфами. Типичным примером являются аллотропы углерода , к которым относятся графит, алмаз и лондсдейлит. Хотя все три формы являются аллотропами, графит не является полиморфной модификацией алмаза и лондсдейлита. Причина в том, что графит химически отличен, имея гибридизованную связь sp 2 , тогда как алмаз и лондсдейлит химически идентичны, оба имеют гибридизованную связь sp 3 . Алмаз и лондсдейлит различаются по своей кристаллической структуре, но не различаются химически. [2] Изомеризация и аллотропия — это лишь два явления, связанных с полиморфизмом. Дополнительную информацию о выявлении полиморфизма и отличии его от других явлений см. в обзоре Brog et. ал. [2]
Полиморфизм имеет практическое значение для фармацевтических препаратов , агрохимикатов , пигментов , красителей , пищевых продуктов и взрывчатых веществ .
Ранние записи об открытии полиморфизма приписывают Эйльхарду Мицерлиху и Йонсу Якобу Берцелиусу исследования фосфатов и арсенатов в начале 1800-х годов. Исследования включали измерение межфазных углов кристаллов, чтобы показать, что химически идентичные соли могут иметь две разные формы. Мицерлих первоначально назвал это открытие изоморфизмом. [8] Измерение плотности кристаллов также использовалось Вильгельмом Оствальдом и выражалось в коэффициенте Оствальда. [9]
Развитие микроскопа расширило возможности наблюдения за полиморфизмом и помогло исследованиям Морица Людвига Франкенхайма в 1830-х годах. Он смог продемонстрировать методы, вызывающие фазовые изменения кристаллов, и формально обобщил свои выводы о природе полиморфизма. Вскоре после этого вошел в употребление более сложный поляризационный световой микроскоп , который обеспечил лучшую визуализацию кристаллических фаз, позволив кристаллографам различать различные полиморфные модификации. Горячий столик был изобретен и установлен на поляризационном световом микроскопе Отто Леманном примерно в 1877 году. Это изобретение помогло кристаллографам определять точки плавления и наблюдать полиморфные переходы. [8]
Хотя использование микроскопов с горячим столиком продолжалось на протяжении 1900-х годов, тепловые методы также стали широко использоваться для наблюдения теплового потока, который возникает во время фазовых изменений, таких как плавление и полиморфные переходы. Один из таких методов, дифференциальная сканирующая калориметрия (ДСК), продолжает использоваться для определения энтальпии полиморфных переходов. [8]
В 20 веке рентгеновская кристаллография стала широко использоваться для изучения кристаллической структуры полиморфных модификаций. Для измерения кристаллической элементарной ячейки используются методы дифракции рентгеновских лучей на монокристалле и порошковой рентгеновской дифракции. Каждая полиморфная модификация соединения имеет уникальную кристаллическую структуру. В результате разные полиморфы будут давать разные картины дифракции рентгеновских лучей. [8]
Методы колебательной спектроскопии стали использоваться для исследования полиморфизма во второй половине двадцатого века и стали более широко использоваться по мере совершенствования оптических, компьютерных и полупроводниковых технологий. Эти методы включают инфракрасную (ИК) спектроскопию , терагерцовую спектроскопию и спектроскопию комбинационного рассеяния света . Среднечастотная ИК- и рамановская спектроскопия чувствительны к изменениям структуры водородных связей . Такие изменения впоследствии могут быть связаны со структурными различиями. Кроме того, терагерцовая и низкочастотная рамановская спектроскопия выявляют колебательные моды, возникающие в результате межмолекулярных взаимодействий в кристаллических твердых телах. Опять же, эти моды колебаний связаны с кристаллической структурой и могут использоваться для выявления различий в трехмерной структуре полиморфов. [10]
Вычислительная химия может использоваться в сочетании с методами колебательной спектроскопии, чтобы понять происхождение вибраций внутри кристаллов. [10] Сочетание методов дает подробную информацию о кристаллических структурах, аналогичную тому, что можно получить с помощью рентгеновской кристаллографии. Помимо использования вычислительных методов для улучшения понимания спектроскопических данных, последней разработкой в области выявления полиморфизма в кристаллах является область прогнозирования кристаллической структуры . Этот метод использует вычислительную химию для моделирования образования кристаллов и прогнозирования существования определенных полиморфных модификаций соединения до того, как они будут обнаружены учеными экспериментально. [11] [12]
Многие соединения обладают полиморфизмом. Утверждалось, что «каждое соединение имеет разные полиморфные формы и что, как правило, количество форм, известных для данного соединения, пропорционально времени и деньгам, затраченным на исследование этого соединения». [13] [6] [14]
Явление было открыто в 1832 году Фридрихом Вёлером и Юстусом фон Либихом . Они заметили, что шелковистые иглы свежекристаллизованного бензамида медленно превращались в ромбические кристаллы. [15] Современный анализ [16] идентифицирует три полиморфа бензамида: наименее стабильным, образующимся при мгновенном охлаждении, является ромбическая форма II. За этим типом следует моноклинная форма III (наблюденная Вёлером/Либихом). Наиболее устойчивой формой является моноклинная форма I. Механизмы водородных связей одинаковы для всех трех фаз; однако они сильно различаются по своим пи-пи-взаимодействиям.
В 2006 году , через 124 года после изучения первой кристаллической формы, был открыт новый полиморф малеиновой кислоты . [17] Малеиновая кислота производится в промышленных масштабах в химической промышленности. Он образует соли, используемые в медицине. Новый тип кристаллов получается, когда сокристалл кофеина и малеиновой кислоты (2: 1 ) растворяется в хлороформе и когда растворителю дают медленно испаряться. В то время как форма I имеет моноклинную пространственную группу P 2 1 / c , новая форма имеет пространственную группу Pc . Обе полиморфные модификации состоят из листов молекул, соединенных водородными связями групп карбоновой кислоты : в форме I листы чередуются по суммарному дипольному моменту , а в форме II листы ориентированы в одном направлении.
После 125 лет исследований 1,3,5-тринитробензол дал вторую полиморфную модификацию. Обычная форма имеет пространственную группу Pbca , но в 2004 году была получена вторая полиморфная модификация в пространственной группе Pca 2 1 , когда соединение кристаллизовали в присутствии добавки тризиндана. Этот эксперимент показывает, что добавки могут вызывать появление полиморфных форм. [18]
Акридин получен в виде восьми полиморфов [19] , а арипипразол – в девяти. [20] Рекорд по наибольшему количеству хорошо охарактеризованных полиморфов принадлежит соединению, известному как ROY . [21] [22] Глицин кристаллизуется в виде моноклинных и гексагональных кристаллов . Полиморфизм органических соединений часто является результатом конформационного полиморфизма . [23]
Полиморфизм бинарных оксидов металлов привлек большое внимание, поскольку эти материалы имеют значительную экономическую ценность. Один набор известных примеров имеет состав SiO 2 , который образует множество полиморфов. Важные из них включают: α-кварц , β-кварц , тридимит , кристобалит , моганит , коэсит и стишовит . [24] [25]
Классическими примерами полиморфизма являются пара минералов кальцит и арагонит , оба являются формами карбоната кальция .
β-HgS выпадает в осадок в виде черного твердого вещества при обработке солей Hg(II) H 2 S. При осторожном нагревании суспензии черный полиморф превращается в красную форму. [27]
Согласно правилу Оствальда , обычно менее стабильные полиморфы кристаллизуются раньше стабильной формы. Эта концепция основана на идее о том, что нестабильные полиморфы более похожи на состояние в растворе и, следовательно, имеют кинетические преимущества. Этот случай иллюстрирует основополагающий случай волокнистого и ромбического бензамида. Другой пример – две полиморфные модификации диоксида титана . [26] Тем не менее, существуют известные системы, такие как метацетамол , где только узкая скорость охлаждения способствует получению метастабильной формы II. [28]
Полиморфы обладают разной стабильностью. Некоторые быстро конвертируются при комнатной (или любой) температуре. Большинство полиморфов органических молекул различаются по энергии решетки всего на несколько кДж/моль. Примерно 50% известных пар полиморфов различаются менее чем на 2 кДж/моль, а различия в стабильности более 10 кДж/моль встречаются редко. [29] Стоит отметить, что стабильность полиморфа может меняться в зависимости от температуры [30] [31] [32] или давления. [33] [34] Важно отметить, что структурная и термодинамическая стабильность различны. Термодинамическую стабильность можно изучать с помощью экспериментальных или вычислительных методов. [35] [36]
На полиморфизм влияют детали кристаллизации . Растворитель во всех отношениях влияет на природу полиморфа, включая концентрацию других компонентов растворителя, т.е. видов, ингибирующих или способствующих определенным закономерностям роста. [37] Решающим фактором часто является температура растворителя, из которого проводится кристаллизация . [38]
Метастабильные полиморфы не всегда получаются воспроизводимо, что приводит к случаям « исчезновения полиморфов », что обычно имеет негативные последствия для права и бизнеса. [13] [11] [39]
Лекарства получают одобрение регулирующих органов и получают патенты только на одну полиморфную модификацию.
В классическом патентном споре GlaxoSmithKline защитила свой патент на полиморф типа II активного ингредиента Zantac от конкурентов, в то время как срок действия полиморфа типа I уже истек. [40]
Полиморфизм в лекарствах также может иметь прямые медицинские последствия, поскольку скорость растворения зависит от полиморфа. Полиморфную чистоту образцов лекарственных средств можно проверить с помощью таких методов, как порошковая рентгеновская дифракция, ИК/рамановская спектроскопия, а также в некоторых случаях используя различия в их оптических свойствах. [41]
Известные случаи до 2015 года обсуждаются в обзорной статье Бучара, Ланкастера и Бернштейна. [11]
Дибензоксазепины
Междисциплинарные исследования с использованием экспериментальных и вычислительных подходов были применены к фармацевтическим молекулам, чтобы облегчить сравнение их твердотельных структур. В частности, это исследование было сосредоточено на изучении того, как изменения в молекулярной структуре влияют на молекулярную конформацию, мотивы упаковки, взаимодействия в образующихся кристаллических решетках и степень разнообразия этих соединений в твердом состоянии. Результаты подчеркивают ценность исследований по прогнозированию кристаллической структуры и расчетов PIXEL для интерпретации наблюдаемого поведения твердого тела, количественной оценки межмолекулярных взаимодействий в упакованных структурах и выявления ключевых стабилизирующих взаимодействий. Экспериментальный скрининг выявил 4 физические формы клозапина по сравнению с 60 различными физическими формами оланзапина . Результаты экспериментального скрининга клозапина согласуются с его энергетическим ландшафтом, который подтверждает, что никакая альтернативная упаковка не является термодинамически конкурентоспособной по отношению к экспериментально полученной структуре. В то время как в случае оланзапина энергетический ландшафт кристаллов подчеркивает, что обширный экспериментальный скрининг, вероятно, не обнаружил всех возможных полиморфов оланзапина , и дальнейшее разнообразие твердых форм может быть нацелено на лучшее понимание роли кинетики в его кристаллизации. Исследования CSP смогли предложить объяснение отсутствия центросимметричного димера в безводном клозапине . PIXEL-расчеты всех кристаллических структур клозапина показали, что, как и в случае с оланзапином , в энергии межмолекулярного взаимодействия в каждой структуре также доминирует Ed. Несмотря на сходство молекулярной структуры амоксапина и локсапина (молекулы группы 2), кристаллическая упаковка, наблюдаемая у полиморфов локсапина, существенно отличается от амоксапина . Совместное экспериментальное и вычислительное исследование показало, что метильная группа в локсапине оказывает значительное влияние на увеличение диапазона доступных твердых форм и предпочтение различным альтернативным вариантам упаковки. Исследования CSP снова помогли объяснить наблюдаемое разнообразие локсапина и амоксапина в твердом состоянии. Расчеты PIXEL показали, что в отсутствие сильных Н-связей ключевую роль в стабилизации кристаллической решетки обеих молекул играют слабые Н-связи, такие как C–H…O, C–H…N и дисперсионные взаимодействия. Эффективная кристаллическая упаковка амоксапина, по-видимому, способствует его мономорфному поведению по сравнению со сравнительно менее эффективной упаковкой локсапина .молекулы в обеих полиморфах. Сочетание экспериментальных и вычислительных подходов позволило глубже понять факторы, влияющие на твердотельную структуру и разнообразие этих соединений. Поверхности Хиршфельда с использованием Crystal Explorer представляют собой еще один способ изучения режимов упаковки и межмолекулярных взаимодействий в молекулярных кристаллах. Влияние изменений малых заместителей на форму и распределение электронов также можно исследовать путем сопоставления общей электронной плотности с электростатическим потенциалом молекул в газовой фазе. Это позволяет легко визуализировать и сравнивать общую форму, богатые электронами и электронодефицитные области внутри молекул. Форму этих молекул можно дополнительно исследовать, чтобы изучить ее влияние на разнообразие твердого тела. [42]
Позаконазол
Оригинальные препараты позаконазола, представленные на рынке под лицензией Noxafil (R), были составлены с использованием формы I позаконазола . Открытие полиморфов позаконазола быстро росло и привело к большому количеству исследований в области кристаллографии позаконазола . Сольват метанола и сокристалл 1,4-диоксана были добавлены в Кембриджскую структурную базу данных (CSD). [43]
Противовирусный препарат ритонавир существует в виде двух полиморфов, сильно различающихся по эффективности. Такие проблемы были решены путем переформулирования препарата в гелевые капсулы и таблетки, а не в оригинальные капсулы. [44]
Был только один доказанный полиморф формы I аспирина , хотя существование другого полиморфа обсуждалось с 1960-х годов, и в одном отчете 1981 года сообщалось, что при кристаллизации в присутствии ангидрида аспирина дифрактограмма аспирина имеет слабые дополнительные пики. Хотя в то время его считали простой примесью, в ретроспективе это был аспирин формы II . [11]
Форма II была обнаружена в 2005 году [45] [46] после попытки совместной кристаллизации аспирина и леветирацетама из горячего ацетонитрила .
В форме I пары молекул аспирина образуют центросимметричные димеры через ацетильные группы с (кислотным) метильным протоном к карбонильным водородным связям . В форме II каждая молекула аспирина образует такие же водородные связи, но с двумя соседними молекулами вместо одной. По водородным связям, образованным карбоксильными группами , обе полиморфные модификации образуют идентичные димерные структуры. Полиморфы аспирина содержат идентичные двумерные участки и поэтому более точно описываются как политипы. [47]
Чистый аспирин формы II можно получить путем внесения в партию безводного аспирина в концентрации 15% по массе. [11]
Порошок парацетамола имеет плохие компрессионные свойства, что затрудняет изготовление таблеток. Был найден второй полиморф с более подходящими сжимающими свойствами. [48]
Ацетат кортизона существует как минимум в пяти различных полиморфах, четыре из которых нестабильны в воде и переходят в стабильную форму.
Карбамазепин , эстроген , пароксетин [49] и хлорамфеникол также демонстрируют полиморфизм.
Пиразинамид имеет как минимум 4 полиморфа. [50] Все они переходят в стабильную α-форму при комнатной температуре при хранении или механической обработке. [51] Недавние исследования доказывают, что α-форма термодинамически стабильна при комнатной температуре. [30] [32]
Политипы — это особый случай полиморфов, когда несколько плотноупакованных кристаллических структур различаются только в одном измерении. Политипы имеют одинаковые плотноупакованные плоскости, но различаются последовательностью укладки в третьем измерении, перпендикулярном этим плоскостям. Карбид кремния (SiC) имеет более 170 известных политипов , хотя большинство из них редки. Все политипы SiC имеют практически одинаковую плотность и свободную энергию Гиббса . Наиболее распространенные политипы SiC представлены в таблице 1.
Таблица 1 : Некоторые политипы SiC. [52]
Вторая группа материалов с различными политипами — это дихалькогениды переходных металлов , слоистые материалы, такие как дисульфид молибдена (MoS 2 ). Для этих материалов политипы оказывают более отчетливое влияние на свойства материала, например, для MoS 2 политип 1T имеет металлический характер, тогда как форма 2H является более полупроводниковой. [53] Другим примером является дисульфид тантала , где встречаются общие политипы 1T и 2H, а также более сложные типы «смешанной координации», такие как 4Hb и 6R, где смешаны тригонально-призматические и октаэдрические геометрические слои. [54] Здесь политип 1T демонстрирует волну зарядовой плотности с явным влиянием на проводимость в зависимости от температуры, тогда как политип 2H демонстрирует сверхпроводимость .
ZnS и CdI 2 также политипичны. [55] Было высказано предположение, что этот тип полиморфизма обусловлен кинетикой, при которой винтовые дислокации быстро периодически воспроизводят частично неупорядоченные последовательности.
_and_monotropic_behaviour_(right)..jpg/440px-Energy-Temperature_diagrams_of_a_system_exhibiting_two_polymorphic_forms_with_enantiotropic_behaviour_(left)_and_monotropic_behaviour_(right)..jpg)
С точки зрения термодинамики выделяют два типа полиморфного поведения. Для монотропной системы графики зависимости свободной энергии различных полиморфов от температуры не пересекаются до того, как все полиморфы расплавятся. В результате любой переход от одной полиморфной модификации к другой ниже температуры плавления будет необратимым. Для энантиотропной системы график зависимости свободной энергии от температуры показывает точку пересечения перед различными точками плавления. [56] Также возможно взаимозаменяемое преобразование между двумя полиморфными модификациями путем нагревания или охлаждения или посредством физического контакта с полиморфной модификацией с более низкой энергией.
Простая модель полиморфизма заключается в моделировании свободной энергии Гиббса шарообразного кристалла как . Здесь первое слагаемое — это поверхностная энергия, а второе — объемная энергия. Оба параметра . Функция возрастает до максимума, а затем падает, пересекая ноль в точке . Чтобы кристаллизоваться, хрустальный шар преодолевает энергетический барьер на пути к части энергетического ландшафта. [57]
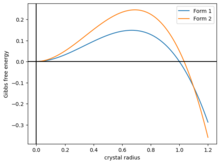
Теперь предположим, что существуют два типа кристаллов с разными энергиями и , и если они имеют ту же форму, что и на рисунке 2, то две кривые пересекаются в некоторой точке . Тогда система имеет три фазы:
Если кристалл выращивать медленно, он может кинетически застрять в форме 1.